Clear Sky Science · ru
Ассоциированный с купроптозом PDHA1 способствует прогрессированию сарком и чувствительности к иммунотерапии через ось E2F1–PD-L1: исследование с использованием мультиомики и клинической валидации
Почему это исследование важно
Саркомы — редкие, но агрессивные опухоли, которые часто устойчи́вы к современным иммунным методам лечения. У многих пациентов с распространённой болезнью исчерпываются стандартные опции, такие как операция, химио‑ и лучевая терапия, и при этом прогноз остаётся неблагоприятным. В этом исследовании изучается скрытый метаболический переключатель в клетках саркомы, который, по-видимому, одновременно подпитывает рост опухоли и формирует иммунный ответ. Понимание этого переключателя может открыть новые пути для прогнозирования того, какие пациенты получат пользу от иммунотерапии, и для разработки более разумных комбинированных подходов.
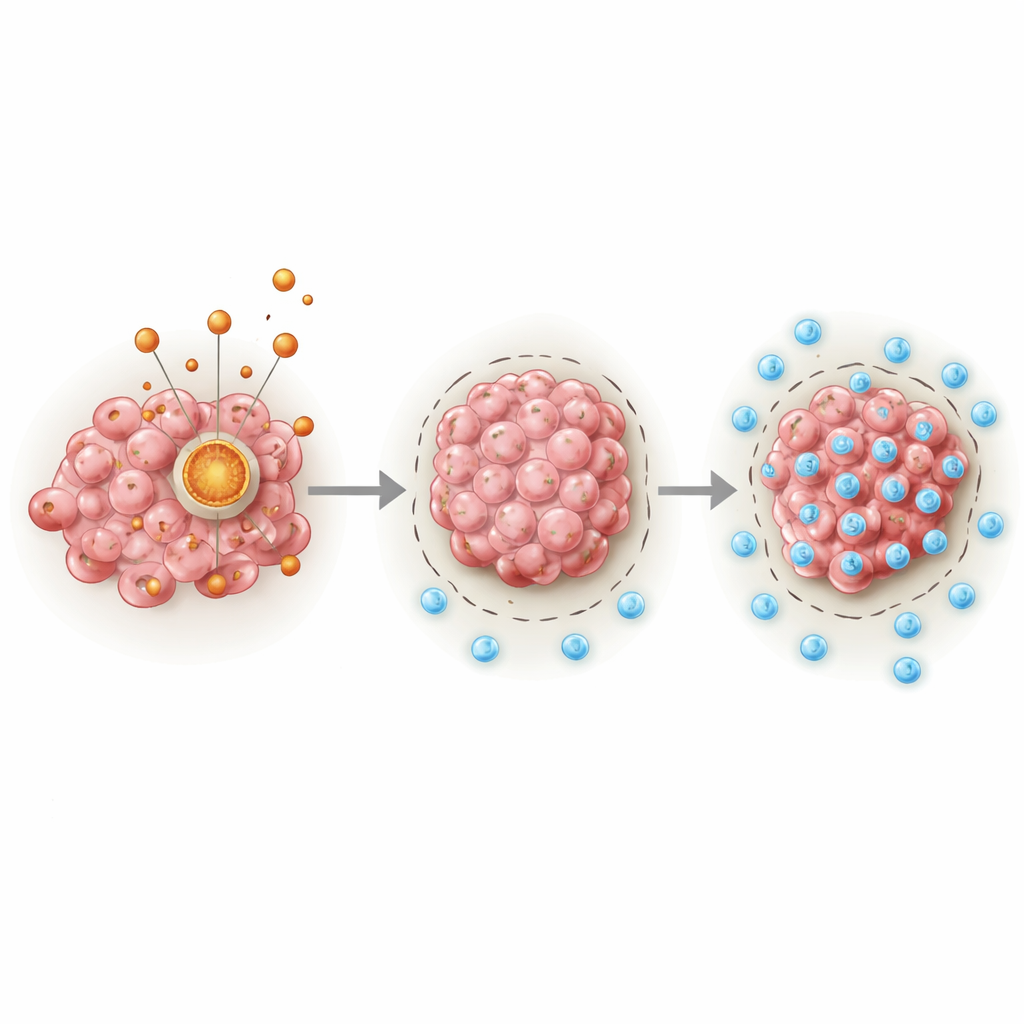
Скрытый двигатель внутри раковых клеток
В центре истории — PDHA1, белок, выполняющий роль ключевого шлюза между расщеплением сахаров и основным энергетическим циклом митохондрий. Авторы проанализировали большие онкологические базы данных и клинические образцы и обнаружили, что саркомы стабильно характеризуются повышенным уровнем PDHA1 по сравнению с нормальными тканями. У пациентов с опухолями, содержащими больше PDHA1, наблюдалась более короткая выживаемость независимо от возраста, пола и ряда других клинических факторов. Комбинируя уровень PDHA1 со стандартной клинической информацией, команда создала инструмент для прогнозирования, который точнее оценивал выживаемость на один, три и пять лет по сравнению с традиционными методами.
Как метаболизм формирует «соседство» опухоли
Помимо простого стимулирования роста, PDHA1, по-видимому, перестраивает микроокружение опухоли — совокупность иммунных и стромальных клеток вокруг рака. С помощью вычислительных методов, позволяющих выводить типы иммунных клеток по массовому РНК-профилю опухолей, а также с помощью одно‑клеточного секвенирования отдельных иммунных клеток, авторы показали, что PDHA1 активен не только в опухолевых, но и во множестве иммунных популяций, особенно в Т‑клетках и миелоидных клетках. Саркомы с высоким PDHA1 чаще демонстрировали признаки «иммунного исключения»: меньше эффективных киллерных Т‑клеток глубоко в опухоли, больше признаков плотного фиброзного стромы и шаблоны, указывающие на то, что иммунные клетки удерживаются на периферии и не могут атаковать.
Молекулярная цепочка, блокирующая иммунную атаку
Лабораторные эксперименты показали, как PDHA1 связывает метаболизм с уходом от иммунного надзора. При снижении уровня PDHA1 в клеточных линиях сарком клетки делились реже, меньше мигрировали, образовывали меньше колоний и чаще входили в программируемую гибель. Одновременно падали уровни E2F1 — ядерного регулятора генов, вовлечённых в деление клеток — и PD-L1 — иммунной «тормозной» молекулы на поверхности опухолевых клеток. Анализ публичных данных по связыванию ДНК и таргетные эксперименты показали, что E2F1 прямо связывается с регуляторным участком гена PD-L1 и активирует его. Восстановление E2F1 в клетках с дефицитом PDHA1 возвращало PD-L1 и частично восстанавливало выживание клеток, что помещает PDHA1 выше по потоку в цепочке E2F1–PD-L1, помогающей опухолям скрываться от Т‑клеток.
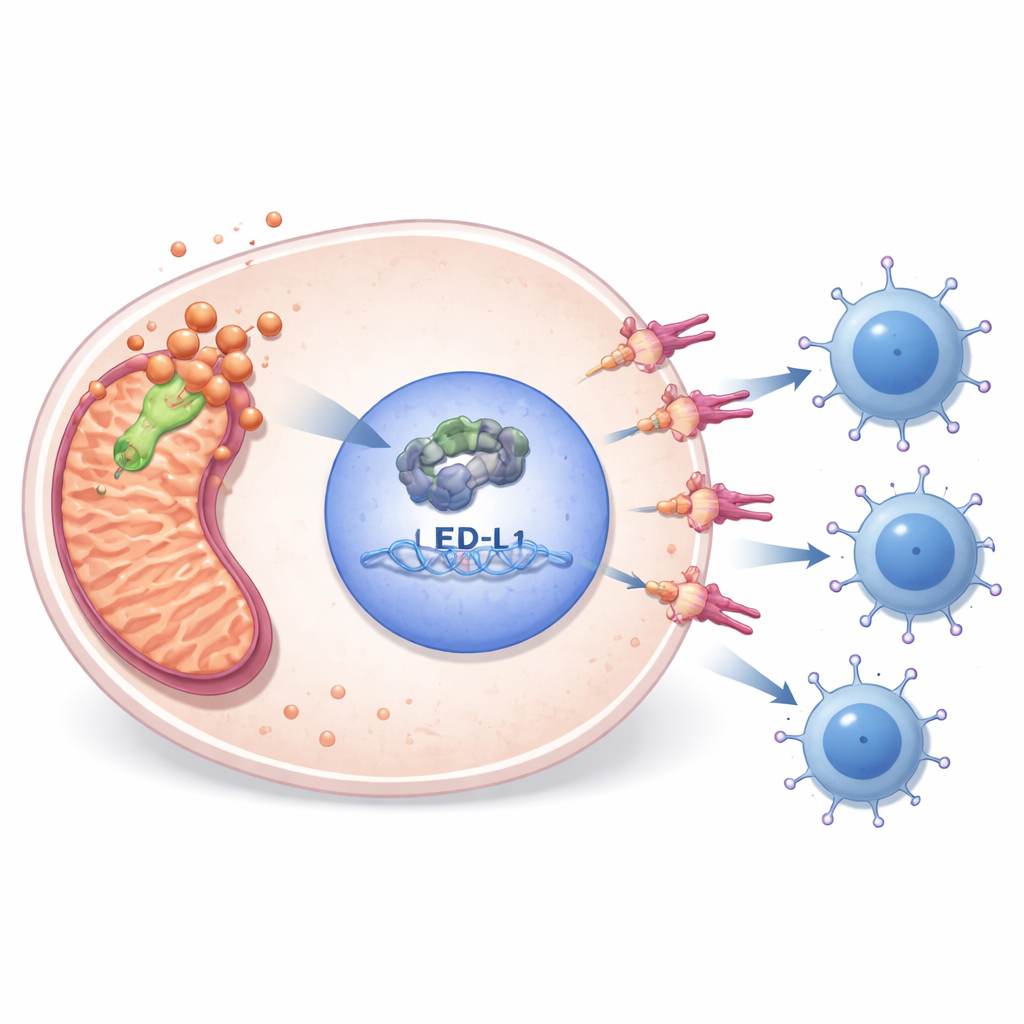
Связанная с медью гибель клеток и лекарственные возможности
PDHA1 также связан с недавно описанной формой смерти клеток, вызванной медью, называемой купроптозом. В исследовании показано, что блокада доступности меди с помощью препарата уменьшает уровень липоиллированного митохондриального белка, связанного с этим путём, и ослабляет цепочку PDHA1–E2F1–PD-L1, особенно в сочетании с нокаутом PDHA1. Геномные и эпигенетические анализы предполагали, что высокий PDHA1 часто совпадает с ДНК-изменениями, низкой метиляцией гена PDHA1 и паттернами РНК‑модификаций, ассоциированными с более агрессивными опухолями. Базы данных скрининга лекарств и клеточные тесты указали на ряд препаратов — например, метаболический агент фенформин и ингибитор пути E2F1 — к которым саркомы с активным PDHA1 могут быть особенно чувствительны, намекая на обоснованные комбинации с ингибиторами контрольных точек иммунитета.
Преобразование плохого прогноза в руководство по лечению
В экспериментах на животных и в биоптатах пациентов опухоли с высоким PDHA1 были крупнее, более пролиферативны, содержали больше PD-L1 и имели меньше инфильтрирующих CD8⁺ киллерных Т‑клеток. В то же время такие же опухоли демонстрировали признаки — например, более высокую нагрузку мутаций и усиленные сигналы контрольных точек — которые часто ассоциируются с лучшим ответом на блокаду PD-1 или PD-L1. В небольшой клинической когорте пациентов с продвинутой саркомой, получавших такую иммунотерапию, пациенты с высоким PDHA1 чаще получали пользу. Для неспециалиста вывод таков: PDHA1 выступает одновременно в роли педали газа для роста саркомы и щита против иммунной атаки, но это же поведение может сделать эти опухоли уязвимыми, когда применяются правильные «тормоза». Измерение и таргетинг PDHA1 может помочь выявить пациентов с высоким риском, направить использование иммунотерапии и вдохновить новые метаболико‑иммунные комбинации лекарств против упорных сарком.
Цитирование: Qin, H., Qi, T., Yao, N. et al. Cuproptosis-associated PDHA1 promotes sarcoma progression and immunotherapy responsiveness via the E2F1–PD-L1 axis: a multi-omics and clinical validation study. npj Precis. Onc. 10, 156 (2026). https://doi.org/10.1038/s41698-026-01298-0
Ключевые слова: иммунотерапия сарком, метаболизм рака, PDHA1, блокада иммунных контрольных точек, микроокружение опухоли