Clear Sky Science · de
Cuproptose‑assoziiertes PDHA1 fördert das Fortschreiten von Sarkomen und die Ansprechbarkeit auf Immuntherapie über die E2F1–PD‑L1‑Achse: eine Multi‑Omics‑ und klinische Validierungsstudie
Warum diese Forschung wichtig ist
Sarkome sind seltene, aber aggressive Tumoren, die häufig gegen moderne immunbasierte Behandlungen resistent sind. Viele Patientinnen und Patienten mit fortgeschrittener Erkrankung haben die standardmäßigen Optionen wie Operation, Chemotherapie und Strahlentherapie ausgeschöpft und haben dennoch eine schlechte Überlebensprognose. Diese Studie untersucht einen verborgenen Stoffwechsel‑Schalter in Sarkomzellen, der offenbar sowohl das Tumorwachstum antreibt als auch die Reaktion des Immunsystems beeinflusst. Das Verständnis dieses Schalters könnte neue Wege eröffnen, vorherzusagen, welche Patientinnen und Patienten von einer Immuntherapie profitieren, und intelligentere Kombinationsbehandlungen zu entwickeln.
Ein verborgener Motor in Krebszellen
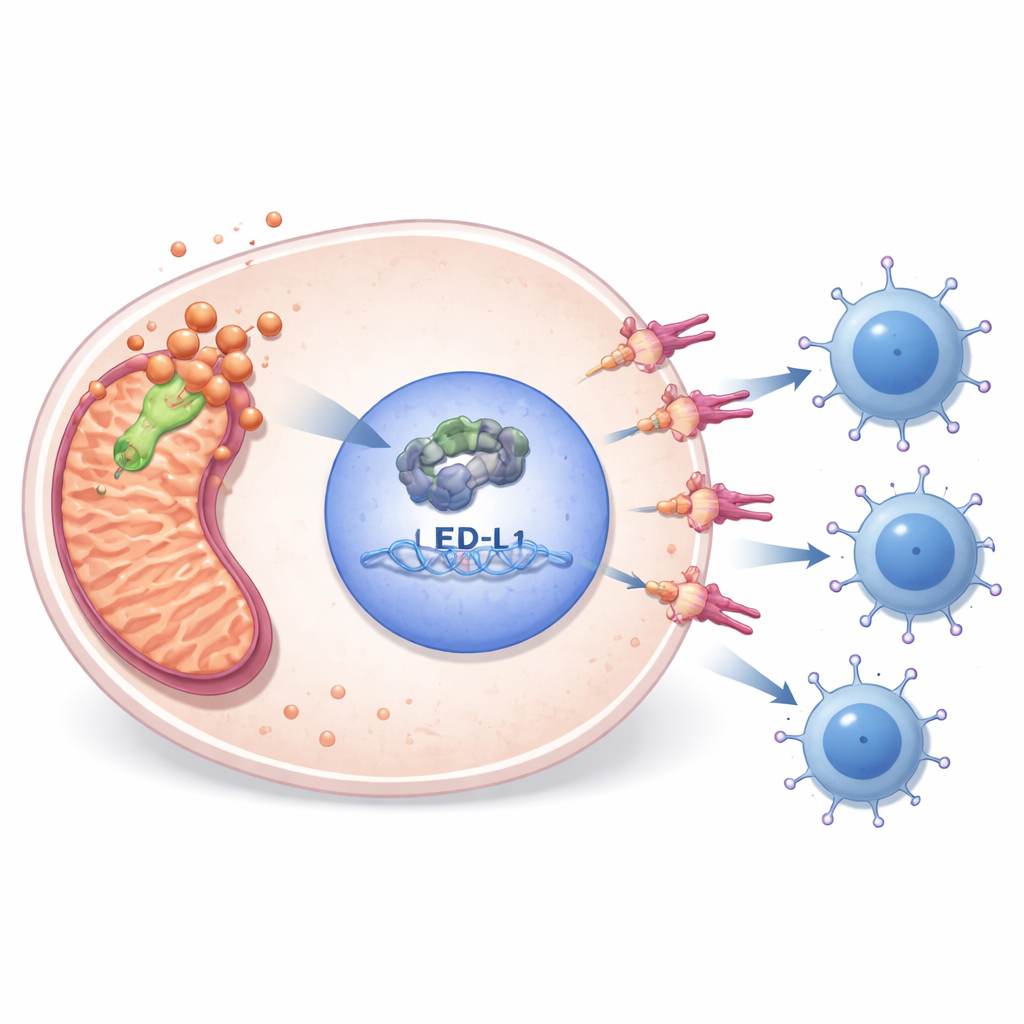
Zentral in dieser Geschichte steht PDHA1, ein Protein, das als wichtige Schaltstelle zwischen dem Zuckerabbau und dem zentralen Energiezyklus der Zelle in den Mitochondrien fungiert. Die Autoren analysierten umfangreiche Krebsdatenbanken und klinische Proben und fanden heraus, dass Sarkome durchgängig höhere PDHA1‑Spiegel aufweisen als normales Gewebe. Patientinnen und Patienten, deren Tumoren mehr PDHA1 enthielten, lebten tendenziell kürzer, unabhängig von Alter, Geschlecht oder mehreren anderen klinischen Faktoren. Durch die Kombination von PDHA1‑Werten mit standardmäßigen klinischen Informationen entwickelte das Team ein Vorhersagewerkzeug, das das Ein‑, Drei‑ und Fünfjahresüberleben genauer einschätzte als traditionelle Maße allein.
Wie der Stoffwechsel die Tumornachbarschaft formt
Über die reine Wachstumsförderung hinaus schien PDHA1 die Tumornachbarschaft — das Gemisch aus Immun‑ und Stützszellen um den Tumor herum — umzugestalten. Mit computergestützten Verfahren, die Immunzelltypen aus Bulk‑Tumor‑RNA ableiten, sowie Einzelzellsequenzierung individueller Immunzellen zeigten die Autoren, dass PDHA1 nicht nur in Tumorzellen aktiv ist, sondern auch in vielen Immunpopulationen, insbesondere in T‑Zellen und myeloiden Zellen. Sarkome mit hohem PDHA1 wiesen eher Merkmale eines „immun‑exkludierten“ Zustands auf: weniger hilfreiche Killer‑T‑Zellen tief im Tumor, mehr Anzeichen für steife, faserige Stroma und Muster, die darauf hindeuten, dass Immunzellen an den Rändern gehalten werden, statt eindringen zu können und anzugreifen.
Eine molekulare Kette, die den Immunangriff blockiert
Laborversuche zeigten, wie PDHA1 den Stoffwechsel mit der Immunflucht verbindet. Wenn die Forschenden PDHA1 in Sarkomzelllinien reduzierten, teilten sich die Zellen weniger, bewegten sich weniger, bildeten weniger Kolonien und durchliefen häufiger programmierter Zelltod. Gleichzeitig sanken die Spiegel von E2F1 — einem nukleären Regulator von Genen der Zellteilung — und von PD‑L1 — einer immunologischen „Bremse“ an der Oberfläche von Tumorzellen. Durch die Auswertung öffentlicher DNA‑Bindungsdaten und gezielte Experimente demonstrierte das Team, dass E2F1 direkt an die Kontrollregion des PD‑L1‑Gens bindet und dessen Aktivität steigert. Die Wiederherstellung von E2F1 in PDHA1‑defizienten Zellen hob PD‑L1 wieder an und rettete teilweise das Überleben der Zellen, wodurch PDHA1 als vorgelagerter Faktor einer E2F1–PD‑L1‑Kette verortet wird, die Tumoren hilft, sich vor T‑Zellen zu verbergen.
Kupfervermittelter Zelltod und therapeutische Chancen
PDHA1 steht außerdem in Verbindung mit einer kürzlich beschriebenen Form des Zelltods, die durch Kupfer ausgelöst wird und als Cuproptose bezeichnet wird. Die Studie zeigte, dass die Blockade der Kupferverfügbarkeit mit einem Wirkstoff ein lipoyliertes mitochondriales Protein, das diesem Weg zugeordnet ist, verringerte und die PDHA1–E2F1–PD‑L1‑Kette dämpfte, vor allem in Kombination mit PDHA1‑Herunterregulierung. Genomische und epigenetische Analysen deuteten darauf hin, dass hohes PDHA1 häufig mit DNA‑Veränderungen, niedriger Methylierung des PDHA1‑Gens und RNA‑Modifikationsmustern zusammenfällt, die mit aggressiveren Tumoren assoziiert sind. Wirkstoff‑Screening‑Datenbanken und zellbasierte Assays hoben mehrere Substanzen hervor — etwa das stoffwechselwirksame Medikament Phenformin und einen Inhibitor der E2F1‑Signalachse — auf die Sarkome mit aktivem PDHA1 möglicherweise besonders empfindlich reagieren, was rationale Kombinationen mit Immun‑Checkpoint‑Inhibitoren nahelegt.
Ein schlechtes Zeichen als Behandlungswegweiser nutzen
In Tiermodellen und Patientenbiopsien waren Tumoren mit hohem PDHA1 größer, stärker proliferativ, reicher an PD‑L1 und schlechter durch CD8⁺‑Killer‑T‑Zellen infiltriert. Gleichzeitig zeigten diese PDHA1‑starken Tumoren Merkmale — wie höhere Mutationslast und stärkere Checkpoint‑Signale — die oft mit besseren Ansprechen auf PD‑1‑ oder PD‑L1‑Blockade assoziiert sind. In einer kleinen klinischen Kohorte fortgeschrittener Sarkompatientinnen und ‑patienten, die eine solche Immuntherapie erhielten, profitierten diejenigen mit hohem PDHA1 eher. Für eine allgemeinverständliche Leserschaft lautet die Schlussfolgerung: PDHA1 wirkt sowohl als Gaspedal für Sarkomwachstum als auch als Schutzschild gegen Immunangriffe, aber genau dieses Verhalten könnte diese Tumoren verwundbarer machen, sobald die richtigen Bremsen angesetzt werden. Die Messung und das gezielte Ansprechen auf PDHA1 könnten daher helfen, Hochrisikopatienten zu identifizieren, den Einsatz von Immuntherapien zu lenken und neue metabolisch‑immunologische Wirkstoffkombinationen für hartnäckige Sarkome anzustoßen.
Zitation: Qin, H., Qi, T., Yao, N. et al. Cuproptosis-associated PDHA1 promotes sarcoma progression and immunotherapy responsiveness via the E2F1–PD-L1 axis: a multi-omics and clinical validation study. npj Precis. Onc. 10, 156 (2026). https://doi.org/10.1038/s41698-026-01298-0
Schlüsselwörter: Sarkom‑Immuntherapie, Krebsstoffwechsel, PDHA1, Blockade von Immun-Checkpoint, Tumormikroumgebung