Clear Sky Science · pt
PDHA1 associado à cuproptose promove progressão de sarcoma e responsividade à imunoterapia via o eixo E2F1–PD-L1: um estudo de validação multi-ômica e clínica
Por que esta pesquisa importa
Os sarcomas são cânceres raros, porém agressivos, que frequentemente resistem a tratamentos modernos baseados no sistema imunológico. Muitos pacientes com doença avançada esgotam opções padrão como cirurgia, quimioterapia e radiação, e ainda enfrentam baixa sobrevida. Este estudo explora um interruptor metabólico oculto dentro das células de sarcoma que aparentemente tanto alimenta o crescimento tumoral quanto molda a resposta do sistema imune. Entender esse interruptor pode abrir novas formas de prever quais pacientes se beneficiam da imunoterapia e de projetar combinações de tratamento mais inteligentes.
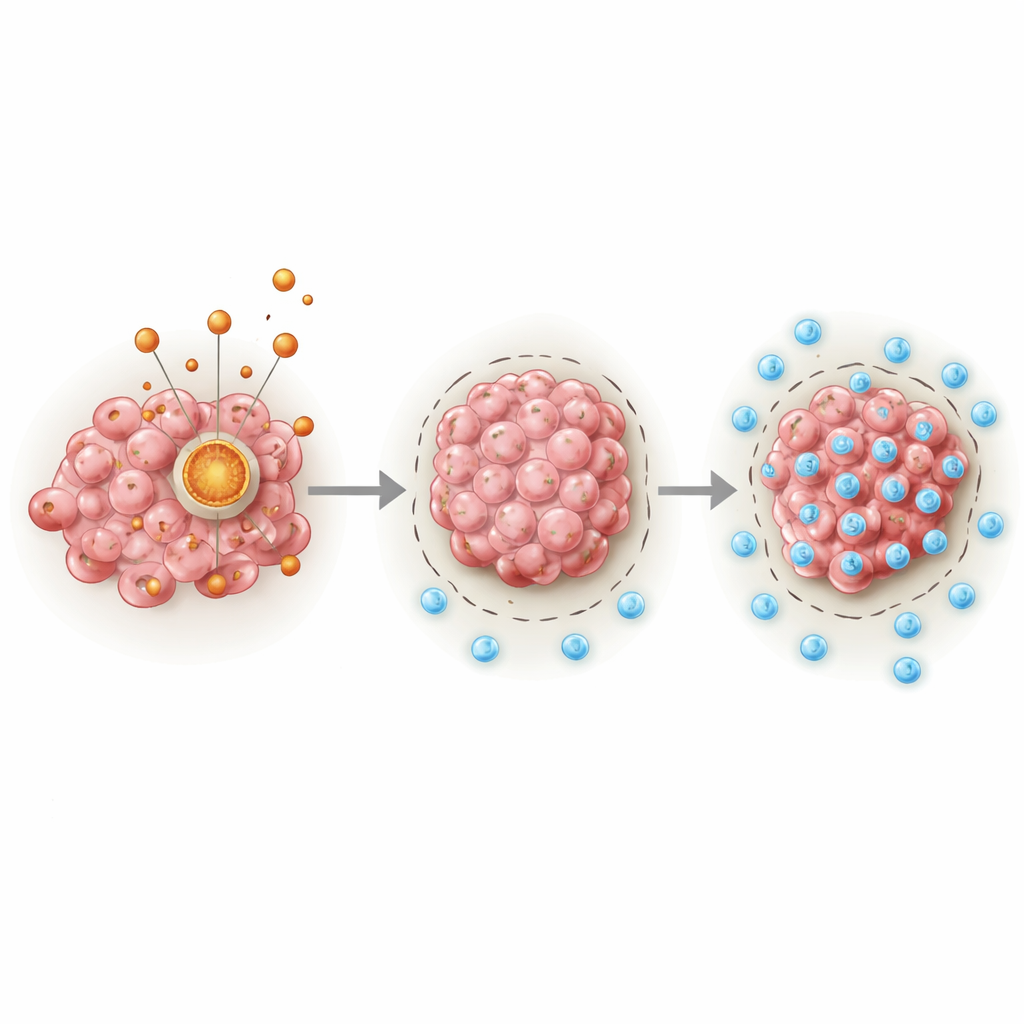
Um motor oculto dentro das células cancerosas
No centro da história está a PDHA1, uma proteína que funciona como uma chave entre a degradação da glicose e o principal ciclo de energia da célula nas mitocôndrias. Os autores analisaram grandes bancos de dados de câncer e amostras clínicas e descobriram que os sarcomas consistentemente apresentam níveis mais altos de PDHA1 do que tecidos normais. Pacientes cujos tumores tinham mais PDHA1 tendiam a apresentar sobrevida mais curta, independentemente de idade, sexo ou vários outros fatores clínicos. Ao combinar os níveis de PDHA1 com informações clínicas padrão, a equipe construiu uma ferramenta de predição que estimou a sobrevida em um, três e cinco anos com maior precisão do que as medidas tradicionais isoladas.
Como o metabolismo molda o entorno tumoral
Além de simplesmente promover o crescimento, a PDHA1 parece remodelar o entorno do tumor — a mistura de células imunes e de suporte que circunda o câncer. Usando métodos computacionais que inferem tipos celulares imunes a partir de RNA tumoral em massa, bem como sequenciamento de célula única de células imunes individuais, os autores mostraram que a PDHA1 está ativa não apenas em células tumorais, mas também em muitas populações imunes, especialmente células T e mieloides. Sarcomas com alta PDHA1 tendiam a apresentar sinais de um estado “excluído” imune: menos células T citotóxicas úteis no interior profundo do tumor, mais sinais de estroma fibroso e rígido e padrões sugerindo que células imunes eram mantidas nas margens em vez de serem permitidas atacar.
Uma cadeia molecular que bloqueia o ataque imune
Experimentos de laboratório revelaram como a PDHA1 conecta metabolismo ao escape imune. Quando os pesquisadores reduziram os níveis de PDHA1 em linhagens de sarcoma, as células dividiram-se menos, migraram menos, formaram menos colônias e passaram por mais morte celular programada. Ao mesmo tempo, os níveis de E2F1 — um regulador nuclear de genes envolvidos na divisão celular — e de PD-L1 — um “freio” imune na superfície das células tumorais — caíram. Ao examinar dados públicos de ligação ao DNA e realizar experimentos direcionados, a equipe mostrou que E2F1 liga-se diretamente à região de controle do gene PD-L1 e o ativa. Restaurar E2F1 em células deficientes em PDHA1 elevou PD-L1 novamente e resgatou parcialmente a sobrevivência celular, posicionando PDHA1 a montante de uma cadeia E2F1–PD-L1 que ajuda os tumores a se esconderem das células T.
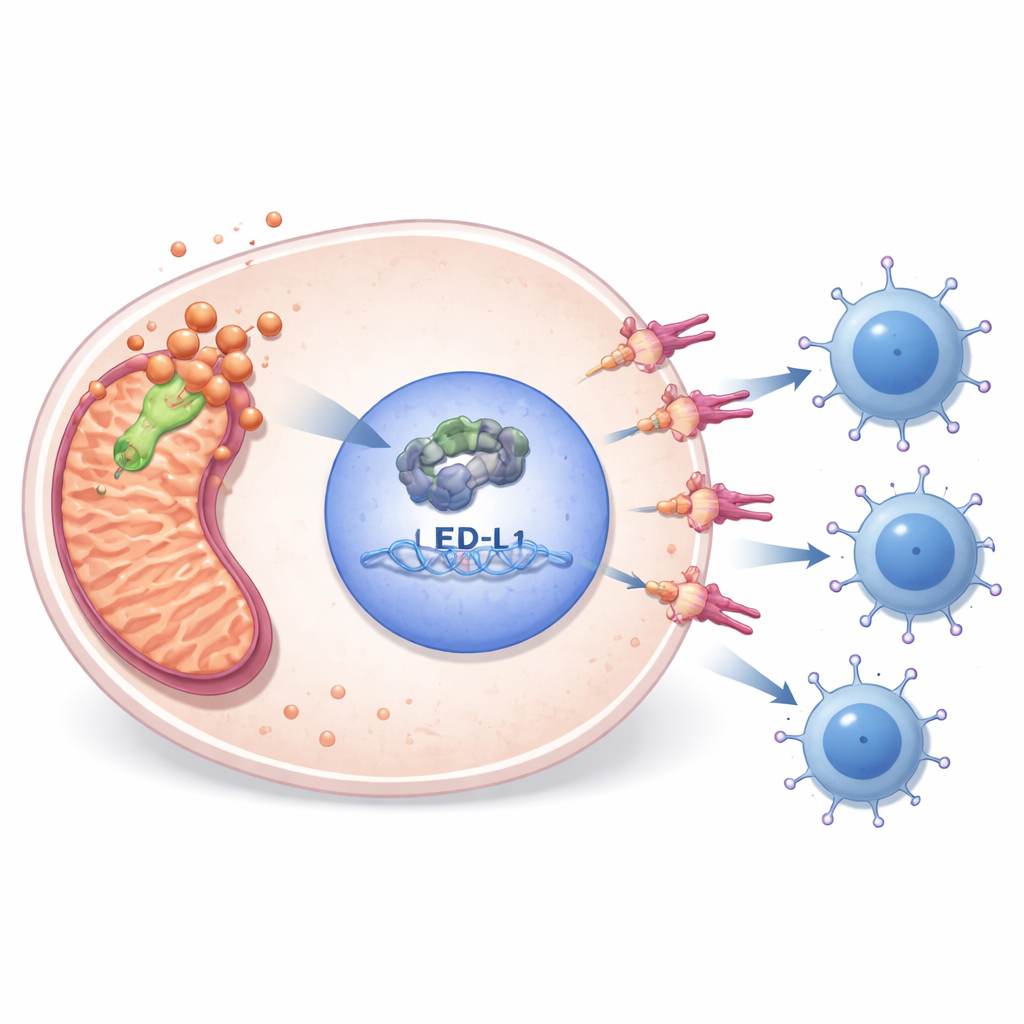
Morte celular ligada ao cobre e oportunidades farmacológicas
A PDHA1 também está ligada a uma forma recentemente descrita de morte celular desencadeada por cobre, chamada cuproptose. O estudo mostrou que bloquear a disponibilidade de cobre com um fármaco reduziu uma proteína mitocondrial lipoilada associada a essa via e atenuou a cadeia PDHA1–E2F1–PD-L1, especialmente quando combinado com silenciamento de PDHA1. Análises genômicas e epigenéticas sugeriram que alta PDHA1 frequentemente coincide com alterações no DNA, baixa metilação do gene PDHA1 e padrões de modificação de RNA associados a tumores mais agressivos. Bancos de dados de triagem de fármacos e ensaios celulares apontaram para vários medicamentos — como o agente metabólico phenformin e um inibidor da via E2F1 — aos quais sarcomas com PDHA1 ativa podem ser particularmente sensíveis, sugerindo combinações racionais com inibidores de ponto de verificação imune.
Transformando um mau sinal em guia terapêutico
Em modelos animais e biópsias de pacientes, tumores com alta PDHA1 eram maiores, mais proliferativos, mais ricos em PD-L1 e pobres em infiltração de células T CD8⁺ citotóxicas. Ainda assim, esses mesmos tumores de alta PDHA1 também exibiram características — como maior carga de mutações e sinais de checkpoint mais fortes — que estão frequentemente associadas a respostas melhores a drogas que bloqueiam PD-1 ou PD-L1. Em uma pequena coorte clínica de pacientes com sarcoma avançado recebendo essa imunoterapia, aqueles com alta PDHA1 foram mais propensos a beneficiar-se. Para um leitor leigo, a conclusão é que a PDHA1 atua tanto como acelerador do crescimento do sarcoma quanto como escudo contra o ataque imune, mas esse mesmo comportamento pode tornar esses tumores mais vulneráveis uma vez que os freios certos sejam aplicados. Medir e direcionar a PDHA1 poderia, portanto, ajudar a identificar pacientes de alto risco, orientar o uso de imunoterapia e inspirar novas combinações de fármacos metabólico-imunes para sarcomas difíceis de tratar.
Citação: Qin, H., Qi, T., Yao, N. et al. Cuproptosis-associated PDHA1 promotes sarcoma progression and immunotherapy responsiveness via the E2F1–PD-L1 axis: a multi-omics and clinical validation study. npj Precis. Onc. 10, 156 (2026). https://doi.org/10.1038/s41698-026-01298-0
Palavras-chave: imunoterapia de sarcoma, metabolismo do câncer, PDHA1, bloqueio de ponto de verificação imune, microambiente tumoral