Clear Sky Science · nl
Cuproptose-geassocieerde PDHA1 bevordert sarcoomprogressie en responsiviteit voor immunotherapie via de E2F1–PD-L1-as: een multi-omics en klinische validatiestudie
Waarom dit onderzoek ertoe doet
Sarcomen zijn zeldzame maar agressieve kankers die vaak resistent zijn tegen moderne immuungerichte behandelingen. Veel patiënten met gevorderde ziektes raken door de standaardopties zoals chirurgie, chemotherapie en bestraling heen en hebben desondanks nog steeds een slechte overleving. Deze studie onderzoekt een verborgen metabool schakelaar in sarcoomcellen die zowel tumorgroei lijkt te voeden als de immuunreactie vormt. Inzicht in deze schakelaar kan nieuwe manieren openen om te voorspellen welke patiënten baat hebben bij immunotherapie en om slimmer samengestelde behandelingen te ontwerpen.
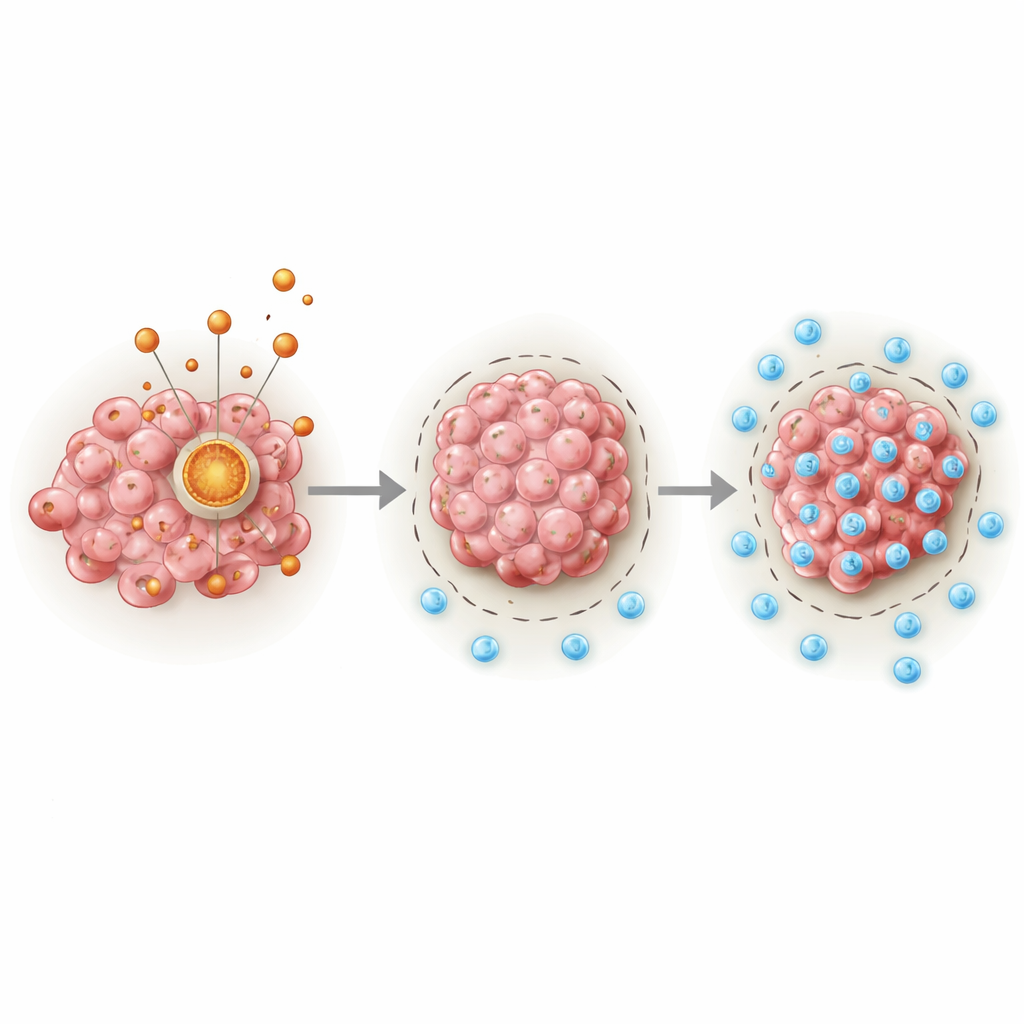
Een verborgen motor in kankercellen
Midden in het verhaal staat PDHA1, een eiwit dat fungeert als een belangrijke poort tussen de afbraak van suikers en de belangrijkste energieketen van de cel in de mitochondriën. De auteurs analyseerden grote kanker-databases en klinische monsters en vonden dat sarcomen consequent hogere PDHA1-niveaus dragen dan normaal weefsel. Patiënten van wie de tumoren meer PDHA1 hadden, leefden over het algemeen korter, ongeacht leeftijd, geslacht of meerdere andere klinische factoren. Door PDHA1-niveaus te combineren met standaard klinische informatie bouwde het team een voorspellend instrument dat de één-, drie- en vijfjaarsoverleving beter inschatte dan traditionele maatstaven alleen.
Hoe metabolisme de tumoromgeving vormt
Buiten het puur aansturen van groei, leek PDHA1 de buurt van de tumor te hervormen — de mix van immuun- en ondersteunende cellen rond de kanker. Met behulp van computationele methoden die immuunceltypes afleiden uit bulk tumorrna, evenals enkelcelsequencing van individuele immuuncellen, toonden de auteurs aan dat PDHA1 actief is niet alleen in tumorcellen maar ook in veel immuunpopulaties, vooral T-cellen en myeloïde cellen. Sarcomen met hoge PDHA1 toonden vaak kenmerken van een “immuun-uitgesloten” toestand: minder behulpzame killer-T-cellen diep in de tumor, meer signalen van stug, vezelig stroma, en patronen die suggereren dat immuuncellen aan de rand werden gehouden in plaats van toegelaten om aan te vallen.
Een moleculaire keten die immuunaanval blokkeert
Laboratoriumexperimenten onthulden hoe PDHA1 metabolisme koppelt aan immuunontsnapping. Toen de onderzoekers PDHA1-niveaus verlaagden in sarcoomcelijnen, deelden de cellen minder, bewogen minder, vormden minder kolonies en ondergingen meer geprogrammeerde celdood. Tegelijkertijd daalden niveaus van E2F1 — een kernregulator van genen die betrokken zijn bij celdeling — en PD-L1 — een immuunremmende factor op het oppervlak van tumorcellen. Door publieke DNA-bindingsdata te onderzoeken en gerichte experimenten uit te voeren, toonde het team aan dat E2F1 direct bindt aan het controlegebied van het PD-L1-gen en het activeert. Het terugbrengen van E2F1 in PDHA1-deficiënte cellen herstelde PD-L1 deels en redde gedeeltelijk de celdeling, wat PDHA1 plaatst stroomopwaarts van een E2F1–PD-L1-keten die tumoren helpt zich te verbergen voor T-cellen.
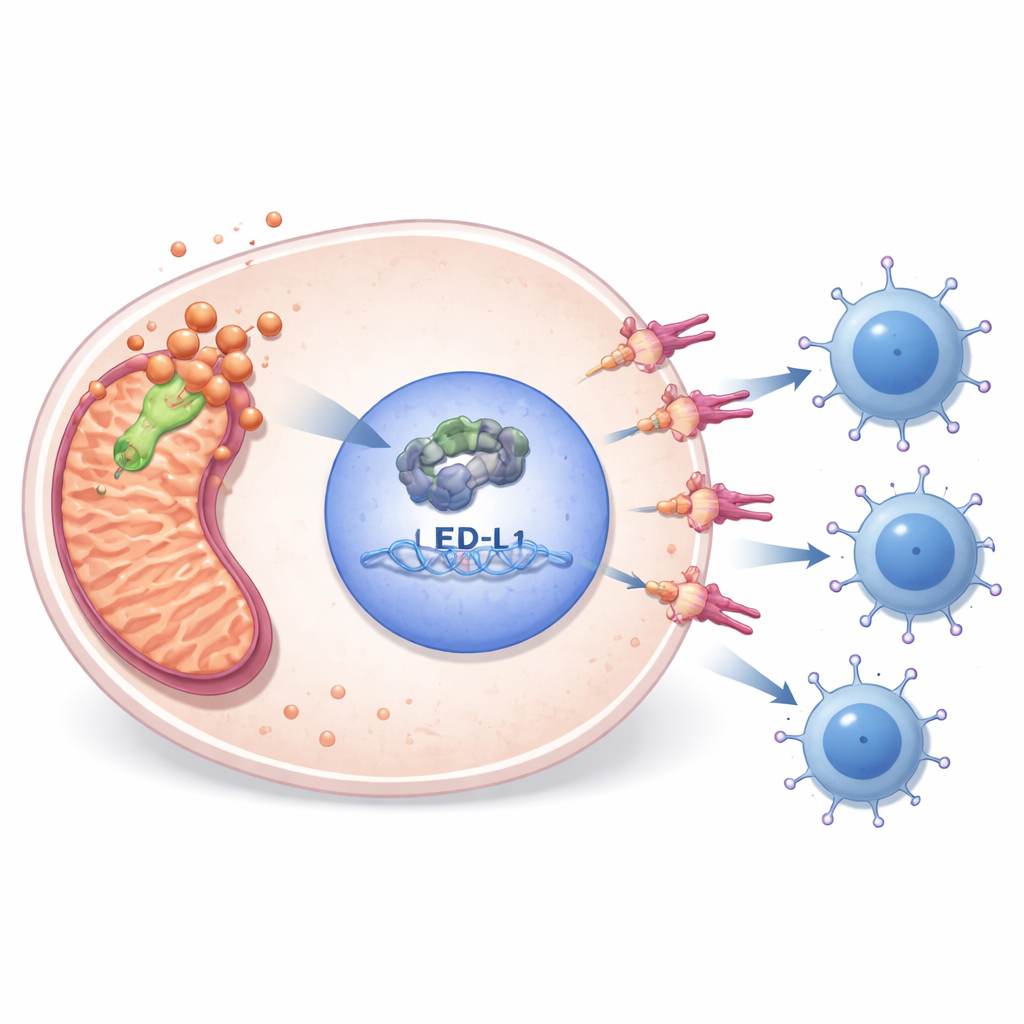
Kopergebonden celdood en medicatiekansen
PDHA1 is ook verbonden met een recent beschreven vorm van celdood die door koper wordt getriggerd, cuproptose genoemd. De studie toonde aan dat het blokkeren van koperbeschikbaarheid met een geneesmiddel een gelipoyeerd mitochondriaal eiwit dat aan deze route gekoppeld is verminderde en de PDHA1–E2F1–PD-L1-keten dempte, vooral wanneer gecombineerd met PDHA1-knockdown. Genomische en epigenetische analyses suggereerden dat hoge PDHA1 vaak samenvalt met DNA-veranderingen, lage methylering van het PDHA1-gen en RNA-modificatiepatronen die geassocieerd zijn met agressievere tumoren. Medicijnscreening-databases en celgebaseerde assays wezen op meerdere middelen — zoals de metabole stof phenformin en een remmer van de E2F1-route — waar sarcomen met actieve PDHA1 mogelijk bijzonder gevoelig voor zijn, wat wijst op rationele combinaties met immuuncheckpointremmers.
Een slecht teken omzetten in een behandelingsrichtlijn
In diermodellen en patiëntbiopten waren tumoren met hoge PDHA1 groter, meer proliferatief, rijker aan PD-L1 en armer aan infiltratie door CD8⁺ killer T-cellen. Toch toonden dezezelfde hoge-PDHA1-tumoren ook kenmerken — zoals een hogere mutatielast en sterkere checkpointsignalen — die vaak samenhangen met betere responsen op middelen die PD-1 of PD-L1 blokkeren. In een kleine klinische cohort van gevorderde sarcoompatiënten die dergelijke immunotherapie kregen, hadden degenen met hoge PDHA1 meer kans op voordeel. Voor een niet-specialistische lezer is de conclusie dat PDHA1 zowel als gaspedaal voor sarcoomgroei fungeert als schild tegen immuunaanval, maar dat dit gedrag deze tumoren juist kwetsbaarder kan maken zodra de juiste remmen worden toegepast. Het meten en richten op PDHA1 kan daarom helpen hoog-risico patiënten te identificeren, het gebruik van immunotherapie te sturen en nieuwe metabool-immuun combinaties te inspireren voor hardnekkige sarcomen.
Bronvermelding: Qin, H., Qi, T., Yao, N. et al. Cuproptosis-associated PDHA1 promotes sarcoma progression and immunotherapy responsiveness via the E2F1–PD-L1 axis: a multi-omics and clinical validation study. npj Precis. Onc. 10, 156 (2026). https://doi.org/10.1038/s41698-026-01298-0
Trefwoorden: sarcoom immunotherapie, kankermetabolisme, PDHA1, remming van immuuncheckpoints, tumormicro-omgeving