Clear Sky Science · zh
基于磺胺嘧啶-水杨醛席夫碱的合成、表征与抗癌活性
为何这项研究重要
癌症药物常常在杀伤肿瘤的同时损伤健康细胞,导致难以承受的副作用。本研究探讨了两种实验室合成的密切相关分子,旨在尽可能在保留正常细胞的前提下促使癌细胞进入可控的自我毁灭程序。通过追踪这些分子在癌细胞中的行为,研究人员寻找可为未来更安全、更精确治疗提供线索的早期证据。
设计新型小分子
团队聚焦于一类称为席夫碱的化合物,这是一类结构灵活、已知具有多种生物活性的小分子。他们以常见的抗生素构件磺胺嘧啶为起点,通过连接略有差异的环状结构合成了两种新变体,命名为SB1和SB2。包括红外光谱和核磁共振在内的严格化学测试证实了两种分子具有预期的构型和高纯度,这是任何生物测试可信赖之前的必备条件。
在实验室测试癌细胞
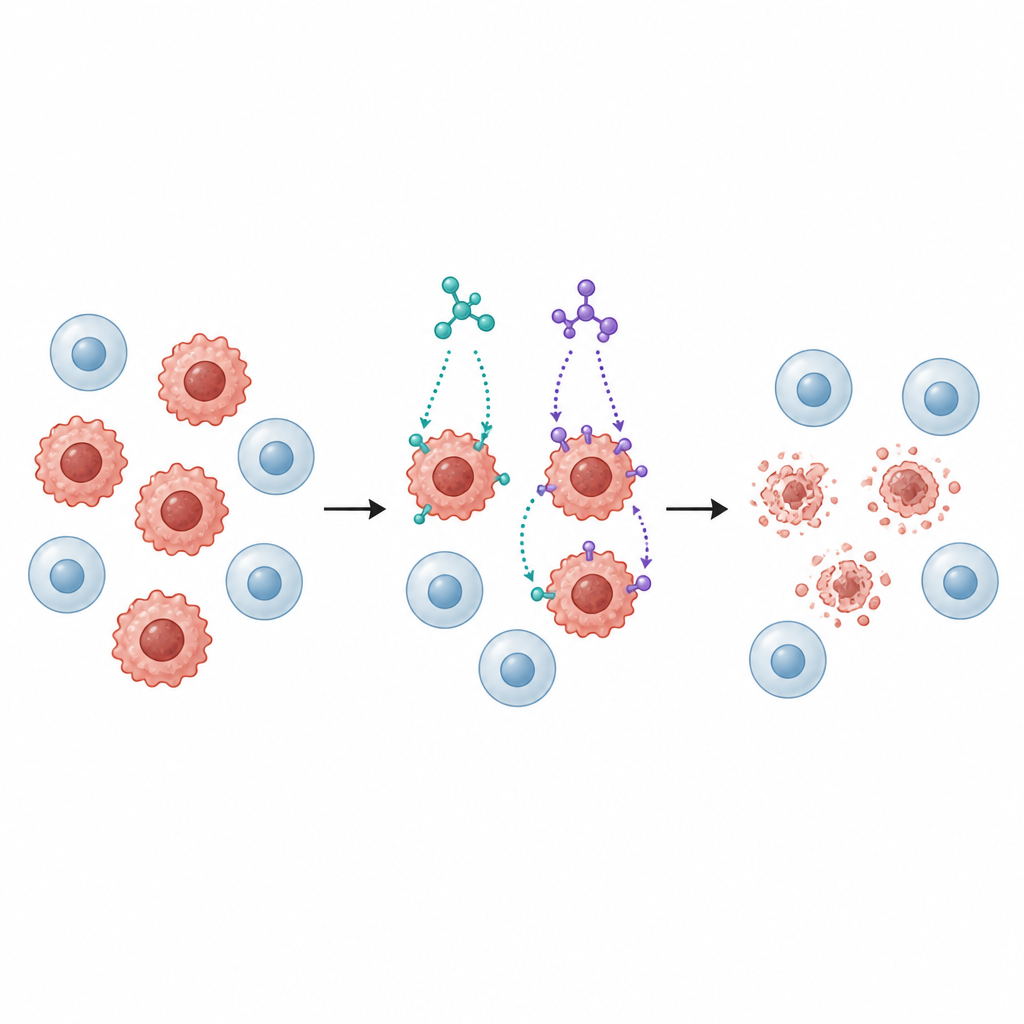
随后,研究人员将多种人类癌细胞系暴露于SB1和SB2,包括乳腺、结肠、肺、肝和膀胱癌细胞,并以一株正常肺细胞系作比较。两种分子均呈剂量依赖性地抑制癌细胞生长,但SB2通常在低剂量下更有效,尤其针对乳腺(MCF‑7)和结肠(HCT116)细胞。值得注意的是,正常肺细胞对这些化合物的敏感性低于肿瘤细胞,表明存在一定程度的选择性,这对任何潜在抗癌药物来说都是重要品质。
触发有序的细胞死亡程序
仅仅抑制生长并不足以清除癌细胞。因此团队进一步检测SB1和SB2是否促使细胞进入凋亡——一种有序的自我毁灭程序,细胞在其中分解而不会向周围组织释放有害内容物。利用基于染料的流式细胞术测试,结果显示在乳腺和结肠癌细胞系中,两种分子显著增加了处于早期和晚期凋亡阶段的细胞比例。与该通路相关的关键蛋白水平也以协调的方式发生变化:促凋亡信号上升,保护性蛋白下降,称为半胱天冬酶的酶被激活,所有这些模式均一致指向通过线粒体介导的凋亡途径。
对DNA与关键酶的应激作用
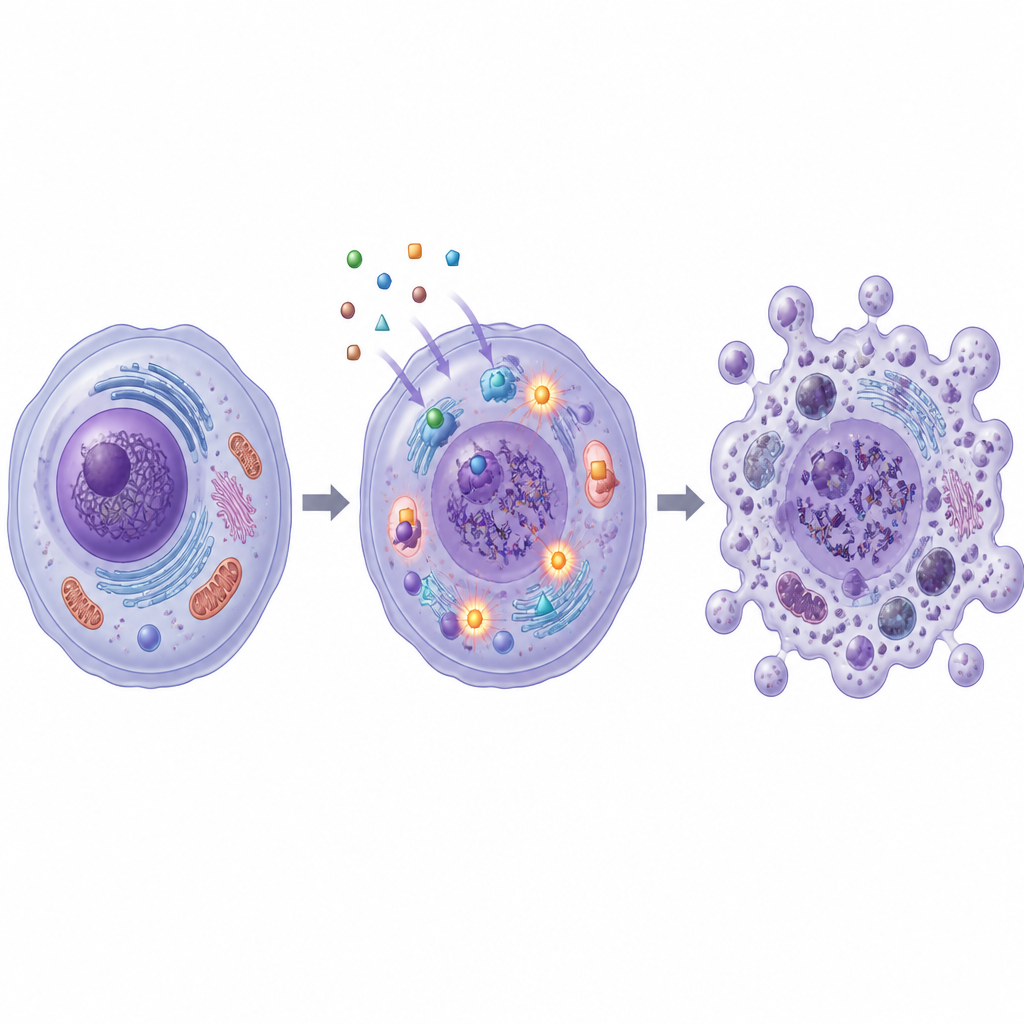
研究还探查了这些分子如何从内部损伤癌细胞。SB1和SB2提高了活性氧(ROS)的生成,活性氧是不稳定分子,能损害细胞结构和DNA。基于显色的DNA片段检测显示,受处理的癌细胞携带更多断裂的遗传物质,SB2尤其显著。与此同时,两种化合物都降低了称为拓扑异构酶I和II的酶的活性,这些酶在DNA复制和修复过程中负责管理DNA的扭转与解扭。计算机模拟支持了这些实验发现,表明SB1和SB2能够紧密嵌入拓扑异构酶II和另一种与癌症相关的蛋白——碳酸酐酶XII的结合口袋。
单个原子的作用
尽管SB1与SB2仅在SB2上多出一个溴原子,这一微小的化学修饰却产生了明显影响。在大多数测试中,SB2在抑制癌细胞增殖、提高氧化应激、促成DNA断裂和阻断拓扑异构酶活性方面均表现更强。额外的溴原子很可能改变了分子与细胞膜及蛋白靶标的相互作用,提升其进入细胞的能力并增强与关键位点的结合力。这说明分子设计中的细微变化可以显著重塑生物学行为。
对此的未来意义
综上所述,这些基于磺胺嘧啶的席夫碱,尤其是SB2,能够在体外将癌细胞推向可控的自我毁灭途径,同时对正常细胞的伤害较小。它们似乎通过一系列机制发挥作用:增加氧化应激、造成DNA损伤并阻断癌细胞赖以生长与分裂的酶。尽管这些化合物尚未达到可作为药物使用的阶段,但它们为化学家提供了有前途的先导分子,可在后续工作中改进以获得更佳的稳定性和安全性,从而发展成未来的抗癌剂。
引用: Nasr, E., Moustafa, A.H., El-Sayed, A.S.A. et al. Synthesis, characterization, and anticancer potency of sulfadiazine salicylaldehyde-based Schiff bases. Sci Rep 16, 15047 (2026). https://doi.org/10.1038/s41598-026-51752-z
关键词: 席夫碱, 抗癌化合物, 细胞凋亡, 活性氧, 拓扑异构酶抑制