Clear Sky Science · sv
Syntes, karakterisering och anticancerpotential hos sulfadiazin-salicylaldehyd-baserade Schiff-baser
Varför denna forskning är viktig
Cancerläkemedel skadar ofta friska celler tillsammans med tumörer, vilket ger svåra biverkningar. Denna studie undersöker två nära besläktade laboratorieframställda molekyler som syftar till att få cancerceller att genomgå en kontrollerad form av självdestruktion samtidigt som normala celler skonas så mycket som möjligt. Genom att följa hur dessa molekyler beter sig i cancerceller söker forskarna tidiga ledtrådar som kan peka mot säkrare och mer preciserade behandlingar i framtiden.
Utformning av nya småmolekyler
Gruppen fokuserade på en familj föreningar som kallas Schiff-baser, en flexibel klass småmolekyler som redan är kända för ett brett spektrum biologiska effekter. Med utgångspunkt i en vanlig antibiotikabygsten, sulfadiazin, skapade de två nya varianter kallade SB1 och SB2 genom att fästa något olika ringstrukturer. Noggranna kemiska tester, inklusive infraröda mätningar och kärnmagnetisk resonans, bekräftade att båda molekylerna hade de avsedda strukturerna och hög renhet, vilket är avgörande innan några biologiska tester kan ha tillförlitligt värde.
Testning av cancerceller i laboratoriet
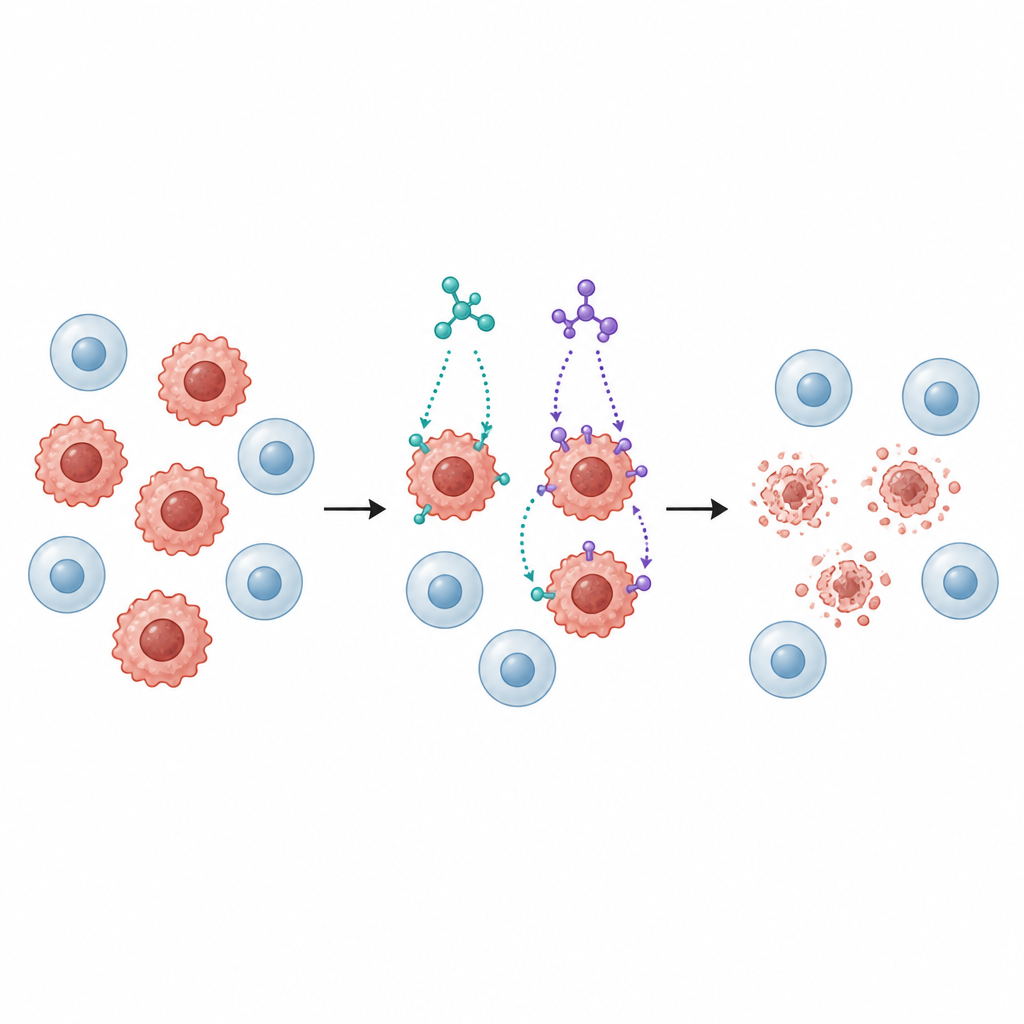
Därefter exponerade forskarna flera mänskliga cancercellinjer för SB1 och SB2, inklusive bröst-, kolorektal-, lung-, lever- och blåscancerceller, tillsammans med en normal lungcellinje för jämförelse. Båda molekylerna bromsade cancercellernas tillväxt på ett dosberoende sätt, men SB2 fungerade vanligen vid lägre doser än SB1, särskilt mot bröstceller (MCF 7) och kolonceller (HCT116). Viktigt är att normala lungceller var mindre känsliga än tumörceller, vilket tyder på viss selektivitet — en viktig egenskap för ett potentiellt cancerläkemedel.
Utlösning av ett ordnat celldödsprogram
Att stoppa tillväxt är bara användbart om cancerceller också avlägsnas. Forskarna undersökte därför om SB1 och SB2 driver celler mot apoptos, ett ordnat självdestruktionprogram där celler sönderfaller utan att läcka skadliga innehåll till omgivande vävnad. Med hjälp av ett färgbaserat flödescytometritest visade de att båda molekylerna kraftigt ökade andelen celler i tidiga och sena stadier av apoptos i bröst- och koloncellinjerna. Nivåerna av nyckelproteiner kopplade till denna väg förändrades samordnat: pro-dödsignaler ökade, skyddande proteiner minskade och enzymer kallade kaspaser aktiverades, alla mönster som stämmer med en mitokondriell apoptosisväg.
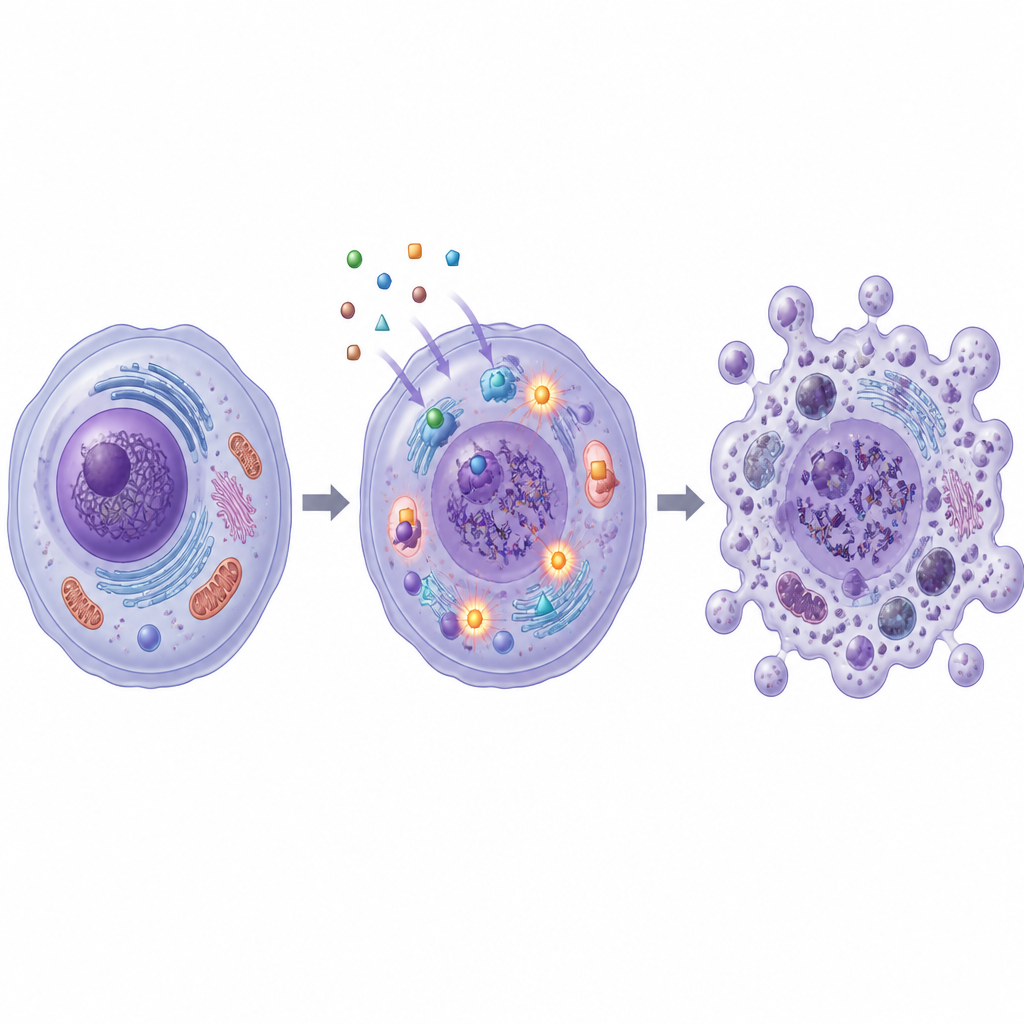
Stress på DNA och viktiga enzymer
Studien undersökte också hur dessa molekyler skadar cancerceller inifrån. SB1 och SB2 ökade produktionen av reaktiva syrearter, instabila molekyler som kan skada cellstrukturer och DNA. Ett färgbaserat test för DNA-fragment visade att behandlade cancerceller bar på betydligt mer brutet genetiskt material, särskilt vid behandling med SB2. Samtidigt minskade båda föreningarna aktiviteten hos enzymerna topoisomeras I och II, som hanterar DNA:s tvinnande och upptvinning vid kopiering och reparation. Datorsimuleringar stödde dessa laboratoriefynd och indikerade att SB1 och SB2 kan sitta tätt i bindningsfickorna hos topoisomeras II och ett annat cancerrelaterat protein, karbanhydrashydras XII.
Betydelsen av en enda atom
Även om SB1 och SB2 skiljer sig endast genom förekomsten av en enda bromatom på SB2, hade denna lilla kemiska justering tydlig påverkan. I de flesta tester visade SB2 starkare förmåga att stoppa cancercellstillväxt, öka oxidativ stress, fragmentera DNA och blockera topoisomerasaktivitet. Den tillsatta bromen ändrar sannolikt hur molekylen interagerar med cellmembran och proteinmål, vilket förbättrar dess inträde i celler och dess bindning till kritiska platser inuti dem. Detta illustrerar hur subtila förändringar i molekylär design kan kraftigt omforma biologiskt beteende.
Vad detta innebär framöver
Sammantaget tyder resultaten på att dessa sulfadiazinbaserade Schiff-baser, och särskilt SB2, kan driva cancerceller mot ett kontrollerat självdestruktionsförlopp samtidigt som de är mindre skadliga för normala celler i odlingsskålar. De verkar verka genom en kombination av ökad oxidativ stress, DNA-skada och blockering av enzymer som cancerceller är beroende av för att växa och dela sig. Även om dessa föreningar inte är redo att användas som läkemedel, utgör de lovande startpunkter, så kallade lead-molekyler, för kemister att vidareutveckla till framtida anticancerläkemedel med bättre stabilitet och säkerhetsprofil.
Citering: Nasr, E., Moustafa, A.H., El-Sayed, A.S.A. et al. Synthesis, characterization, and anticancer potency of sulfadiazine salicylaldehyde-based Schiff bases. Sci Rep 16, 15047 (2026). https://doi.org/10.1038/s41598-026-51752-z
Nyckelord: Schiff-baser, anticancerföreningar, apoptos, reaktiva syrearter, topoisomerasinhibering