Clear Sky Science · nl
Synthese, karakterisering en antikankereffect van sulfadiazine-salicylaldehyde gebaseerde Schiff-basen
Waarom dit onderzoek ertoe doet
Kankergeneesmiddelen beschadigen vaak gezonde cellen naast tumoren, wat leidt tot ingrijpende bijwerkingen. Deze studie onderzoekt twee nauw verwante in het laboratorium gemaakte moleculen die gericht kankercellen in een gecontroleerde vorm van zelfvernietiging willen sturen, terwijl normale cellen zoveel mogelijk worden gespaard. Door te volgen hoe deze moleculen zich gedragen in kankercellen, zoeken de onderzoekers naar vroege aanwijzingen die in de toekomst kunnen leiden tot veiligere, preciezere behandelingen.
Ontwerp van nieuwe kleine moleculen
Het team richtte zich op een familie van verbindingen die bekendstaat als Schiff-basen, een flexibele klasse van kleine moleculen met uiteenlopende biologische effecten. Met behulp van een veelgebruikt antibiotisch bouwblok, sulfadiazine, creëerden ze twee nieuwe varianten, SB1 en SB2, door licht verschillende ringstructuren aan te koppelen. Zorgvuldige chemische tests, waaronder infraroodmetingen en kernspinresonantie, bevestigden dat beide moleculen de beoogde structuren en een hoge zuiverheid hadden — essentieel voordat biologische tests betrouwbaar zijn.
Testen van kankercellen in het laboratorium
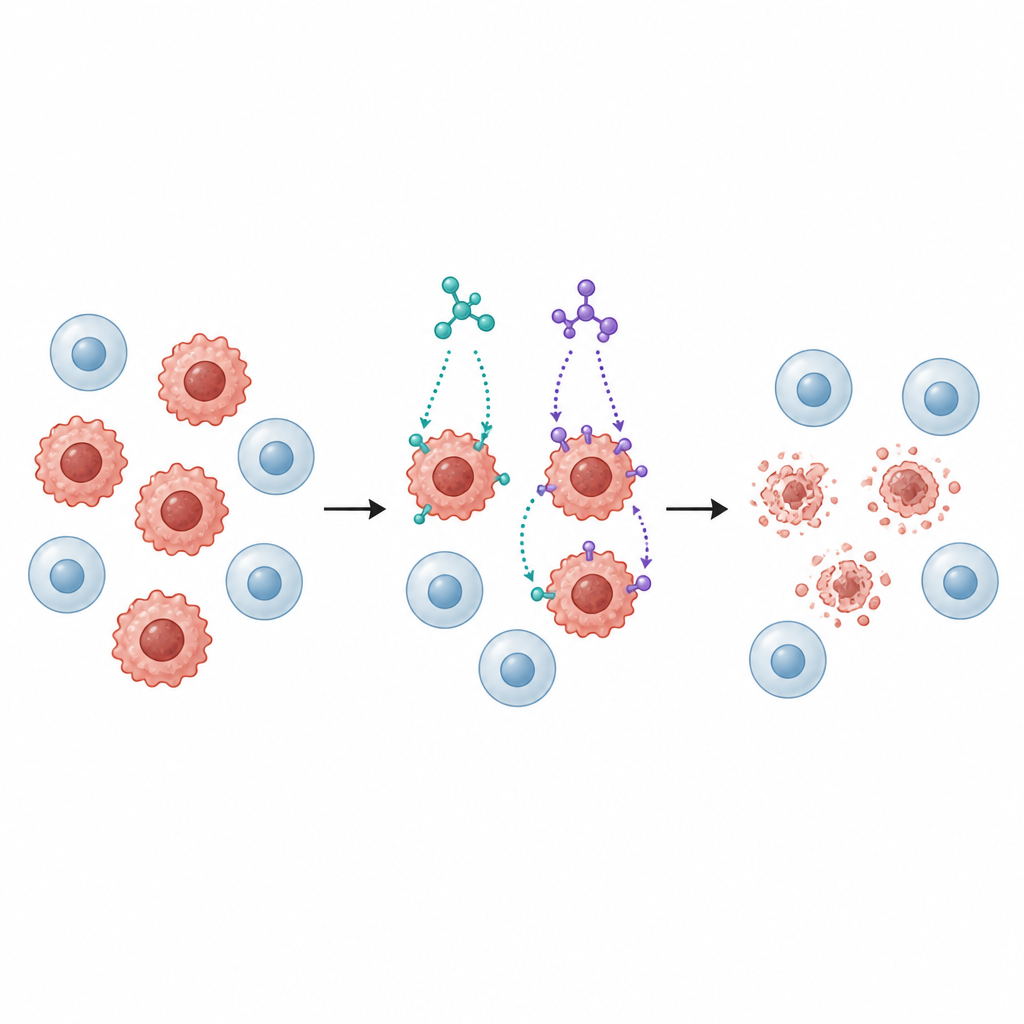
Vervolgens brachten de onderzoekers meerdere humane kankercellijnen in contact met SB1 en SB2, waaronder borstkanker-, darm-, long-, lever- en blaaskankercellen, naast een normale longcellijn ter vergelijking. Beide moleculen vertraagden de groei van kankercellen op een dosisafhankelijke manier, maar SB2 werkte doorgaans bij lagere doses dan SB1, met name tegen borstkanker (MCF-7) en darmkanker (HCT116) cellen. Belangrijk is dat normale longcellen minder gevoelig waren dan tumorcellen, wat wijst op enige mate van selectiviteit — een cruciale eigenschap voor mogelijke kankergeneesmiddelen.
Het opwekken van een ordelijke celdood
Groeistop is alleen nuttig als kankercellen ook worden verwijderd. Daarom onderzochten de onderzoekers of SB1 en SB2 cellen in apoptose duwen, een ordelijk zelfvernietigingsprogramma waarbij cellen afbreken zonder schadelijke inhoud in omliggend weefsel te lekken. Met een kleurstofgebaseerde flowcytometrie-test lieten ze zien dat beide moleculen het aandeel cellen in vroege en late stadia van apoptose in borsten darmkankerlijnen sterk verhoogden. De niveaus van sleutelproteïnen die met dit pad verbonden zijn, verschoof op een gecoördineerde manier: pro-death signalen stegen, beschermende eiwitten daalden en enzymen genaamd caspases werden geactiveerd — allemaal patronen die passen bij een mitochondriale route naar apoptose.
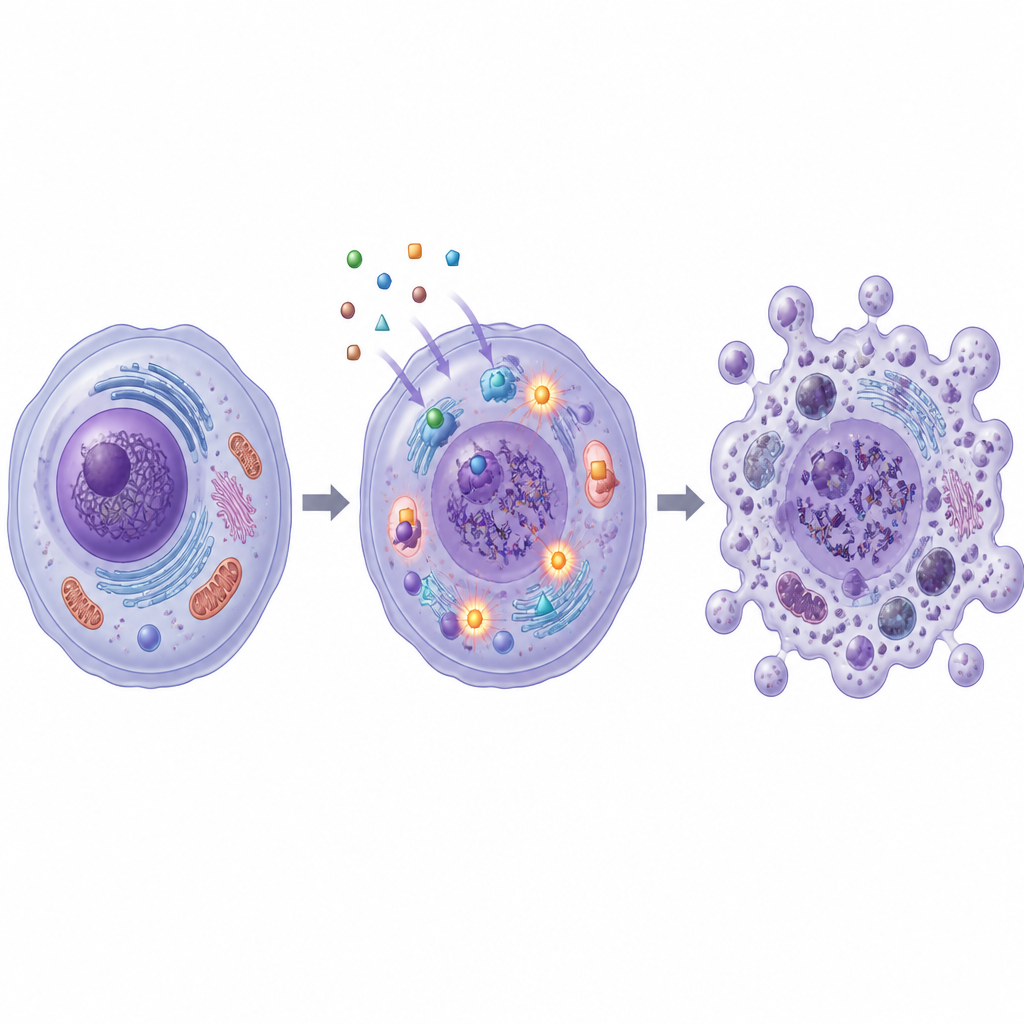
DNA- en enzymstress
De studie onderzocht ook hoe deze moleculen kankercellen van binnenuit beschadigen. SB1 en SB2 verhoogden de productie van reactieve zuurstofsoorten, instabiele moleculen die cellulaire structuren en DNA kunnen beschadigen. Een kleurgebaseerde test van DNA-fragmenten toonde aan dat behandelde kankercellen veel meer gebroken genetisch materiaal droegen, vooral bij SB2. Tegelijkertijd verminderden beide verbindingen de activiteit van enzymen die topoisomerases I en II worden genoemd, verantwoordelijk voor het draaien en ontwarren van DNA tijdens replicatie en herstel. Computersimulaties ondersteunden deze laboratoriumbevindingen en wezen uit dat SB1 en SB2 goed in de bindingspockets van topoisomerase II en een ander kankerg gerelateerd eiwit, carbonic anhydrase XII, kunnen passen.
De rol van één atoom
Hoewel SB1 en SB2 slechts verschillen door de aanwezigheid van één broomatoom op SB2, had deze kleine chemische wijziging een duidelijk effect. In de meeste tests toonde SB2 een sterkere capaciteit om kankercelgroei te remmen, oxidatieve stress te verhogen, DNA te fragmenteren en topoisomerase-activiteit te blokkeren. Het toegevoegde broom verandert waarschijnlijk hoe het molecuul interacteert met celmembranen en proteïnedoelen, waardoor de opname in cellen en de binding aan cruciale plekken verbetert. Dit illustreert hoe subtiele wijzigingen in moleculair ontwerp het biologische gedrag sterk kunnen hervormen.
Wat dit betekent voor de toekomst
Samengevat suggereren de resultaten dat deze sulfadiazine-gebaseerde Schiff-basen, en in het bijzonder SB2, kankercellen kunnen duwen richting een gecontroleerd zelfvernietigingspad terwijl ze in kweek minder schadelijk lijken voor normale cellen. Ze lijken te werken via een combinatie van verhoogde oxidatieve stress, DNA-schade en blokkade van enzymen waarop kankercellen vertrouwen om te groeien en te delen. Hoewel deze verbindingen nog niet klaar zijn om als geneesmiddelen te worden gebruikt, vormen ze veelbelovende uitgangspunten — leadmoleculen — voor chemici om verder te verfijnen tot toekomstige antikankeragentia met betere stabiliteit en veiligheidsprofielen.
Bronvermelding: Nasr, E., Moustafa, A.H., El-Sayed, A.S.A. et al. Synthesis, characterization, and anticancer potency of sulfadiazine salicylaldehyde-based Schiff bases. Sci Rep 16, 15047 (2026). https://doi.org/10.1038/s41598-026-51752-z
Trefwoorden: Schiff-basen, antikankerverbindingen, apoptose, reactieve zuurstofsoorten, topoisomeraseremming