Clear Sky Science · he
סינתזה, מאפיין ועצמת אנטי‑סרטן של בסיסי שיף מבוססי סולפדיאזין‑סליצילאלדהיד
למה המחקר הזה חשוב
תרופות נגד סרטן לעתים מזיקות גם לתאים בריאים לצד הגידולים, וגורמות לתופעות לוואי קשות. מחקר זה חוקר שתי מולקולות מעבדתיות קרובות שמטרתן לדחוף תאי סרטן לתהליך מבוקר של השמדת עצמי, תוך שמירה מירבית על תאים נורמליים. במעקב אחר האופן שבו מולקולות אלה מתנהגות בתאי סרטן, החוקרים מחפשים רמזים מוקדמים שיכולים להנחות טיפולים בטוחים ומדויקים יותר בעתיד.
עיצוב מולקולות קטנות חדשות
הצוות התמקד במשפחה של תרכובות הידועות כבסיסי שיף, קבוצת מולקולות קטנות וגמישה שכבר ידועה בשל מגוון השפעות ביולוגיות. באמצעות בלוק בנייה אנטיביוטי נפוץ, סולפדיאזין, ייצרו הם שתי וריאנטים חדשים הקרויים SB1 ו‑SB2 על ידי חיבור מבני טבעת שונים במעט. בדיקות כימיות קפדניות, כולל מדידות אינפרה‑אדום והדמיית תהודה מגנטית גרעינית, אישרו ששתי המולקולות בעלות הצורות המקוות וטוהר גבוה — דבר החיוני לפני שניתן לסמוך על תוצאות הבדיקות הביולוגיות.
בדיקת תאי סרטן במעבדה
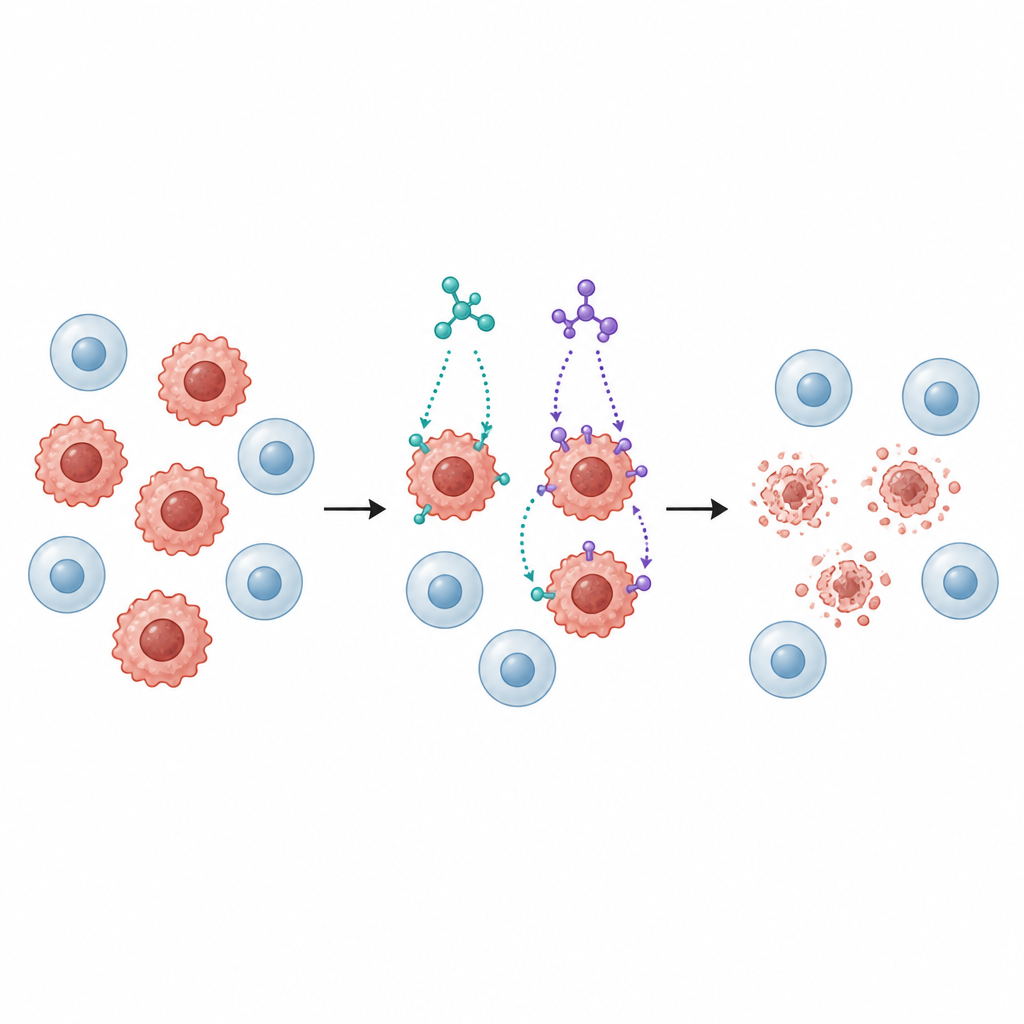
בהמשך, החוקרים חשפו מספר שורות תאי סרטן אנושיים ל‑SB1 ו‑SB2, כולל תאי סרטן שד, מעי גס, ריאה, כבד ושלפוחית השתן, לצד שורת תאי ריאה נורמלית להשוואה. שתי המולקולות האטו את גדילת תאי הסרטן במידה תלויה במינון, אך בדרך כלל SB2 עברה להשפעה במינונים נמוכים יותר מ‑SB1, במיוחד נגד תאי סרטן שד (MCF‑7) ומעי גס (HCT116). חשוב מכך, תאי ריאה נורמליים היו פחות רגישים מתאי הגידול, מה שמרמז על מידה מסוימת של בררנות — תכונה חשובה עבור כל חוץ פוטנציאלי.
הפעלת תוכנית מוות מסודרת של התא
עצירת גדילה מועילה רק אם תאי הסרטן גם הוסרו. לכן הצוות בחן האם SB1 ו‑SB2 דוחפים תאים לאפופטוזה, תהליך השמדת עצמי מאורגן שבו התאים מתפרקים מבלי לשפוך תContents מזיקים לרקמות הסמוכות. בעזרת בדיקת צביעת זרימה, הראו החוקרים ששתי המולקולות הגדילו במידה ניכרת את החלק של התאים שעוברים שלבי אפופטוזה מוקדמים ומאוחרים בקווי סרטן של שד ומעי. רמות חלבונים מפתח הקשורים למסלול זה השתנו באופן מתואם: אותות פרו‑מוות עלו, חלבונים מגן ירדו, ואנזימים שנקראים קספאזות הופעלו — דפוסים התואמים למסלול מיטוכונדריאלי לאפופטוזה.
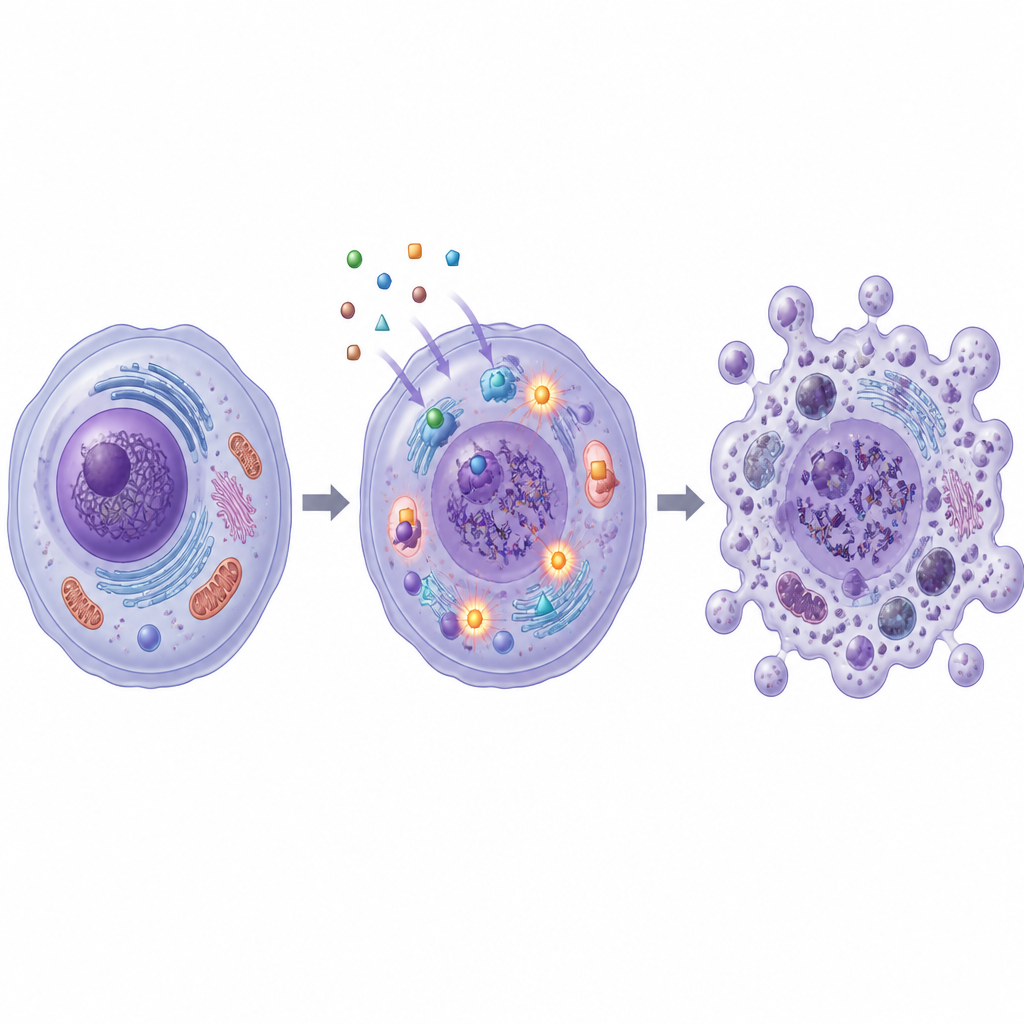
מתיחת דנ"א ואנזימים חיוניים
המחקר גם בדק כיצד מולקולות אלה פוגעות בתאי הסרטן מבפנים. SB1 ו‑SB2 הגבירו את ייצור מיני חמצון פעילים, מולקולות בלתי יציבות היכולות לפגוע במבנים תאיים ובדנ"א. בדיקה מבוססת צבע של שברי דנ"א הראתה שתאי סרטן מטופלים נשאו הרבה יותר חומר גנטי שבור, במיוחד עם SB2. בו זמנית, שתי התרכובות הפחיתו את פעילותם של אנזימים הנקראים טופואיזומראזות I ו‑II, שמנהלות את פיתול־ההפיכה של הדנ"א במהלך שכפול ותיקון. הדמיות ממוחשבות תמכו בממצאים האלה במעבדה, והראו ש‑SB1 ו‑SB2 יכולות להתמקם בהדוק בכיסי הקשירה של טופואיזומראז II וחלבון קשור לסרטן, אנזים החומצה הפחמתית XII (carbonic anhydrase XII).
תפקידו של אטום בודד
למרות ש‑SB1 ו‑SB2 נבדלות רק בנוכחותו של אטום ברום אחד ב‑SB2, השינוי הכימי הקטן הזה השפיע באופן ברור. ברוב הבדיקות SB2 הראתה יכולת חזקה יותר לעצור גדילת תאי סרטן, להעלות לחץ חמצוני, לפרק דנ"א ולחסום פעילות טופואיזומראז. הברום המתווסף משנה כנראה את האינטראקציה של המולקולה עם ממברנות התאים ויעדי החלבון, ומשפר את כניסת המולקולה לתאים ואת אחיזתה באתרים קריטיים בתוכם. זה ממחיש כיצד שינויים עדינים בעיצוב מולקולרי יכולים לשנות באופן משמעותי התנהגות ביולוגית.
מה משמעות הממצאים להמשך
בסיכום, התוצאות מציעות שבסיסי שיף מבוססי סולפדיאזין אלה, ובמיוחד SB2, יכולים לדחוף תאי סרטן לנתיב השמדה עצמית מבוקר בעוד שהם פחות מזיקים לתאים נורמליים במנות תרבית. נראה שהם פועלים באמצעות שילוב של עלייה בלחץ החמצוני, נזק לדנ"א וחסימה של אנזימים שתאי סרטן נסמכים עליהם לצמיחה וחלוקה. בעוד שתרכובות אלה אינן מוכנות לשימוש כתרופות, הן מספקות נקודות התחלה מבטיחות, מולקולות מובילות, שאותן כימאים יכולים למקד ולשפר לעבר סוכנים אנטי‑סרטן עתידיים עם יציבות ובטיחות טובות יותר.
ציטוט: Nasr, E., Moustafa, A.H., El-Sayed, A.S.A. et al. Synthesis, characterization, and anticancer potency of sulfadiazine salicylaldehyde-based Schiff bases. Sci Rep 16, 15047 (2026). https://doi.org/10.1038/s41598-026-51752-z
מילות מפתח: בסיסי שיף, תרכובות אנטי‑סרטן, אפופטוזה, מיני חמצון פעילים, עיכוב טופואיזומראז