Clear Sky Science · es
Síntesis, caracterización y potencia anticancerígena de bases de Schiff basadas en sulfadiacina y salicilaldehído
Por qué importa esta investigación
Los fármacos contra el cáncer a menudo dañan células sanas junto con los tumores, causando efectos secundarios difíciles. Este estudio explora dos moléculas estrechamente relacionadas sintetizadas en el laboratorio que intentan inducir en las células cancerosas una forma controlada de autodestrucción, preservando en la mayor medida posible las células normales. Al seguir cómo se comportan estas moléculas en células cancerosas, los investigadores buscan pistas tempranas que puedan orientar tratamientos más seguros y precisos en el futuro.
Diseño de nuevas moléculas pequeñas
El equipo se centró en una familia de compuestos conocidos como bases de Schiff, una clase flexible de moléculas pequeñas ya reconocida por una amplia gama de efectos biológicos. Usando un bloque de construcción antibiótico común, la sulfadiacina, crearon dos variantes nuevas llamadas SB1 y SB2 al unir estructuras de anillo ligeramente diferentes. Pruebas químicas cuidadosas, incluidas mediciones por infrarrojo y resonancia magnética nuclear, confirmaron que ambas moléculas tenían las formas previstas y alta pureza, lo cual es esencial antes de confiar en cualquier ensayo biológico.
Pruebas en células cancerosas en el laboratorio
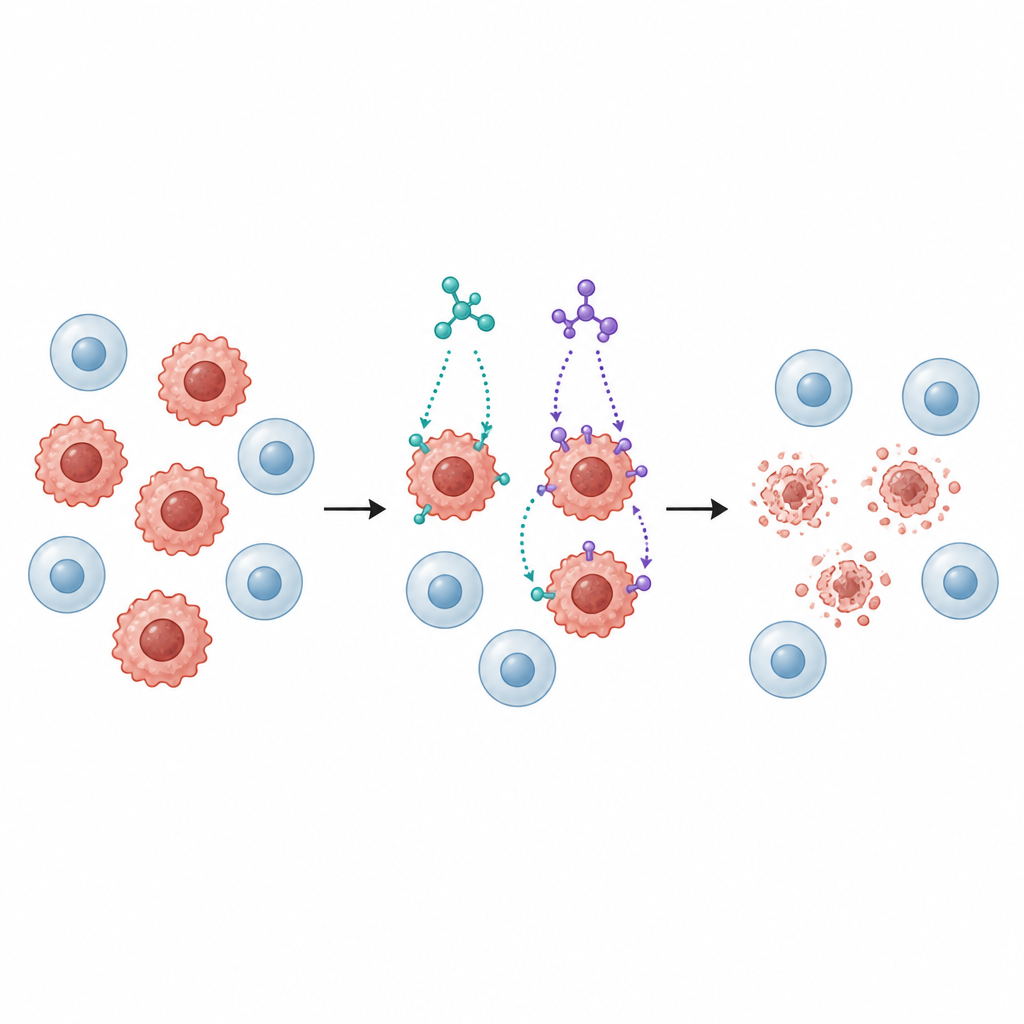
A continuación, los investigadores expusieron varias líneas celulares humanas de cáncer a SB1 y SB2, incluyendo cáncer de mama, colon, pulmón, hígado y vejiga, junto con una línea celular pulmonar normal para comparación. Ambas moléculas ralentizaron el crecimiento de las células cancerosas de forma dependiente de la dosis, pero SB2 generalmente actuó a dosis más bajas que SB1, especialmente frente a las células de cáncer de mama (MCF-7) y colon (HCT116). Es importante que las células pulmonares normales fueron menos sensibles que las tumorales, lo que sugiere cierto grado de selectividad, una cualidad importante para cualquier posible fármaco anticancerígeno.
Activación de un programa ordenado de muerte celular
Detener el crecimiento solo es útil si las células cancerosas también se eliminan. Por ello, el equipo examinó si SB1 y SB2 inducen apoptosis, un programa ordenado de autodestrucción en el que las células se descomponen sin derramar contenidos dañinos al tejido circundante. Mediante un ensayo por citometría de flujo con tinción, demostraron que ambas moléculas aumentaron considerablemente la fracción de células en etapas tempranas y tardías de apoptosis en las líneas de cáncer de mama y colon. Los niveles de proteínas clave vinculadas a esta vía cambiaron de manera coordinada: aumentaron las señales pro‑muerte, disminuyeron las proteínas protectoras y se activaron enzimas llamadas caspasas, patrones compatibles con una vía mitocondrial hacia la apoptosis.
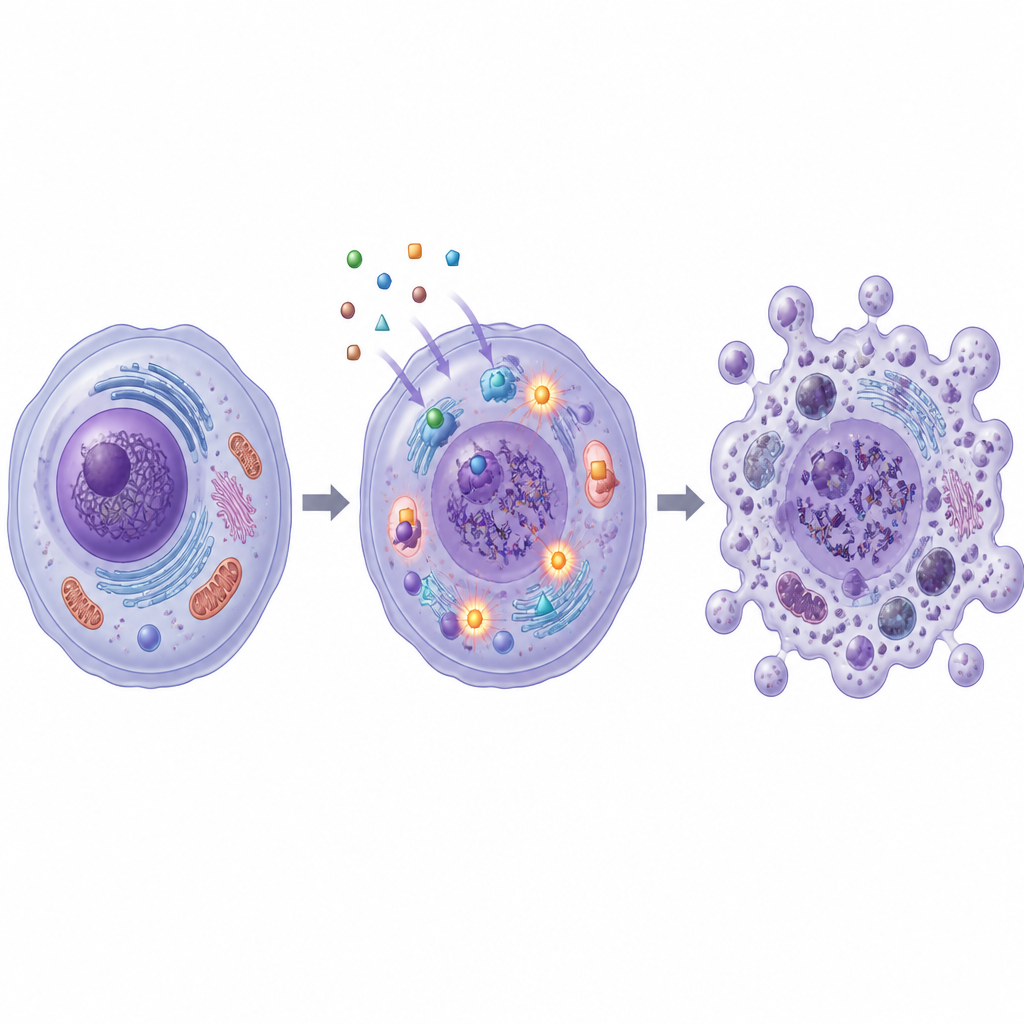
Estrés en el ADN y en enzimas vitales
El estudio también investigó cómo estas moléculas dañan las células cancerosas desde el interior. SB1 y SB2 aumentaron la producción de especies reactivas de oxígeno, moléculas inestables que pueden dañar estructuras celulares y el ADN. Una prueba colorimétrica de fragmentos de ADN mostró que las células cancerosas tratadas presentaban mucho más material genético fragmentado, especialmente con SB2. Al mismo tiempo, ambos compuestos redujeron la actividad de enzimas llamadas topoisomerasas I y II, que gestionan el torsión y destorsión del ADN durante su copia y reparación. Simulaciones por ordenador apoyaron estos hallazgos de laboratorio, indicando que SB1 y SB2 pueden encajar de forma ajustada en los sitios de unión de la topoisomerasa II y de otra proteína relacionada con el cáncer, la anhidrasa carbónica XII.
El papel de un solo átomo
Aunque SB1 y SB2 difieren únicamente por la presencia de un solo átomo de bromo en SB2, este pequeño ajuste químico tuvo un impacto claro. En la mayoría de las pruebas, SB2 mostró una mayor capacidad para detener el crecimiento de células cancerosas, aumentar el estrés oxidativo, fragmentar el ADN y bloquear la actividad de la topoisomerasa. El bromo añadido probablemente altera cómo la molécula interactúa con las membranas celulares y los blancos proteicos, mejorando su entrada en las células y su afinidad por sitios críticos en su interior. Esto ilustra cómo cambios sutiles en el diseño molecular pueden remodelar notablemente el comportamiento biológico.
Qué significa esto de cara al futuro
En conjunto, los resultados sugieren que estas bases de Schiff basadas en sulfadiacina, y en particular SB2, pueden empujar a las células cancerosas hacia una vía controlada de autodestrucción al tiempo que son menos dañinas para las células normales en cultivos. Parecen actuar mediante una combinación de aumento del estrés oxidativo, daño en el ADN y bloqueo de enzimas que las células cancerosas necesitan para crecer y dividirse. Aunque estos compuestos no están listos para usarse como fármacos, proporcionan puntos de partida prometedores, o moléculas guía, para que los químicos las refinen en futuros agentes anticancerígenos con mejores perfiles de estabilidad y seguridad.
Cita: Nasr, E., Moustafa, A.H., El-Sayed, A.S.A. et al. Synthesis, characterization, and anticancer potency of sulfadiazine salicylaldehyde-based Schiff bases. Sci Rep 16, 15047 (2026). https://doi.org/10.1038/s41598-026-51752-z
Palabras clave: Bases de Schiff, compuestos anticancerígenos, apoptosis, especies reactivas de oxígeno, inhibición de topoisomerasa