Clear Sky Science · pt
Síntese, caracterização e potência anticâncer de bases de Schiff à base de sulfadiazina e salicilaldeído
Por que esta pesquisa importa
Medicamentos contra o câncer frequentemente danificam células saudáveis junto com os tumores, causando efeitos colaterais difíceis. Este estudo explora duas moléculas sintéticas intimamente relacionadas que têm como objetivo levar células cancerosas a uma forma controlada de autodestruição, poupando ao máximo as células normais. Ao acompanhar como essas moléculas se comportam em células tumorais, os pesquisadores procuram pistas iniciais que possam orientar tratamentos futuros mais seguros e precisos.
Desenhando novas pequenas moléculas
A equipe focalizou-se numa família de compostos conhecidas como bases de Schiff, uma classe versátil de pequenas moléculas já reconhecida por uma ampla gama de efeitos biológicos. Usando um bloco de construção comum de um antibiótico, a sulfadiazina, eles criaram duas variantes chamadas SB1 e SB2 ao ligar estruturas de anel ligeiramente diferentes. Testes químicos cuidadosos, incluindo medidas por infravermelho e ressonância magnética nuclear, confirmaram que ambas as moléculas apresentavam as formas pretendidas e alta pureza, o que é essencial antes que qualquer ensaio biológico possa ser considerado confiável.
Testando células cancerosas no laboratório
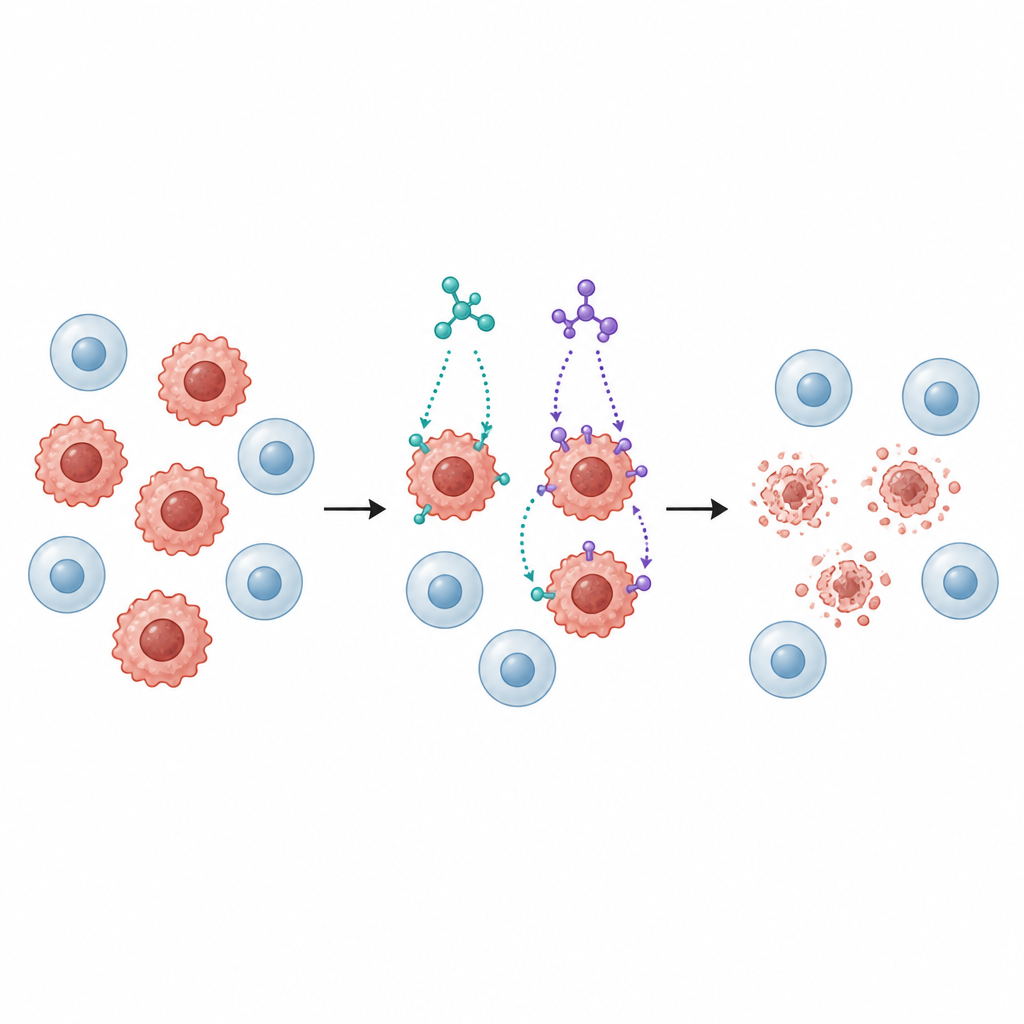
Em seguida, os pesquisadores expuseram várias linhagens humanas de células cancerosas à SB1 e SB2, incluindo câncer de mama, cólon, pulmão, fígado e bexiga, além de uma linhagem de células pulmonares normais para comparação. Ambas as moléculas retardaram o crescimento das células tumorais de forma dependente da dose, mas a SB2 geralmente atuou em doses mais baixas que a SB1, especialmente contra células de mama (MCF‑7) e cólon (HCT116). Importante, as células pulmonares normais mostraram menor sensibilidade do que as tumorais, sugerindo algum grau de seletividade, uma qualidade relevante para qualquer potencial medicamento anticâncer.
Desencadeando um programa organizado de morte celular
Interromper o crescimento é útil apenas se as células cancerosas também forem eliminadas. A equipe, portanto, examinou se SB1 e SB2 induzem apoptose, um programa ordenado de autodestruição no qual as células se desmontam sem liberar conteúdos nocivos ao tecido circundante. Usando um ensaio por citometria de fluxo baseado em corantes, demonstraram que ambas as moléculas aumentaram consideravelmente a fração de células em estágios iniciais e tardios de apoptose nas linhagens de mama e cólon. Os níveis de proteínas-chave associadas a essa via mudaram de forma coordenada: sinais pró‑morte aumentaram, proteínas protetoras diminuíram e enzimas chamadas caspases foram ativadas, todos padrões consistentes com uma via mitocondrial de apoptose.
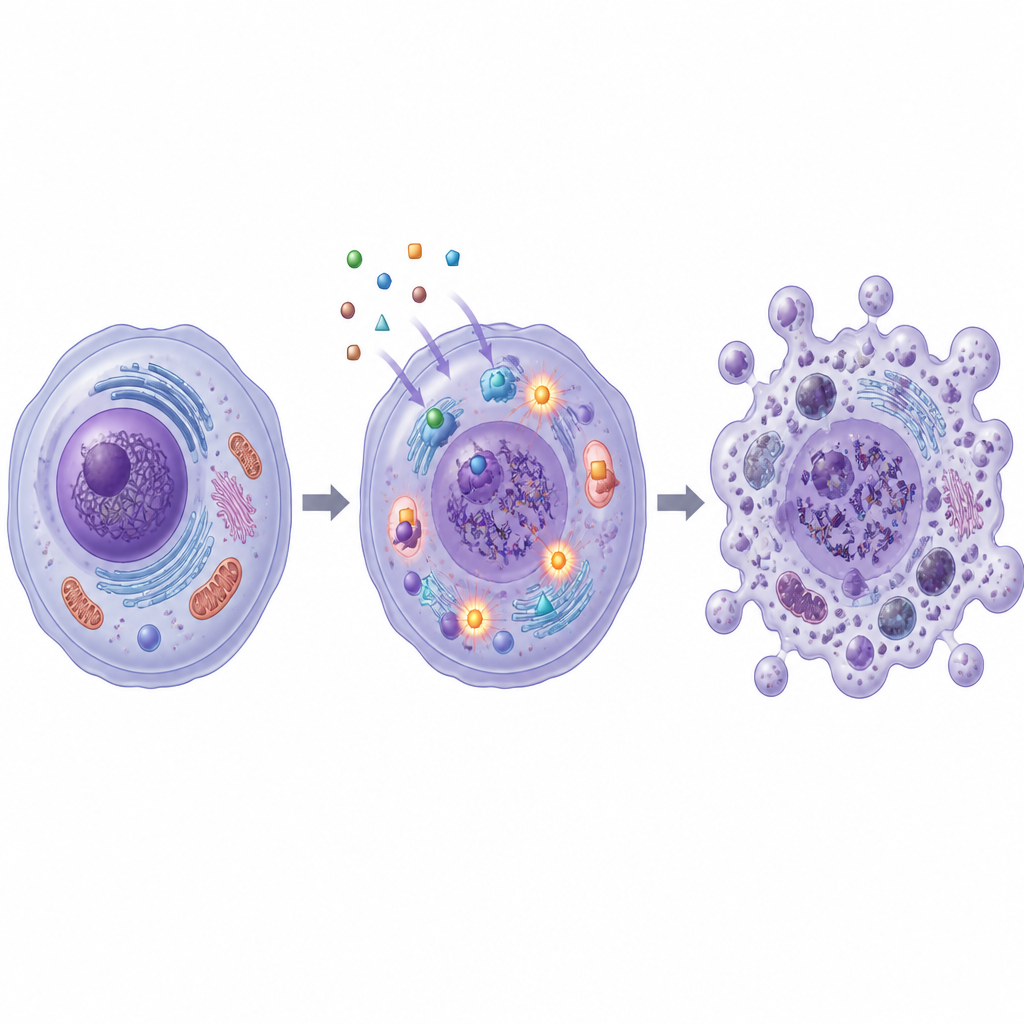
Estressando o DNA e enzimas vitais
O estudo também investigou como essas moléculas danificam as células cancerosas internamente. SB1 e SB2 aumentaram a produção de espécies reativas de oxigênio, moléculas instáveis que podem prejudicar estruturas celulares e o DNA. Um ensaio colorimétrico de fragmentos de DNA mostrou que as células tratadas apresentavam muito mais material genético fragmentado, especialmente com SB2. Ao mesmo tempo, ambos os compostos reduziram a atividade das enzimas topoisomerase I e II, que gerenciam o enrolamento e desenrolamento do DNA durante a replicação e reparo. Simulações computacionais sustentaram esses achados de laboratório, indicando que SB1 e SB2 podem encaixar-se de forma favorável nos bolsões de ligação da topoisomerase II e de outra proteína relacionada ao câncer, a anidrase carbônica XII.
O papel de um único átomo
Embora SB1 e SB2 difiram apenas pela presença de um único átomo de bromo na SB2, esse pequeno ajuste químico teve impacto claro. Na maioria dos testes, SB2 mostrou maior capacidade de deter o crescimento celular, elevar o estresse oxidativo, fragmentar o DNA e bloquear a atividade da topoisomerase. O bromo adicionado provavelmente altera como a molécula interage com membranas celulares e alvos proteicos, melhorando sua entrada nas células e sua afinidade por sítios críticos no interior delas. Isso ilustra como mudanças sutis no projeto molecular podem remodelar marcadamente o comportamento biológico.
O que isso significa para o futuro
Em conjunto, os resultados sugerem que essas bases de Schiff derivadas da sulfadiazina, e especialmente a SB2, podem direcionar células cancerosas para um caminho controlado de autodestruição enquanto são menos nocivas às células normais em placas de cultura. Elas parecem atuar por uma combinação de aumento do estresse oxidativo, dano ao DNA e bloqueio de enzimas das quais as células tumorais dependem para crescer e se dividir. Embora esses compostos ainda não estejam prontos para uso como medicamentos, oferecem pontos de partida promissores, ou moléculas líderes, para químicos refinarem em futuros agentes anticâncer com perfis de estabilidade e segurança melhores.
Citação: Nasr, E., Moustafa, A.H., El-Sayed, A.S.A. et al. Synthesis, characterization, and anticancer potency of sulfadiazine salicylaldehyde-based Schiff bases. Sci Rep 16, 15047 (2026). https://doi.org/10.1038/s41598-026-51752-z
Palavras-chave: bases de Schiff, compostos anticâncer, apoptose, espécies reativas de oxigênio, inibição da topoisomerase