Clear Sky Science · ja
サルファジアジン-サリチルアルデヒド系シッフ塩基の合成、特性評価、および抗がん活性
この研究が重要な理由
がん治療薬は腫瘍とともに正常細胞も損なうことが多く、重大な副作用を引き起こします。本研究は、正常細胞をできるだけ温存しつつがん細胞を制御された自己破壊へ導くことを目的とした、密接に関連する2つの合成小分子を調べます。これらの分子ががん細胞内でどのように振る舞うかを追跡することで、将来のより安全で精密な治療法を導く早期の手がかりを探しています。
新しい小分子の設計
研究チームは、広範な生物学的効果で知られる柔軟な小分子群であるシッフ塩基に着目しました。一般的な抗生物質の構成要素であるサルファジアジンを用いて、わずかに異なる環構造を結合することでSB1とSB2という2つの新変異体を合成しました。赤外分光法や核磁気共鳴などの精密な化学解析により、両分子が意図した構造と高い純度を有していることが確認され、これは生物学的試験の信頼性に不可欠です。
試験管内でのがん細胞試験
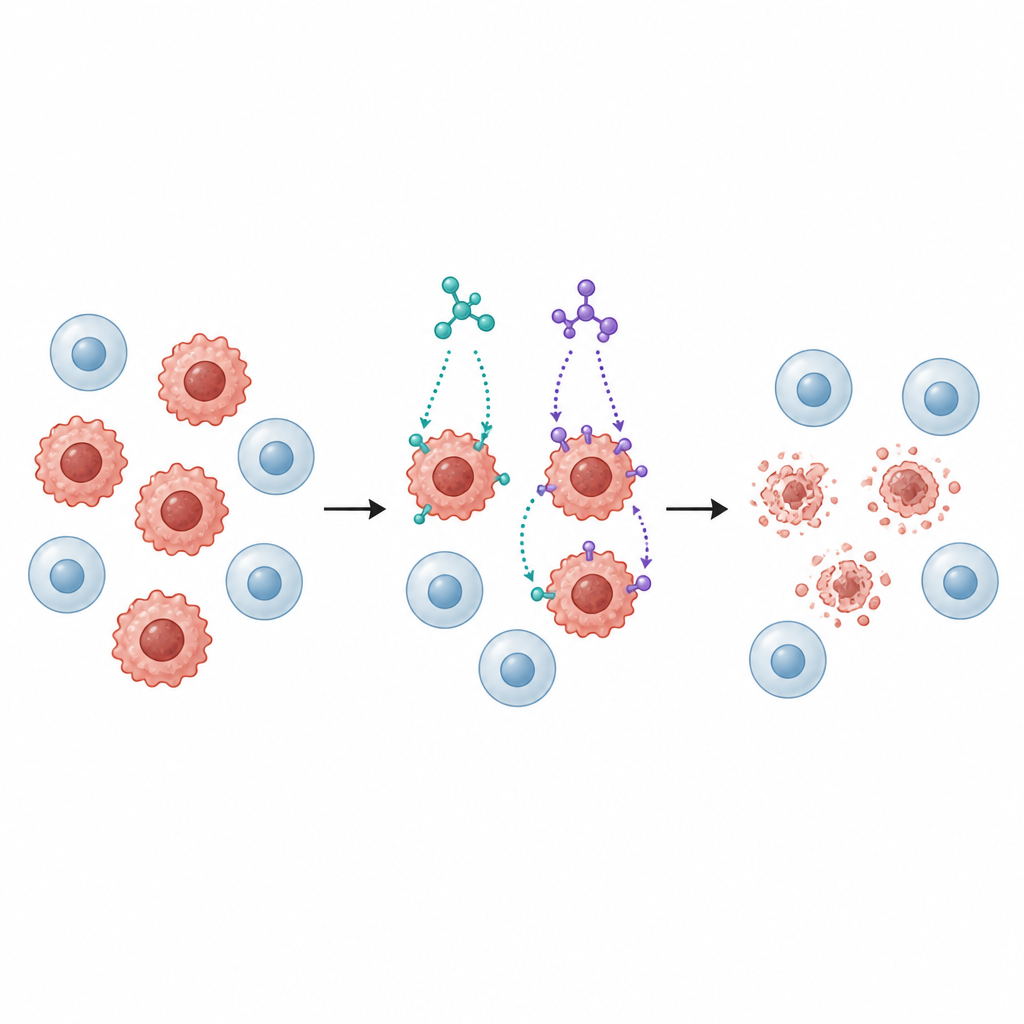
次に、研究者らは乳がん、結腸がん、肺がん、肝臓がん、膀胱がんのヒトがん細胞株と、比較用の正常な肺細胞株にSB1およびSB2を曝露しました。両化合物は用量依存的にがん細胞の増殖を抑制しましたが、特に乳がん(MCF-7)および結腸がん(HCT116)に対してはSB2の方が一般に低用量で効果を示しました。重要な点として、正常肺細胞は腫瘍細胞より感受性が低く、これは潜在的ながん薬にとって重要な選択性を示唆します。
整然とした細胞死プログラムの誘導
増殖抑制はがん細胞の除去を伴わない限り不十分です。そこでチームはSB1とSB2が細胞をアポトーシス、すなわち周囲組織に有害な内容物を漏らさずに細胞が自滅する整然としたプログラムへと誘導するかを調べました。蛍光色素を用いたフローサイトメトリー試験により、両化合物はいずれも乳がん・結腸がん細胞で初期から後期までのアポトーシス段階に入る細胞の割合を大幅に増加させることが示されました。関連する主要タンパク質の量も協調的に変化し、死を促すシグナルが上昇し、防御的タンパク質が減少し、カスパーゼと呼ばれる酵素が活性化するなど、ミトコンドリア経路によるアポトーシスを示すパターンが確認されました。
DNAと重要酵素への負荷
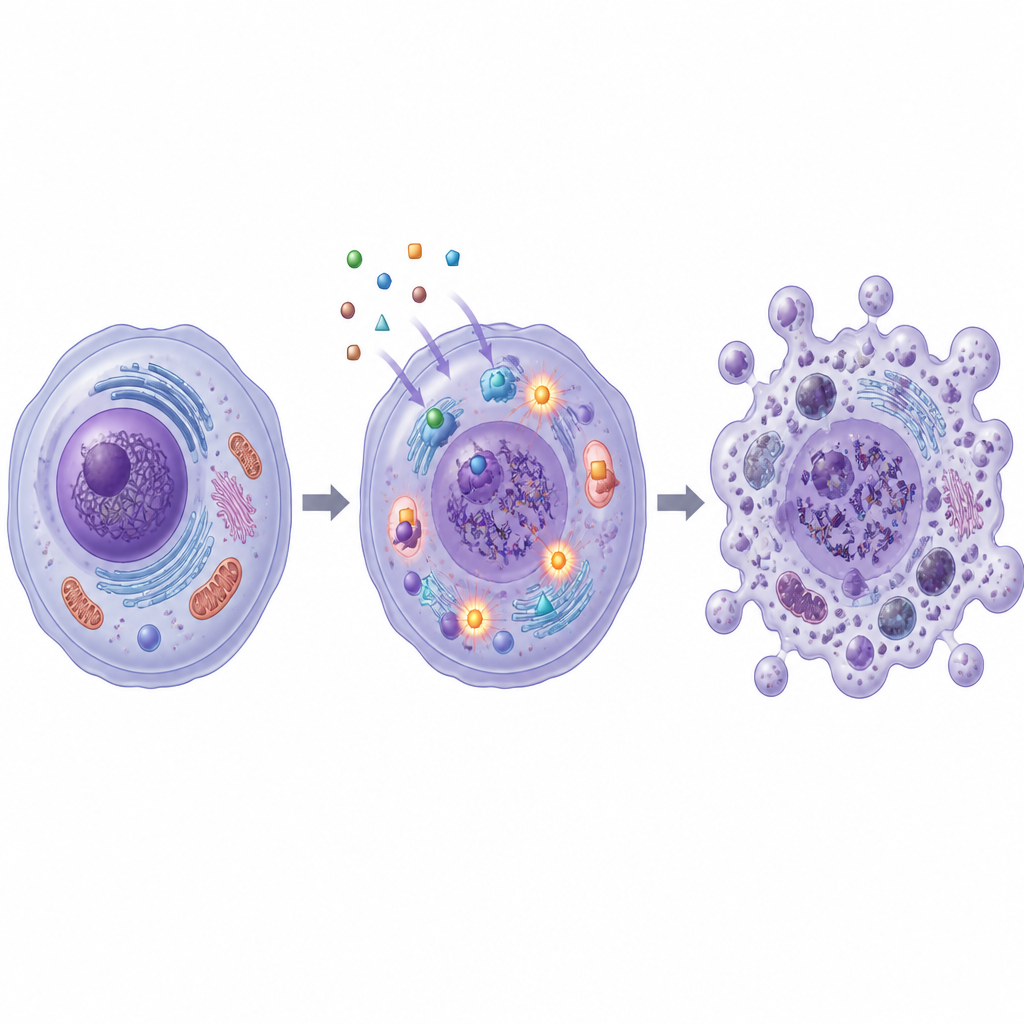
この研究はまた、これらの分子が内側からどのようにがん細胞を損なうかを探りました。SB1とSB2は細胞内で不安定な分子である活性酸素種の生成を増加させ、細胞構造やDNAに損傷を与え得ることが示されました。DNA断片の色素ベースの試験では、処理されたがん細胞が特にSB2でより多くの断片化した遺伝物質を持つことが示されました。同時に、両化合物はDNAの複製や修復時のねじれを管理するトポイソメラーゼIおよびIIの活性を低下させました。計算機シミュレーションはこれらの実験結果を支持し、SB1およびSB2がトポイソメラーゼIIやがん関連タンパク質である炭酸脱水酵素XIIの結合ポケットにぴったり収まる可能性を示しました。
たった一つの原子の役割
SB1とSB2はSB2のみに存在する1つの臭素原子によってのみ異なりますが、この小さな化学的修飾が明確な影響を及ぼしました。ほとんどの試験でSB2はがん細胞の増殖抑制、酸化ストレスの増加、DNA断片化、およびトポイソメラーゼ活性の阻害においてより強い能力を示しました。付加された臭素は分子の細胞膜やタンパク標的との相互作用を変え、細胞内への取り込みや重要部位への結合を改善した可能性があります。これは分子設計の微妙な変化が生物学的挙動を大きく変えうることを示しています。
今後の意義
総じて、これらのサルファジアジンベースのシッフ塩基、特にSB2は、培養皿内で正常細胞への害を抑えつつがん細胞を制御された自己破壊経路へ導く可能性があることを示唆しています。これらは酸化ストレスの増加、DNA損傷、およびがん細胞が増殖・分裂に依存する酵素の遮断という複合的な作用を通じて働くようです。これらの化合物は薬としてすぐに使えるわけではありませんが、化学者が将来の抗がん剤へと改良するための有望な出発点、すなわちリード分子を提供します。安定性や安全性を改善するさらなる改良が必要です。
引用: Nasr, E., Moustafa, A.H., El-Sayed, A.S.A. et al. Synthesis, characterization, and anticancer potency of sulfadiazine salicylaldehyde-based Schiff bases. Sci Rep 16, 15047 (2026). https://doi.org/10.1038/s41598-026-51752-z
キーワード: シッフ塩基, 抗がん化合物, アポトーシス, 活性酸素種, トポイソメラーゼ阻害