Clear Sky Science · it
Sintesi, caratterizzazione e potenza anticancerogena di basi di Schiff a partire da sulfadiazina e salicilaldeide
Perché questa ricerca è importante
I farmaci antitumorali spesso danneggiano le cellule sane insieme ai tumori, causando effetti collaterali difficili da gestire. Questo studio esplora due molecole da laboratorio strettamente correlate che mirano a indurre nelle cellule tumorali una forma controllata di autodistruzione, risparmiando per quanto possibile le cellule normali. Monitorando il comportamento di queste molecole nelle cellule tumorali, i ricercatori cercano indizi precoci che potrebbero guidare trattamenti futuri più sicuri e più mirati.
Progettare nuove piccole molecole
Il team si è concentrato su una famiglia di composti noti come basi di Schiff, una classe versatile di piccole molecole già nota per un ampio spettro di effetti biologici. Usando un blocco costitutivo comune agli antibiotici, la sulfadiazina, hanno creato due nuove varianti chiamate SB1 e SB2 aggiungendo strutture ad anello leggermente diverse. Accurati test chimici, comprese misure a infrarossi e risonanza magnetica nucleare, hanno confermato che entrambe le molecole possedevano la forma prevista e un'elevata purezza, essenziale prima di poter considerare attendibili i test biologici.
Test sulle cellule tumorali in laboratorio
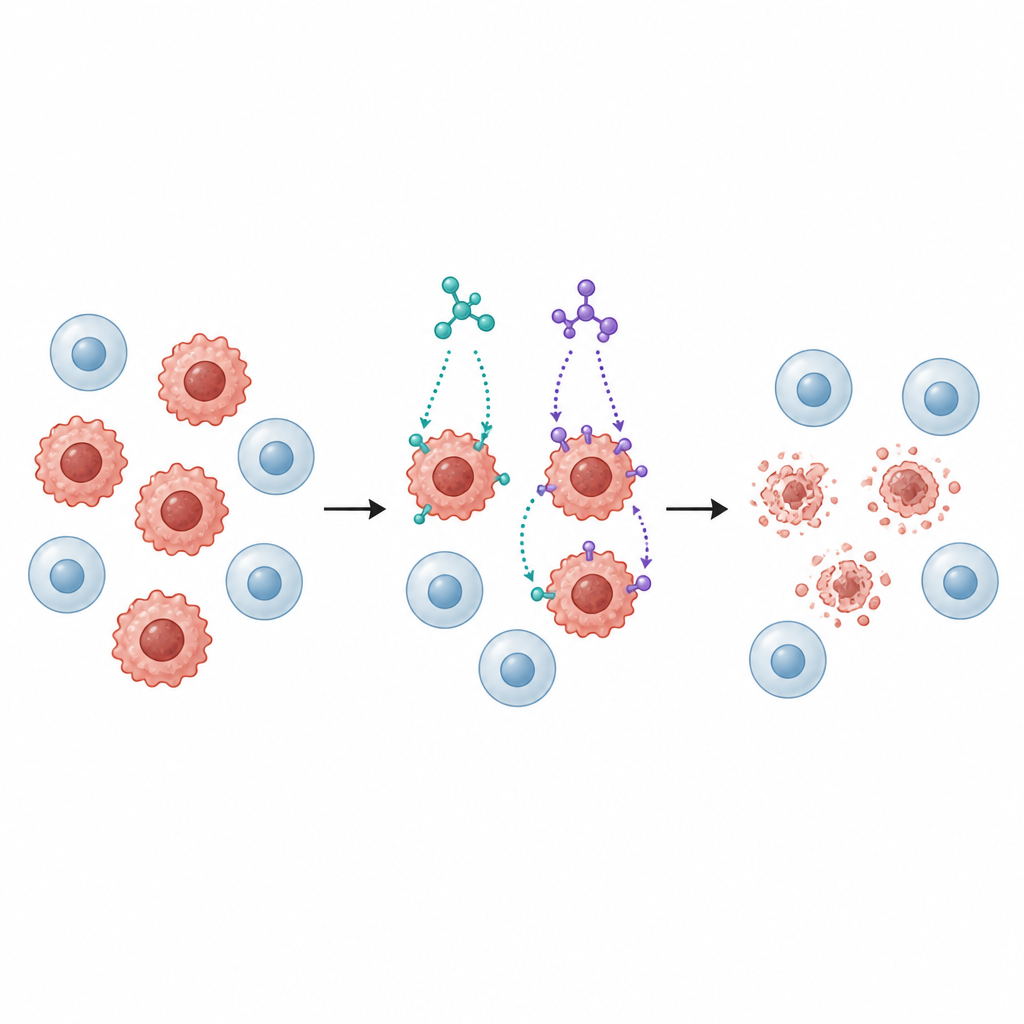
Successivamente, i ricercatori hanno esposto diverse linee cellulari tumorali umane a SB1 e SB2, incluse cellule di tumore al seno, colon, polmone, fegato e vescica, insieme a una linea di cellule polmonari normali come confronto. Entrambe le molecole rallentarono la crescita delle cellule tumorali in modo dipendente dalla dose, ma SB2 ha generalmente agito a dosi più basse rispetto a SB1, in particolare contro le cellule del seno (MCF 7) e del colon (HCT116). È importante che le cellule polmonari normali siano risultate meno sensibili rispetto alle cellule tumorali, suggerendo un certo grado di selettività, una qualità cruciale per un potenziale farmaco antitumorale.
Indurre un programma ordinato di morte cellulare
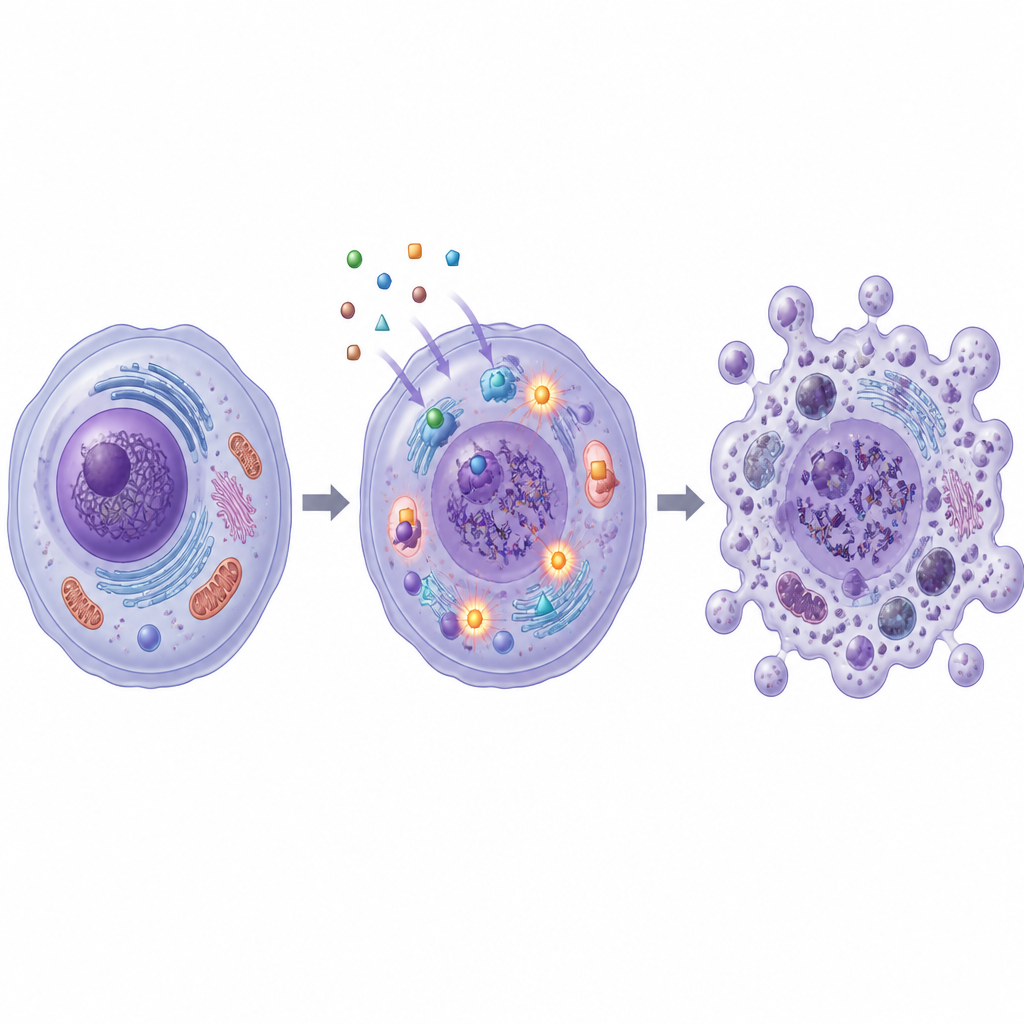
Fermare la crescita è utile solo se le cellule tumorali vengono anche eliminate. Il team ha quindi verificato se SB1 e SB2 inducano l'apoptosi, un programma di autodistruzione ordinato in cui le cellule si degradano senza riversare contenuti dannosi nei tessuti circostanti. Utilizzando un test citometrico basato su colorante, hanno mostrato che entrambe le molecole aumentarono notevolmente la frazione di cellule che attraversano le fasi iniziali e tardive dell'apoptosi nelle linee tumorali di seno e colon. I livelli di proteine chiave collegate a questa via si sono modificati in modo coordinato: i segnali pro-decesso sono aumentati, le proteine protettive sono diminuite e gli enzimi chiamati caspasi si sono attivati, tutti pattern coerenti con una via mitocondriale verso l'apoptosi.
Stress al DNA e agli enzimi vitali
Lo studio ha anche indagato come queste molecole danneggino le cellule tumorali dall'interno. SB1 e SB2 aumentarono la produzione di specie reattive dell'ossigeno, molecole instabili che possono danneggiare strutture cellulari e il DNA. Un test colorimetrico dei frammenti di DNA mostrò che le cellule tumorali trattate presentavano molto più materiale genetico frammentato, in particolare con SB2. Allo stesso tempo, entrambi i composti ridussero l'attività di enzimi chiamati topoisomerasi I e II, che gestiscono l'avvolgimento e lo svolgimento del DNA durante la replicazione e la riparazione. Simulazioni al computer supportarono questi riscontri di laboratorio, indicando che SB1 e SB2 possono adattarsi saldamente nelle tasche di legame della topoisomerasi II e di un altro bersaglio correlato al cancro, l'anidrasi carbonica XII.
Il ruolo di un singolo atomo
Sebbene SB1 e SB2 differiscano solo per la presenza di un singolo atomo di bromo su SB2, questa piccola modifica chimica ha avuto un impatto evidente. Nella maggior parte dei test, SB2 ha mostrato una capacità superiore di arrestare la crescita cellulare tumorale, aumentare lo stress ossidativo, frammentare il DNA e bloccare l'attività delle topoisomerasi. Il bromo aggiunto probabilmente modifica l'interazione della molecola con le membrane cellulari e con i target proteici, migliorandone l'ingresso nelle cellule e l'aderenza a siti critici al loro interno. Ciò illustra come cambiamenti sottili nel design molecolare possano rimodellare marcatamente il comportamento biologico.
Cosa significa per il futuro
Presa nel suo insieme, la ricerca suggerisce che queste basi di Schiff a derivazione di sulfadiazina, in particolare SB2, possono spingere le cellule tumorali verso un percorso controllato di autodistruzione risultando meno dannose per le cellule normali in piastre di laboratorio. Sembrano agire attraverso una combinazione di aumento dello stress ossidativo, danno al DNA e blocco di enzimi su cui le cellule tumorali fanno affidamento per crescere e dividersi. Pur non essendo pronti per essere usati come farmaci, forniscono punti di partenza promettenti, o molecole guida, che i chimici possono perfezionare in futuri agenti anticancerogeni con migliori profili di stabilità e sicurezza.
Citazione: Nasr, E., Moustafa, A.H., El-Sayed, A.S.A. et al. Synthesis, characterization, and anticancer potency of sulfadiazine salicylaldehyde-based Schiff bases. Sci Rep 16, 15047 (2026). https://doi.org/10.1038/s41598-026-51752-z
Parole chiave: Basi di Schiff, composti anticancro, apoptosi, specie reattive dell'ossigeno, inibizione della topoisomerasi