Clear Sky Science · pl
Synteza, charakterystyka i przeciwnowotworowa aktywność zasadowych zasad Schiffa pochodnych sulfadiazyny i salicylaldehydu
Dlaczego te badania są ważne
Leki przeciwnowotworowe często uszkadzają zdrowe komórki razem z guzami, powodując uciążliwe skutki uboczne. W tym badaniu zbadano dwie blisko spokrewnione, laboratoryjnie otrzymane cząsteczki, których celem jest skierowanie komórek nowotworowych na kontrolowaną formę samozniszczenia przy jak największym oszczędzeniu komórek normalnych. Śledząc, jak te molekuły zachowują się w komórkach nowotworowych, badacze poszukują wczesnych wskazówek, które mogłyby naprowadzić na bezpieczniejsze i bardziej precyzyjne terapie w przyszłości.
Projektowanie nowych małych cząsteczek
Zespół skupił się na rodzinie związków znanych jako zasady Schiffa, elastycznej klasie małych cząsteczek o szerokim spektrum efektów biologicznych. Wykorzystując powszechną jednostkę budulcową — antybiotyk sulfadiazynę — stworzyli dwie nowe warianty nazwane SB1 i SB2, przyłączając nieco inne pierścieniowe fragmenty. Staranne testy chemiczne, w tym pomiary w podczerwieni i spektroskopia magnetycznego rezonansu jądrowego, potwierdziły, że obie molekuły mają zamierzone struktury i wysoką czystość, co jest niezbędne przed przeprowadzeniem wiarygodnych testów biologicznych.
Testy na komórkach nowotworowych in vitro
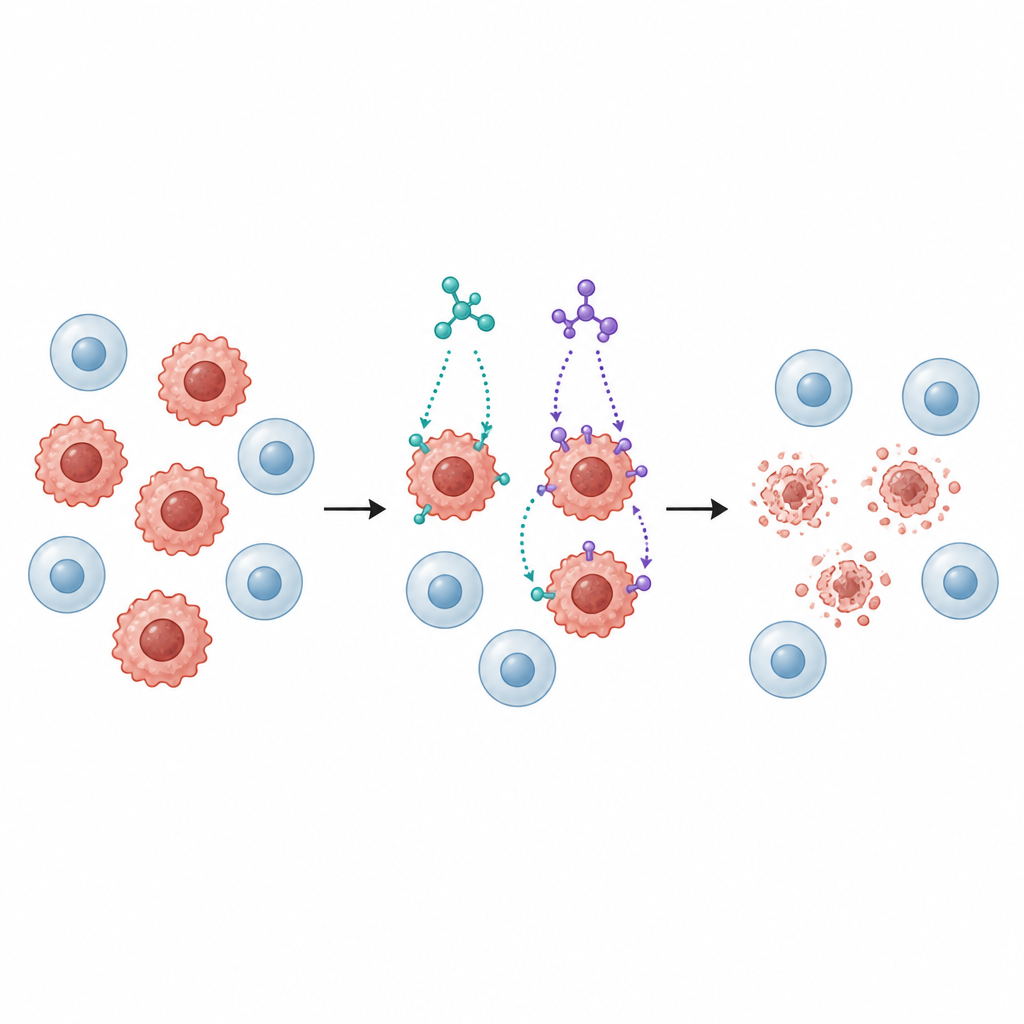
Następnie badacze poddali kilka ludzkich linii komórek nowotworowych działaniu SB1 i SB2, w tym komórki raka piersi, jelita grubego, płuc, wątroby i pęcherza, oraz linię komórek płucnych prawidłowych jako porównanie. Obie molekuły hamowały wzrost komórek nowotworowych w zależności od dawki, lecz SB2 zwykle działała przy niższych stężeniach niż SB1, szczególnie przeciwko komórkom raka piersi (MCF-7) i jelita grubego (HCT116). Co ważne, normalne komórki płuc były mniej wrażliwe niż komórki nowotworowe, co sugeruje pewien stopień selektywności — istotną cechę potencjalnego leku przeciwnowotworowego.
Wywoływanie uporządkowanego programu śmierci komórki
Powstrzymanie wzrostu jest przydatne tylko wtedy, gdy komórki nowotworowe zostaną także usunięte. Zespół zatem zbadał, czy SB1 i SB2 indukują apoptozę — uporządkowany program samozniszczenia, w którym komórki ulegają rozkładowi bez zalewania otaczających tkanek szkodliwymi treściami. Wykorzystując test przepływowej cytometrii oparty na barwniku, wykazano, że obie molekuły znacznie zwiększyły odsetek komórek przechodzących przez wczesne i późne stadia apoptozy w liniach raka piersi i jelita grubego. Poziomy kluczowych białek związanych z tą ścieżką zmieniały się skoordynowanie: sygnały pro‑śmierci wzrastały, białka ochronne malały, a enzymy zwane kaspazami ulegały aktywacji — wszystko to zgodne z mitochondrialną drogą prowadzącą do apoptozy.
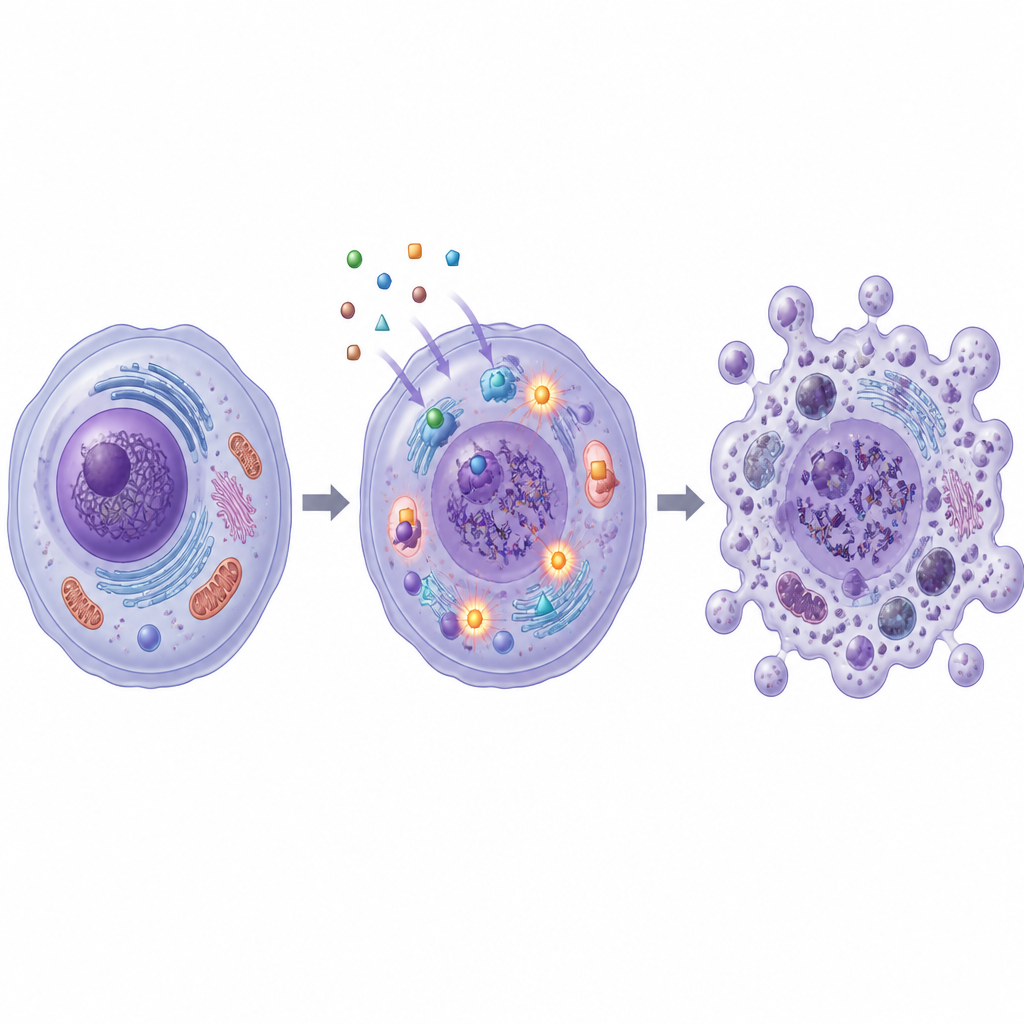
Obciążenie DNA i istotnych enzymów
Badanie sprawdziło także, jak te związki uszkadzają komórki nowotworowe od wewnątrz. SB1 i SB2 zwiększały produkcję reaktywnych form tlenu — niestabilnych cząsteczek mogących uszkadzać struktury komórkowe i DNA. Barwny test fragmentacji DNA wykazał, że traktowane komórki nowotworowe miały znacznie więcej złamanej materii genetycznej, zwłaszcza po ekspozycji na SB2. Równocześnie oba związki zmniejszały aktywność enzymów topoisomeraz I i II, które zarządzają skręcaniem i rozkręcaniem DNA podczas replikacji i naprawy. Symulacje komputerowe potwierdziły te wyniki laboratoryjne, wskazując, że SB1 i SB2 mogą dobrze dopasować się do wnęk wiążących topoizomerazy II oraz innego białka związanego z rakiem, anhydrazy węglanowej XII.
Rola pojedynczego atomu
Choć SB1 i SB2 różnią się tylko obecnością pojedynczego atomu bromu w SB2, ta niewielka modyfikacja chemiczna miała wyraźny wpływ. W większości testów SB2 wykazywała silniejszą zdolność do zatrzymywania wzrostu komórek nowotworowych, zwiększania stresu oksydacyjnego, fragmentowania DNA i blokowania aktywności topoizomeraz. Dodany brom prawdopodobnie zmienia sposób, w jaki cząsteczka oddziałuje z błonami komórkowymi i celami białkowymi, ułatwiając jej wnikanie do komórek oraz mocniejsze wiązanie z krytycznymi miejscami wewnątrz nich. Ilustruje to, jak subtelne zmiany w projekcie molekularnym mogą wyraźnie przekształcić zachowanie biologiczne.
Co to oznacza na przyszłość
Podsumowując, wyniki sugerują, że te zasady Schiffa oparte na sulfadiazynie, a szczególnie SB2, mogą skłaniać komórki nowotworowe do kontrolowanej ścieżki samozniszczenia przy równoczesnym mniejszym uszkodzeniu komórek normalnych w hodowlach in vitro. Wygląda na to, że działają poprzez połączenie zwiększonego stresu oksydacyjnego, uszkodzeń DNA i blokowania enzymów, od których komórki nowotworowe zależą w procesie wzrostu i podziału. Choć związki te nie nadają się jeszcze do stosowania jako leki, stanowią obiecujące punkty wyjścia — cząsteczki wiodące — które chemicy mogą udoskonalać, aby stworzyć przyszłe środki przeciwnowotworowe o lepszej stabilności i profilu bezpieczeństwa.
Cytowanie: Nasr, E., Moustafa, A.H., El-Sayed, A.S.A. et al. Synthesis, characterization, and anticancer potency of sulfadiazine salicylaldehyde-based Schiff bases. Sci Rep 16, 15047 (2026). https://doi.org/10.1038/s41598-026-51752-z
Słowa kluczowe: zasady Schiffa, związki przeciwnowotworowe, apoptoza, reaktywne formy tlenu, inhibicja topoizomerazy