Clear Sky Science · de
Synthese, Charakterisierung und antikanzerogene Wirksamkeit von sulfadiazin‑salicylaldehyd‑basierten Schiff‑Basen
Warum diese Forschung wichtig ist
Krebsmedikamente schädigen häufig gesunde Zellen ebenso wie Tumoren, was zu belastenden Nebenwirkungen führt. Diese Studie untersucht zwei eng verwandte, im Labor hergestellte Moleküle, die darauf abzielen, Krebszellen in eine kontrollierte Form der Selbstzerstörung zu treiben und normale Zellen möglichst zu schonen. Indem die Forscher verfolgen, wie sich diese Moleküle in Krebszellen verhalten, suchen sie frühe Hinweise, die zukünftig sicherere, präzisere Behandlungen leiten könnten.
Entwurf neuer kleiner Moleküle
Das Team konzentrierte sich auf eine Stoffklasse, die als Schiff‑Basen bekannt ist — eine flexible Gruppe kleiner Moleküle, die bereits für ein breites Spektrum biologischer Effekte bekannt ist. Mit dem häufig verwendeten Antibiotikabaustein Sulfadiazin schufen sie zwei neue Varianten, genannt SB1 und SB2, durch Anfügen leicht unterschiedlicher Ringsysteme. Sorgfältige chemische Analysen, darunter Infrarotspektroskopie und Kernspinresonanz, bestätigten, dass beide Moleküle die beabsichtigten Strukturen und eine hohe Reinheit besitzen, was vor jeglichen biologischen Tests entscheidend ist.
Tests an Krebszellen im Labor
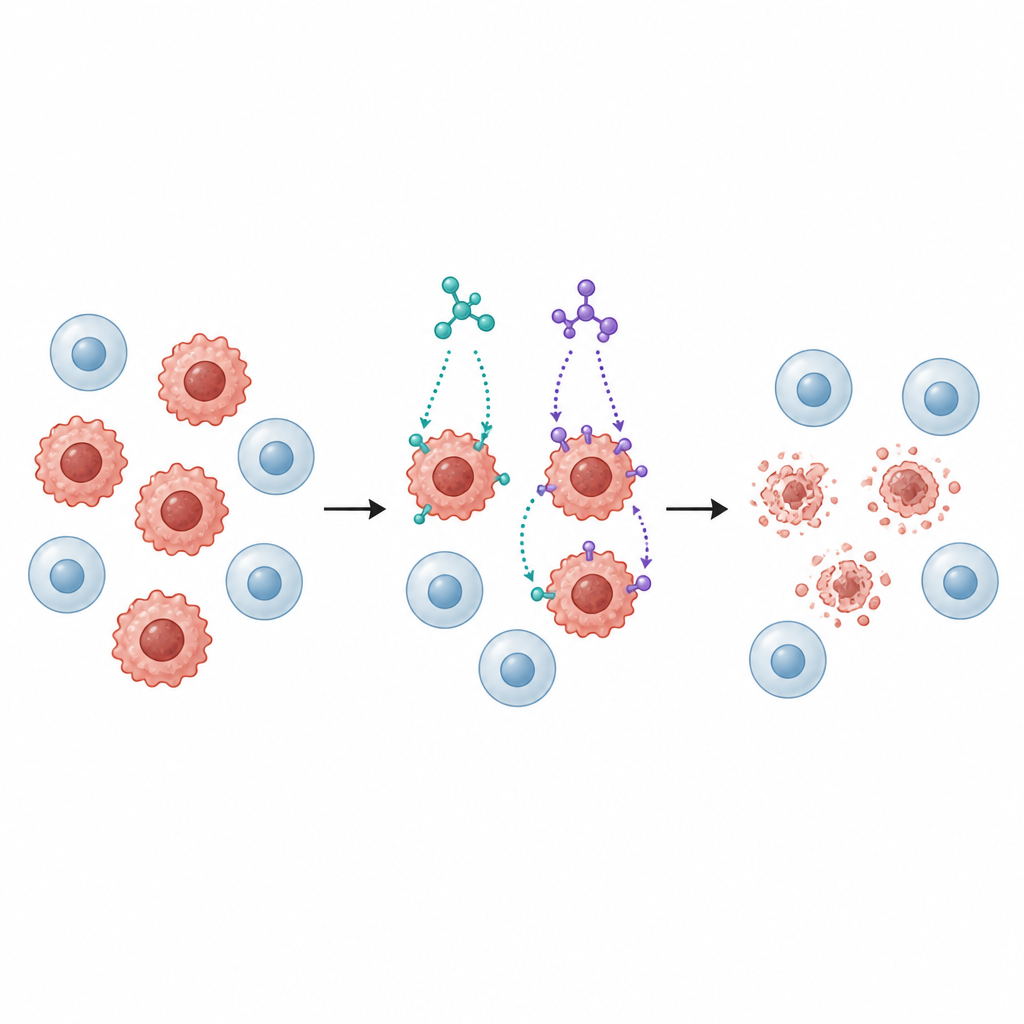
Anschließend setzten die Forscher mehrere humane Krebszelllinien SB1 und SB2 aus, darunter Brust‑, Darm‑, Lungen‑, Leber‑ und Blasenkrebszellen, sowie eine normale Lungenzelllinie zum Vergleich. Beide Moleküle verlangsamten das Wachstum von Krebszellen dosisabhängig, wobei SB2 meist bei geringeren Dosen wirksam war als SB1, insbesondere gegen Brust‑ (MCF‑7) und Darm‑ (HCT116) Krebszellen. Wichtig ist, dass normale Lungenzellen weniger empfindlich reagierten als Tumorzellen, was auf eine gewisse Selektivität hinweist — eine wichtige Eigenschaft für potentielle Krebstherapeutika.
Auslösen eines ordentlichen Zelltodprogramms
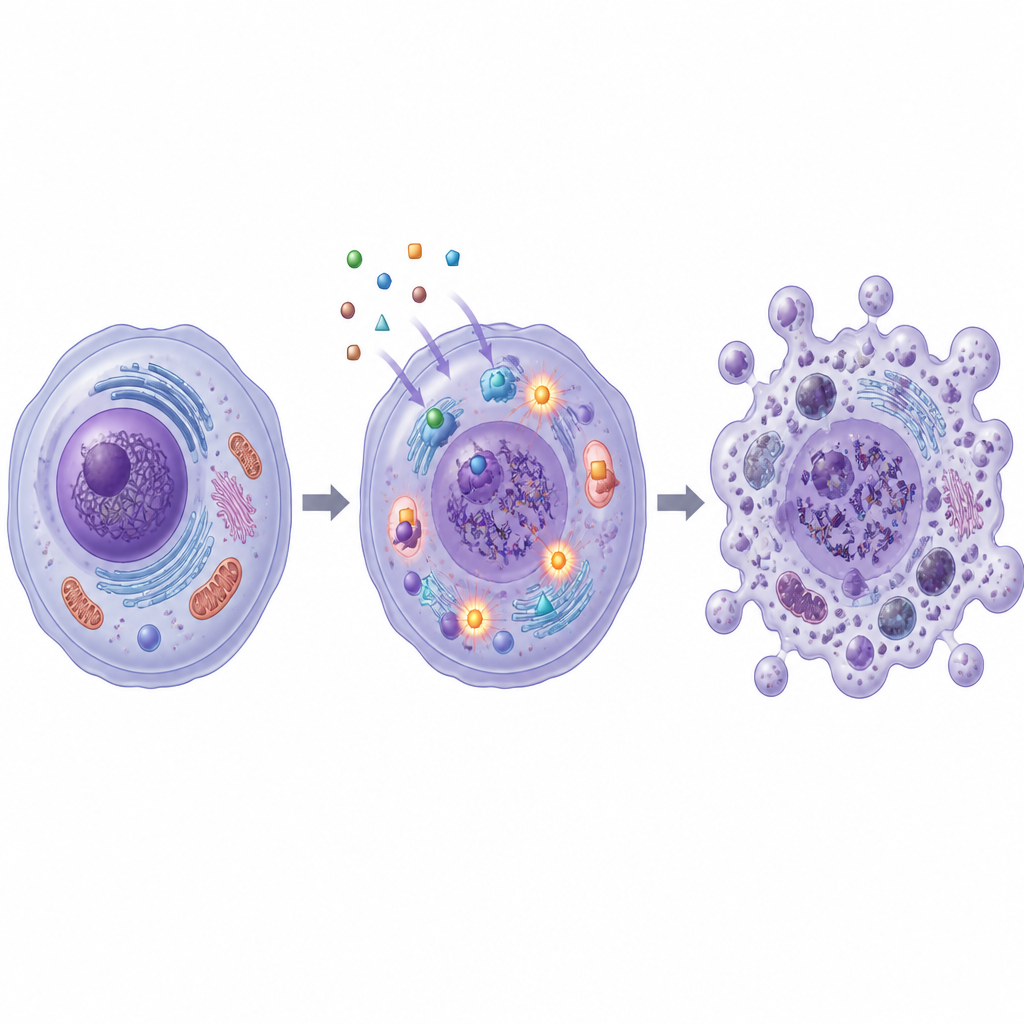
Wachstumshemmung ist nur nützlich, wenn Krebszellen auch entfernt werden. Das Team untersuchte daher, ob SB1 und SB2 Zellen in die Apoptose treiben — ein ordnungsgemäßes Selbstzerstörungsprogramm, bei dem Zellen ohne Auslaufen schädlicher Inhalte abgebaut werden. Mittels einer fluoreszenzbasierten Durchflusszytometrie zeigten sie, dass beide Moleküle den Anteil der Zellen in frühen und späten Apoptosephasen in Brust‑ und Darmzelllinien deutlich erhöhten. Die Spiegel wichtiger mit diesem Weg verknüpfter Proteine änderten sich koordiniert: pro‑apoptotische Signale stiegen, schützende Proteine fielen und Caspase‑Enzyme wurden aktiviert — Muster, die für einen mitochondrialen Apoptoseweg sprechen.
Belastung von DNA und lebenswichtigen Enzymen
Die Studie untersuchte außerdem, wie diese Moleküle Krebszellen von innen schädigen. SB1 und SB2 erhöhten die Bildung reaktiver Sauerstoffspezies, instabiler Moleküle, die Zellstrukturen und DNA schädigen können. Ein kolorimetrischer Test auf DNA‑Fragmente zeigte, dass behandelte Krebszellen deutlich mehr gebrochenes genetisches Material aufwiesen, insbesondere bei SB2. Gleichzeitig reduzierten beide Verbindungen die Aktivität der Enzyme Topoisomerase I und II, die das Auf‑ und Abwickeln der DNA beim Kopieren und Reparieren steuern. Computersimulationen stützten diese Laborbefunde und deuteten darauf hin, dass SB1 und SB2 sich passend in die Bindungstaschen von Topoisomerase II und einem weiteren krebsrelevanten Protein, der Carboanhydrase XII, einfügen können.
Die Rolle eines einzelnen Atoms
Obwohl sich SB1 und SB2 nur durch das Vorhandensein eines einzelnen Bromatoms in SB2 unterscheiden, hatte diese kleine chemische Modifikation deutliche Auswirkungen. In den meisten Tests zeigte SB2 größere Fähigkeit, das Krebszellwachstum zu hemmen, oxidativen Stress zu erhöhen, DNA zu fragmentieren und die Topoisomerase‑Aktivität zu blockieren. Das zusätzliche Brom verändert wahrscheinlich die Wechselwirkung des Moleküls mit Zellmembranen und Proteinzielen und verbessert so dessen Zellaufnahme und die Bindung an kritische Stellen. Das veranschaulicht, wie subtile Änderungen im Moleküldesign das biologische Verhalten deutlich umformen können.
Was das für die Zukunft bedeutet
Insgesamt deuten die Ergebnisse darauf hin, dass diese sulfadiazinbasierten Schiff‑Basen, insbesondere SB2, Krebszellen in einen kontrollierten Selbstzerstörungsweg treiben können, während sie in Zellkulturen weniger schädlich für normale Zellen sind. Sie scheinen durch eine Kombination aus erhöhtem oxidativem Stress, DNA‑Schäden und Hemmung von Enzymen zu wirken, auf die Krebszellen für Wachstum und Teilung angewiesen sind. Obwohl diese Verbindungen noch nicht als Medikamente einsatzbereit sind, liefern sie vielversprechende Ausgangspunkte beziehungsweise Leitmoleküle, die Chemiker zu zukünftigen antikanzerogenen Wirkstoffen mit verbesserter Stabilität und Sicherheitsprofil weiterentwickeln können.
Zitation: Nasr, E., Moustafa, A.H., El-Sayed, A.S.A. et al. Synthesis, characterization, and anticancer potency of sulfadiazine salicylaldehyde-based Schiff bases. Sci Rep 16, 15047 (2026). https://doi.org/10.1038/s41598-026-51752-z
Schlüsselwörter: Schiff‑Basen, antikanzerogene Verbindungen, Apoptose, reaktive Sauerstoffspezies, Topoisomerase‑Hemmung