Clear Sky Science · ar
تصنيع، توصيف، وقدرة مضادة للسرطان لمشتقات شيف من سلفاديازين وساليسيلالدهيد
لماذا تهمّ هذه الدراسة
غالبًا ما تتلف أدوية السرطان الخلايا السليمة إلى جانب الأورام، مما يتسبب في آثار جانبية صعبة. تستكشف هذه الدراسة مركبين مختبريين وثيقَي الصلة يهدفان إلى دفع خلايا السرطان إلى شكل مُتحكّم من الانتحار الخلوي مع الحفاظ على الخلايا الطبيعية قدر الإمكان. من خلال تتبّع كيفية تصرّف هذه الجزيئات داخل الخلايا السرطانية، يبحث الباحثون عن دلائل مبكرة قد توجه علاجات أكثر أمانًا ودقة في المستقبل.
تصميم جزيئات صغيرة جديدة
ركز الفريق على عائلة من المركبات تُعرف بقواعد شيف، وهي فئة مرنة من الجزيئات الصغيرة المعروفة بتأثيراتها البيولوجية المتنوعة. باستخدام كتلة بناء مألوفة من المضاد الحيوي، السلفاديازين، أنشأوا متغيرين جديدين سمّياهما SB1 وSB2 عن طريق ربط هياكل حلقية مختلفة قليلاً. أكدت اختبارات كيميائية دقيقة، بما في ذلك قياسات بالأشعة تحت الحمراء والرنين المغناطيسي النووي، أن كلا الجزيئين لهما الأشكال المطلوبة ونقاء عالٍ — وهو أمر أساسي قبل الاعتماد على أي اختبارات بيولوجية.
اختبار خلايا سرطان في المختبر
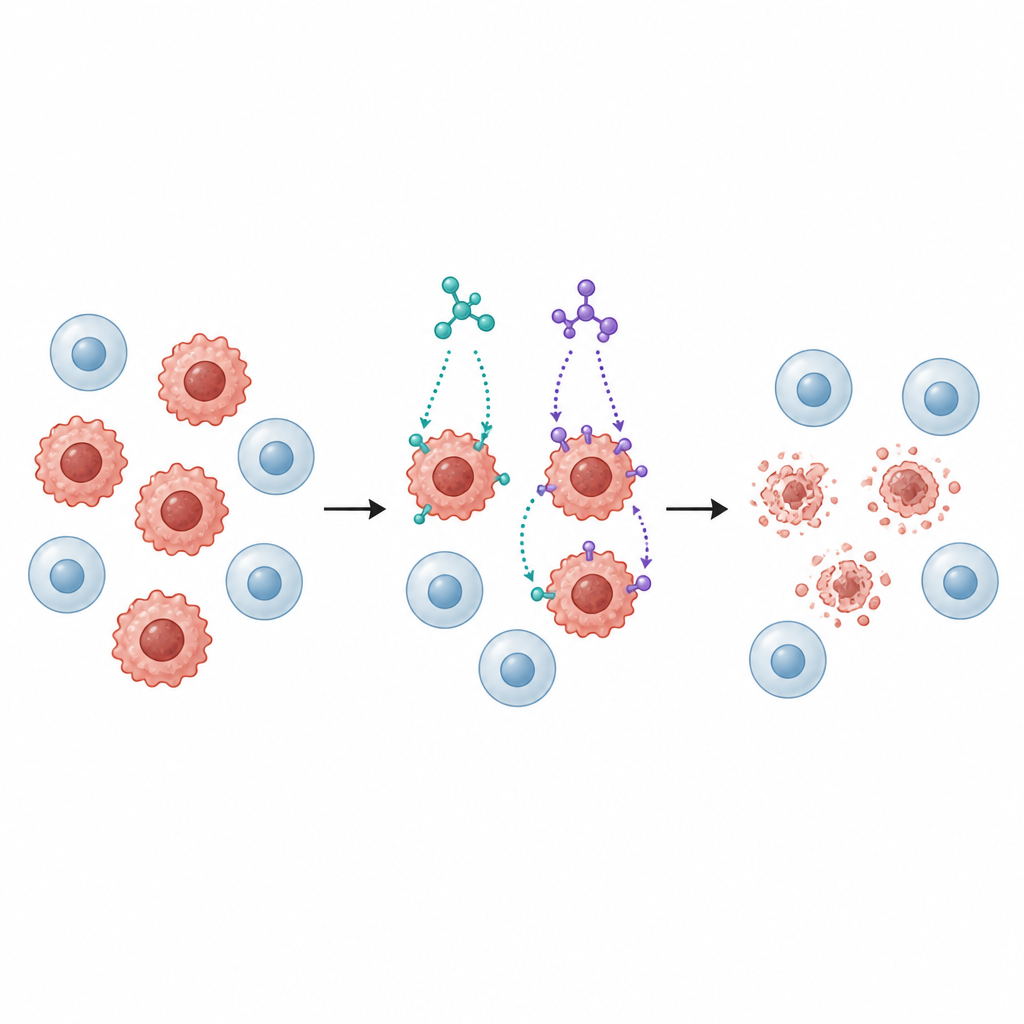
بعد ذلك عرّض الباحثون عدة سلالات من الخلايا السرطانية البشرية لـ SB1 وSB2، بما في ذلك خلايا سرطان الثدي والقولون والرئة والكبد والمثانة، إلى جانب سلالة خلوية رئوية طبيعية للمقارنة. بطأ كلا المولّفين نمو الخلايا السرطانية بطريقة تعتمد على الجرعة، لكن SB2 غالبًا ما كان فعالًا بجرعات أقل من SB1، خصوصًا ضد خلايا سرطان الثدي (MCF 7) والقولون (HCT116). والأهم أن خلايا الرئة الطبيعية كانت أقل حساسية من خلايا الورم، مما يوحي بدرجة من الانتقائية — وهي صفة مهمة لأي دواء مضاد للسرطان محتمل.
تحفيز برنامج موت خلوي منظم
إيقاف النمو مفيد فقط إذا أُزيلت الخلايا السرطانية أيضًا. لذلك فحص الفريق ما إذا كان SB1 وSB2 يدفعان الخلايا إلى الموت المبرمج (الاستماتة)، وهو برنامج ذاتي منظم تتحلل فيه الخلايا دون أن تسكب محتويات ضارة في الأنسجة المحيطة. باستخدام اختبار تلوين يعتمد على قياس التدفق الخلوي، أظهروا أن كلا المركبين زادا بشكل كبير من نسبة الخلايا التي تمر بمراحل مبكرة ومتأخرة من الاستماتة في خطوط سرطان الثدي والقولون. تغيّرت مستويات بروتينات رئيسية مرتبطة بهذا المسار بطريقة منسقة: ارتفعت إشارات الاستماتة، وانخفضت البروتينات الواقية، وتفعّلت إنزيمات تسمى الكاسبيزات — كلها أنماط تتوافق مع مسار ميتوكوندري نحو الاستماتة.
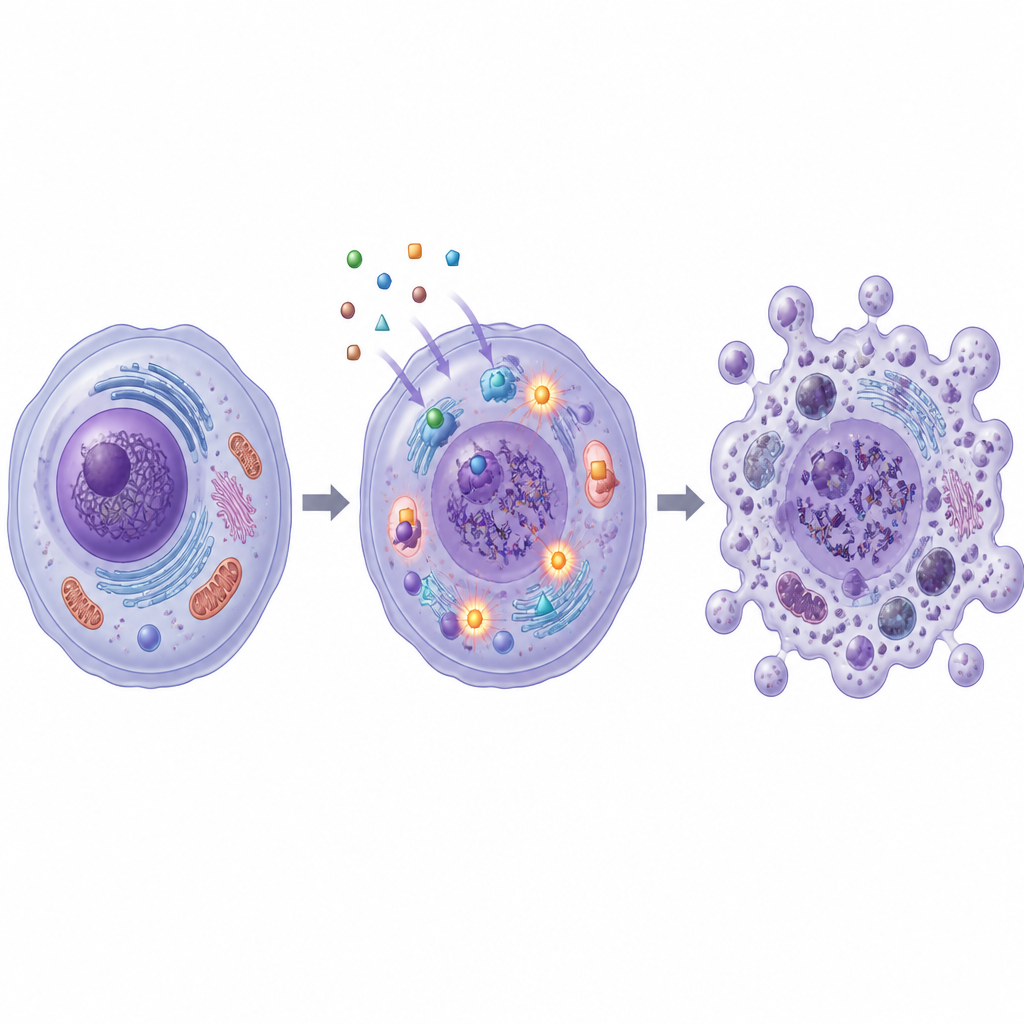
إجهاد الحمض النووي والإنزيمات الحيوية
تحققت الدراسة أيضاً من كيفية إلحاق هذه الجزيئات بالضرر داخل الخلايا السرطانية. زاد كل من SB1 وSB2 من إنتاج أنواع الأكسجين التفاعلية، وهي جزيئات غير مستقرة يمكن أن تضر بالهياكل الخلوية والحمض النووي. أظهر اختبار لوني لكسور الحمض النووي أن الخلايا المعالجة تحمل مزيدًا من المادة الوراثية المتكسرة، خاصة مع SB2. في الوقت نفسه، خفّضت كلتا المركبتين نشاط إنزيمات تسمى التوبويزوميراز I وII، التي تدير لفّ وفكّ لفّ الحمض النووي أثناء نسخه وإصلاحه. دعمت المحاكاة الحاسوبية هذه النتائج المخبرية، مشيرة إلى أن SB1 وSB2 يمكن أن تتناسبا بإحكام مع جيوب الارتباط لتوبويزوميراز II وبروتين مرتبط بالسرطان آخر، الكربونيك أنهيدراز XII.
دور ذرة واحدة
على الرغم من أن SB1 وSB2 يختلفان فقط بوجود ذرة بروم واحدة في SB2، فقد كان لهذا التعديل الكيميائي الصغير تأثير واضح. في معظم الاختبارات، أظهر SB2 قدرة أقوى على إيقاف نمو الخلايا السرطانية، وزيادة الإجهاد التأكسدي، وتفتيت الحمض النووي، وعرقلة نشاط التوبويزوميراز. من المحتمل أن يغيّر البروم المضاف كيفية تفاعل الجزيء مع أغشية الخلايا والأهداف البروتينية، محسنًا دخوله إلى الخلايا وقبضته على مواقع حيوية بداخلها. هذا يوضّح كيف يمكن لتغييرات طفيفة في التصميم الجزيئي أن تعيد تشكيل السلوك البيولوجي بشكل ملحوظ.
ماذا يعني هذا للمستقبل
مجتمعة، تشير النتائج إلى أن قواعد شيف المبنية على السلفاديازين هذه، وعلى الأخص SB2، يمكن أن تدفع الخلايا السرطانية نحو مسار تدمير ذاتي مُتحكّم مع أن تكون أقل ضررًا للخلايا الطبيعية في أطباق المختبر. يبدو أنها تعمل عبر مزيج من زيادة الإجهاد التأكسدي، وإلحاق ضرر بالحمض النووي، وحجب إنزيمات تعتمد عليها الخلايا السرطانية للنمو والانقسام. وعلى الرغم من أن هذه المركبات ليست جاهزة لاستخدامها كأدوية بعد، فإنها توفر نقاط انطلاق واعدة، أو جزيئات رائدة، يمكن للكيميائيين تحسينها لتصبح عوامل مضادة للسرطان مستقبلية ذات ثبات وسلامة محسّنين.
الاستشهاد: Nasr, E., Moustafa, A.H., El-Sayed, A.S.A. et al. Synthesis, characterization, and anticancer potency of sulfadiazine salicylaldehyde-based Schiff bases. Sci Rep 16, 15047 (2026). https://doi.org/10.1038/s41598-026-51752-z
الكلمات المفتاحية: قواعد شيف, مركبات مضادة للسرطان, الموت الخلوي المبرمج (الاستماتة), أنواع الأكسجين التفاعلية, تثبيط التوبويزوميراز