Clear Sky Science · tr
Sülfadiazin salisilaldehit bazlı Schiff bazlarının sentezi, karakterizasyonu ve antikanser etkinliği
Bu araştırma neden önemli
Kanser ilaçları genellikle tümörlerle birlikte sağlıklı hücrelere de zarar vererek zor yan etkilere yol açar. Bu çalışma, normal hücreleri olabildiğince korurken kanser hücrelerini kontrollü bir biçimde yok etmeyi amaçlayan, laboratuvarda üretilmiş iki yakından ilişkili molekülü inceliyor. Araştırmacılar bu moleküllerin kanser hücrelerindeki davranışını izleyerek gelecekte daha güvenli ve daha hedefe yönelik tedaviler için yol gösterici erken ipuçları arıyor.
Yeni küçük moleküller tasarlamak
Araştırma ekibi, geniş bir biyolojik etki yelpazesiyle tanınan esnek bir küçük molekül sınıfı olan Schiff bazlarına odaklandı. Ortak bir antibiyotik yapı taşı olan sülfadiazini kullanarak, hafifçe farklı halka yapıları bağlayarak SB1 ve SB2 adında iki yeni varyant yarattılar. Kızılötesi spektroskopi ve nükleer manyetik rezonans dahil dikkatli kimyasal testler, her iki molekülün de amaçlanan şekle ve yüksek saflığa sahip olduğunu doğruladı; bu, herhangi bir biyolojik testin güvenilir olması için elzemdir.
Laboratuvarda kanser hücrelerini test etmek
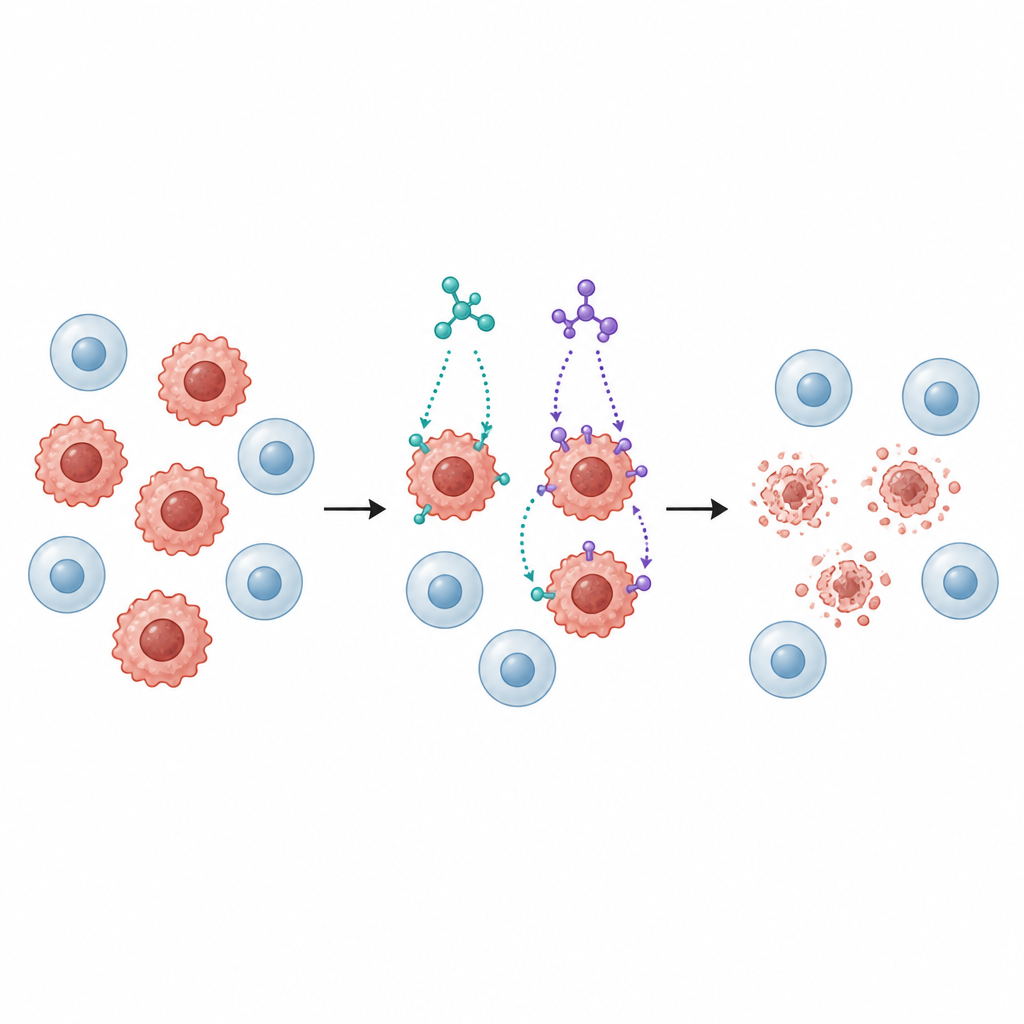
Sonraki adımda araştırmacılar, meme, kolon, akciğer, karaciğer ve mesane kanseri dahil olmak üzere birkaç insan kanser hücre hattını SB1 ve SB2 ile ve karşılaştırma için bir normal akciğer hücre hattıyla muamele etti. Her iki molekül de doz bağımlı olarak kanser hücresi çoğalmasını yavaşlattı, ancak SB2 genellikle özellikle meme (MCF 7) ve kolon (HCT116) kanser hücrelerine karşı daha düşük dozlarda etkiliydi. Önemli olarak, normal akciğer hücreleri tümör hücrelerinden daha az duyarlıydı; bu da potansiyel bir kanser ilacı için önemli olan bir dereceye kadar seçiciliği gösteriyor.
Düzgün bir hücre ölüm programını tetiklemek
Büyümeyi durdurmak, kanser hücreleri aynı zamanda ortadan kaldırılmadıkça yeterli değildir. Bu nedenle ekip, SB1 ve SB2’nin hücreleri etrafa zararlı içerik yaymadan bozunan bir düzenli öz yok etme programı olan apoptoza itip itmediğini inceledi. Boya bazlı akım sitometrisi testi kullanarak, her iki molekülün de meme ve kolon kanser hatlarında erken ve geç apoptoz aşamalarında olan hücrelerin oranını önemli ölçüde artırdığını gösterdiler. Bu yolla ilişkili kilit protein seviyeleri koordineli bir şekilde değişti: ölüm sinyalleri arttı, koruyucu proteinler azaldı ve kaspaz adı verilen enzimler aktive oldu; bunların tümü mitokondriyal bir apoptoz yolunu destekleyen desenlerdir.
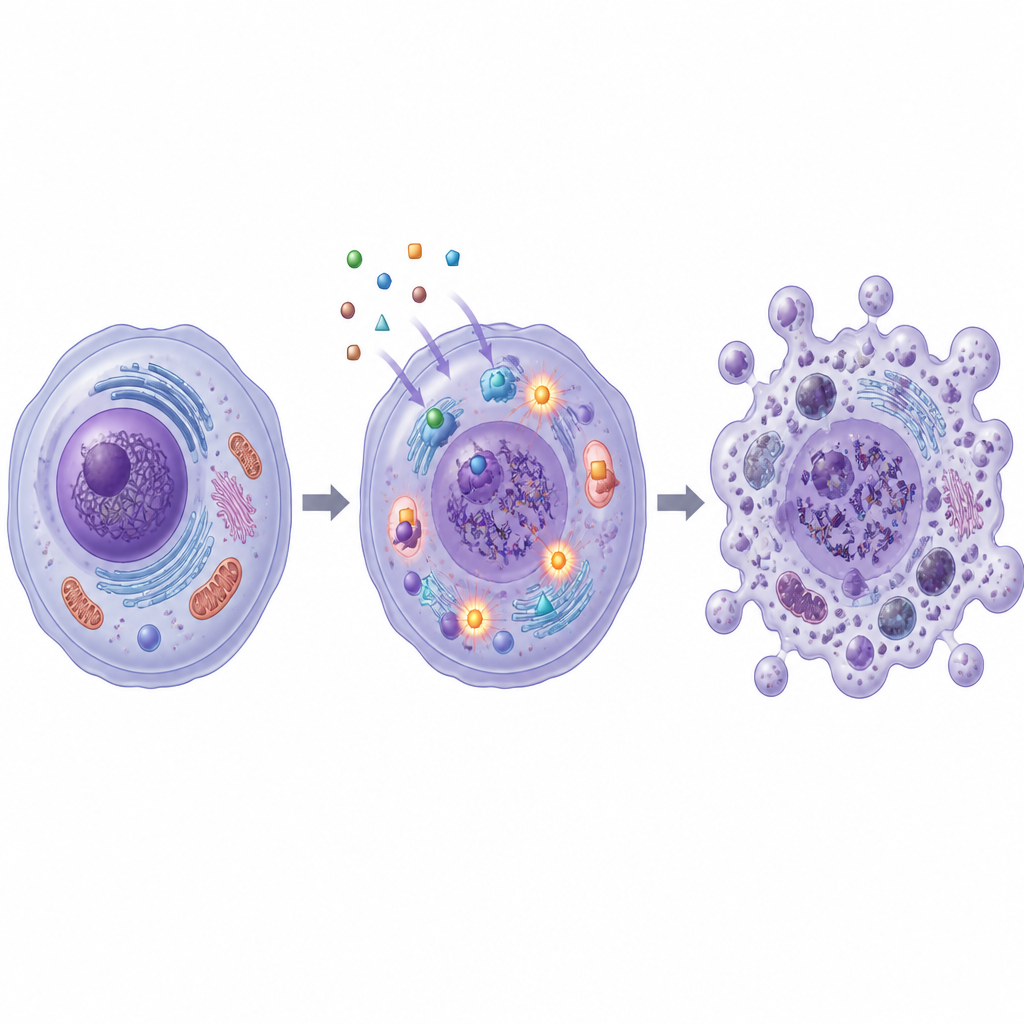
DNA’yı ve hayati enzimleri strese sokmak
Çalışma ayrıca bu moleküllerin kanser hücrelerine içeriden nasıl zarar verdiğini araştırdı. SB1 ve SB2, hücresel yapılara ve DNA’ya zarar verebilen kararsız moleküller olan reaktif oksijen türlerinin üretimini artırdı. Renk bazlı bir DNA fragman testi, muamele edilen kanser hücrelerinin özellikle SB2 ile çok daha fazla kırık genetik materyal taşıdığını gösterdi. Aynı zamanda her iki bileşik de DNA’nın kopyalanması ve tamiri sırasında bükülmeyi yöneten topoizomeraz I ve II adlı enzimlerin aktivitesini azalttı. Bilgisayar simülasyonları bu laboratuvar bulgularını destekleyerek SB1 ve SB2’nin topoizomeraz II ve kanserle ilişkili bir diğer protein olan karbonik anhidraz XII’nin bağlanma ceplerine uyum sağlayabildiğini gösterdi.
Tek bir atomun rolü
SB1 ve SB2 sadece SB2’de bulunan tek bir brom atomu ile farklı olmasına rağmen, bu küçük kimyasal değişiklik belirgin bir etki yarattı. Çoğu testte SB2, kanser hücresi büyümesini durdurma, oksidatif stresi artırma, DNA’yı parçalama ve topoizomeraz aktivitesini bloke etme konusunda daha güçlü bir yetenek gösterdi. Eklenen brom muhtemelen molekülün hücre zarları ve hedef proteinlerle etkileşimini değiştirerek hücreye girişini ve içindeki kritik noktalara tutunmasını iyileştiriyor. Bu, moleküler tasarımdaki ince değişikliklerin biyolojik davranışı önemli ölçüde değiştirebileceğini gösterir.
İleriye dönük anlamı
Bir arada değerlendirildiğinde, bu sülfadiazin bazlı Schiff bazlarının, özellikle SB2’nin, kanser hücrelerini kontrollü bir öz yok etme yoluna itebildiği ve laboratuvar kaplarında normal hücrelere kıyasla daha az zararlı olduğu görülüyor. Bu bileşikler artan oksidatif stres, DNA hasarı ve kanser hücrelerinin büyüme ve bölünme için dayandığı enzimlerin bloke edilmesi kombinasyonu yoluyla etki ediyor gibi görünüyor. Bu bileşikler ilaç olarak kullanılmaya hazır olmasalar da, kimyacıların daha iyi stabilite ve güvenlik profillerine sahip gelecekteki antikanser ajanlara dönüştürebilecekleri umut verici başlangıç noktaları, yani kurşun molekülleri sağlıyorlar.
Atıf: Nasr, E., Moustafa, A.H., El-Sayed, A.S.A. et al. Synthesis, characterization, and anticancer potency of sulfadiazine salicylaldehyde-based Schiff bases. Sci Rep 16, 15047 (2026). https://doi.org/10.1038/s41598-026-51752-z
Anahtar kelimeler: Schiff bazları, antikanser bileşikler, apoptoz, reaktif oksijen türleri, topoizomeraz inhibisyonu