Clear Sky Science · ru
Синтез, характеристика и противораковая активность шифовых оснований на основе сульфадиазина и салицилальдегида
Почему это исследование важно
Противораковые препараты часто повреждают здоровые клетки вместе с опухолями, вызывая тяжёлые побочные эффекты. В этом исследовании изучают две близкие по структуре синтетические молекулы, которые стремятся инициировать управляемую самоуничтожение раковых клеток, максимально щадя нормальные клетки. Отслеживая поведение этих молекул в раковых клетках, исследователи ищут ранние подсказки, которые могут направить разработку более безопасных и точных терапий в будущем.
Проектирование новых малых молекул
Команда сосредоточилась на семействе соединений, известных как шифовы основания — гибком классе малых молекул, уже известном своим широким спектром биологических эффектов. Используя в качестве строительного блока распространённый антибиотик сульфадиазин, они создали две новые разновидности, названные SB1 и SB2, присоединив к ним слегка разные циклические фрагменты. Тщательные химические тесты, включая инфракрасную спектроскопию и ядерный магнитный резонанс, подтвердили, что обе молекулы имеют предполагаемую структуру и высокую чистоту, что важно для достоверности последующих биологических исследований.
Испытания на раковых клетках в лаборатории
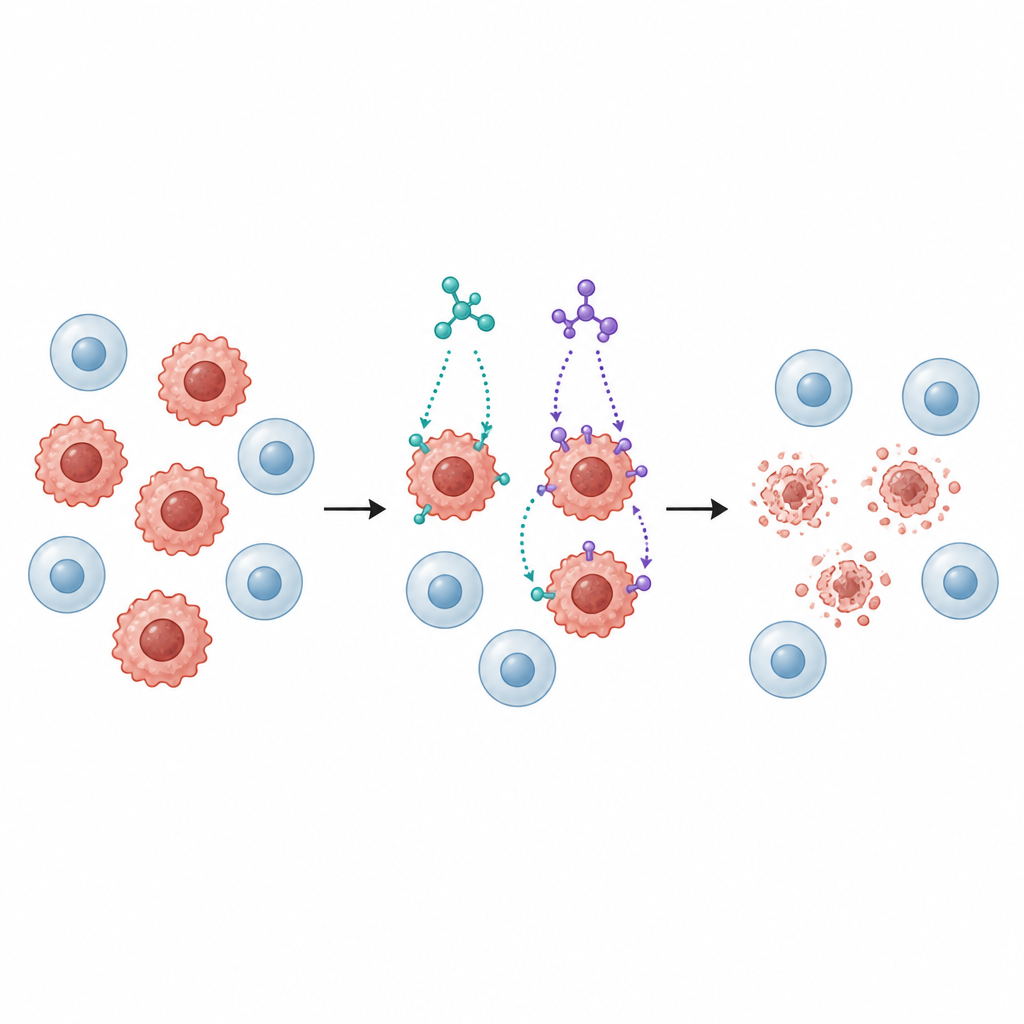
Далее исследователи подвергли воздействию SB1 и SB2 несколько линий человеческих раковых клеток, включая клетки рака молочной железы, толстой кишки, лёгкого, печени и мочевого пузыря, а также нормальную линию лёгочных клеток для сравнения. Обе молекулы замедляли рост раковых клеток в дозозависимом режиме, но SB2, как правило, действовала при более низких концентрациях, чем SB1, особенно против клеток молочной железы (MCF‑7) и толстой кишки (HCT116). Важно, что нормальные лёгочные клетки были менее чувствительны, чем опухолевые, что указывает на некоторую степень селективности — важное качество для потенциального противоракового препарата.
Инициация упорядоченной программы гибели клетки
Остановка роста полезна только в том случае, если раковые клетки действительно удаляются. Поэтому команда изучила, не индуцируют ли SB1 и SB2 апоптоз — упорядоченную программу самоуничтожения, при которой клетки распадаются, не выливая вредных веществ в окружающие ткани. С помощью красителя и проточной цитометрии они показали, что обе молекулы значительно увеличивают долю клеток, находящихся на ранних и поздних стадиях апоптоза в линиях рака молочной железы и толстой кишки. Уровни ключевых белков, связанных с этим путём, сместились согласованно: повышились проапоптотические сигналы, снизились защитные белки, а ферменты — каспазы — активировались, что соответствует митохондриальному механизму апоптоза.
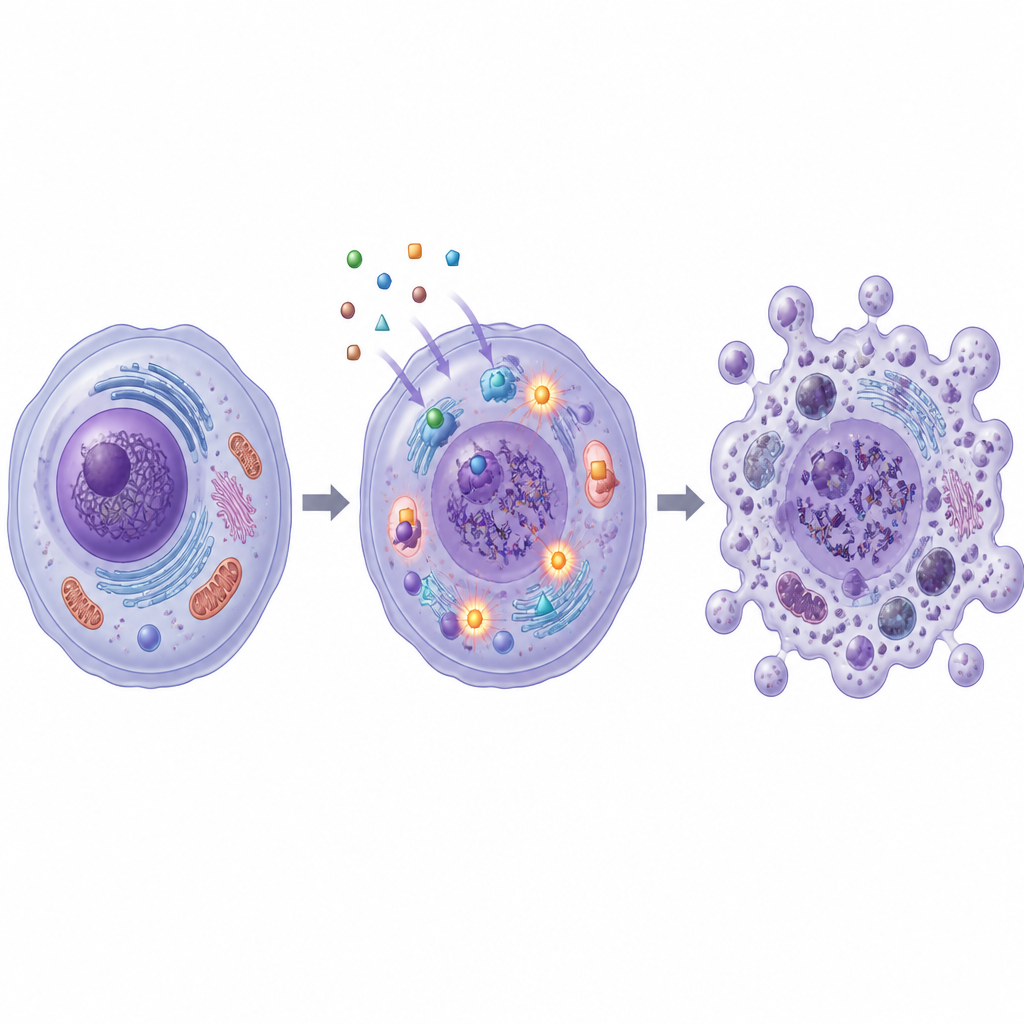
Повреждение ДНК и жизненно важных ферментов
Исследование также изучало, как эти молекулы повреждают раковые клетки изнутри. SB1 и SB2 увеличивали образование реактивных форм кислорода — нестабильных молекул, способных повреждать структурные элементы клетки и ДНК. Цветовой тест на фрагменты ДНК показал, что обработанные клетки имели гораздо больше разорванного генетического материала, особенно при обработке SB2. Одновременно оба соединения снижали активность ферментов топоизомераз I и II, управляющих скручиванием и раскручиванием ДНК при репликации и ремонте. Компьютерное моделирование подтвердило эти лабораторные наблюдения, показав, что SB1 и SB2 могут удобно размещаться в карманах связывания топоизомеразы II и другого белка, связанного с раком, карбоангидразы XII.
Роль одного атома
Хотя SB1 и SB2 отличаются только наличием одного атома брома в SB2, это небольшое химическое изменение оказало заметное влияние. В большинстве тестов SB2 проявляла более сильную способность останавливать рост раковых клеток, повышать окислительный стресс, фрагментировать ДНК и блокировать активность топоизомераз. Добавленный бром, вероятно, изменяет взаимодействие молекулы с клеточными мембранами и белковыми мишенями, улучшая её проникновение в клетки и сцепление с критическими сайтами внутри них. Это иллюстрирует, как тонкие изменения в молекулярном дизайне могут существенно изменить биологическое поведение.
Что это значит для дальнейшей работы
В сумме полученные результаты указывают, что эти шифовы основания на основе сульфадиазина, особенно SB2, способны направлять раковые клетки к управляемой программе самоуничтожения, при этом проявляя меньшую токсичность для нормальных клеток в лабораторных условиях. Они, по-видимому, действуют через комбинацию повышения окислительного стресса, повреждения ДНК и блокирования ферментов, на которые опираются раковые клетки для роста и деления. Хотя эти соединения ещё не готовы к применению в клинике, они представляют собой многообещающие стартовые молекулы, которые химики могут дорабатывать в будущие противораковые агенты с улучшенной стабильностью и профилем безопасности.
Цитирование: Nasr, E., Moustafa, A.H., El-Sayed, A.S.A. et al. Synthesis, characterization, and anticancer potency of sulfadiazine salicylaldehyde-based Schiff bases. Sci Rep 16, 15047 (2026). https://doi.org/10.1038/s41598-026-51752-z
Ключевые слова: шифовы основания, противораковые соединения, апоптоз, реактивные формы кислорода, ингибирование топоизомераз