Clear Sky Science · fr
Synthèse, caractérisation et puissance anticancéreuse de bases de Schiff dérivées de la sulfadiazine et du salicylaldéhyde
Pourquoi cette recherche est importante
Les médicaments anticancéreux endommagent souvent les cellules saines en même temps que les tumeurs, entraînant des effets secondaires lourds. Cette étude explore deux molécules de synthèse étroitement apparentées qui visent à pousser les cellules cancéreuses vers une forme contrôlée d'autodestruction tout en épargnant autant que possible les cellules normales. En suivant le comportement de ces molécules dans des cellules cancéreuses, les chercheurs recherchent des indices précoces susceptibles d'orienter des traitements futurs plus sûrs et plus précis.
Conception de nouvelles petites molécules
L'équipe s'est concentrée sur une famille de composés connus sous le nom de bases de Schiff, une classe flexible de petites molécules déjà reconnues pour une large gamme d'effets biologiques. En utilisant un élément de base issu d'un antibiotique courant, la sulfadiazine, ils ont créé deux variantes nommées SB1 et SB2 en fixant des cycles légèrement différents. Des tests chimiques rigoureux, y compris des mesures infrarouges et la résonance magnétique nucléaire, ont confirmé que les deux molécules présentaient la géométrie prévue et une grande pureté, condition indispensable avant de pouvoir faire confiance aux essais biologiques.
Tests sur des cellules cancéreuses en laboratoire
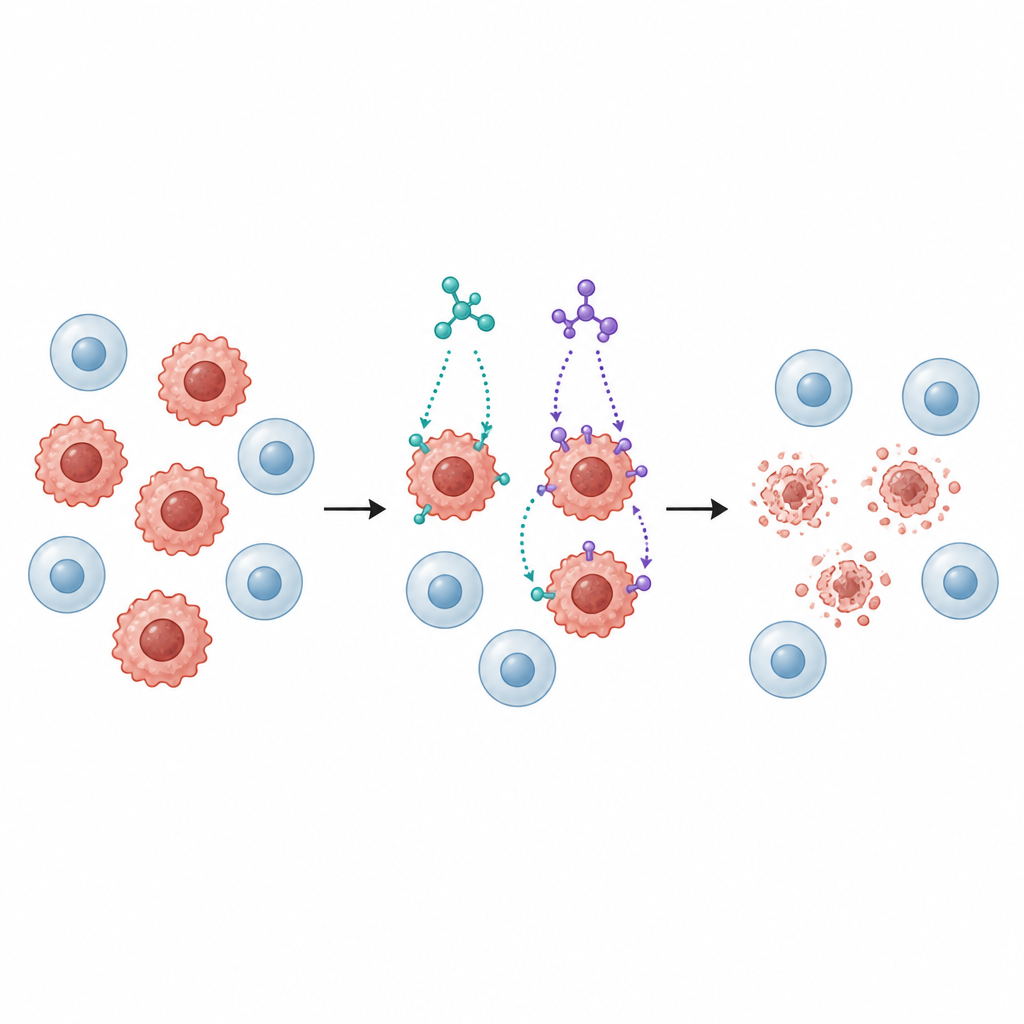
Ensuite, les chercheurs ont exposé plusieurs lignées cellulaires cancéreuses humaines à SB1 et SB2, notamment des cancers du sein, du côlon, du poumon, du foie et de la vessie, ainsi qu'une lignée de cellules pulmonaires normales pour comparaison. Les deux molécules ont ralenti la croissance des cellules cancéreuses de manière dose‑dépendante, mais SB2 a généralement agi à des doses plus faibles que SB1, en particulier contre les cellules du sein (MCF‑7) et du côlon (HCT116). Fait important, les cellules pulmonaires normales étaient moins sensibles que les cellules tumorales, suggérant un certain degré de sélectivité, une qualité importante pour tout médicament anticancéreux potentiel.
Déclenchement d'un programme ordonné de mort cellulaire
Arrêter la croissance n'a de valeur que si les cellules cancéreuses sont aussi éliminées. L'équipe a donc examiné si SB1 et SB2 poussent les cellules vers l'apoptose, un programme ordonné d'autodestruction dans lequel les cellules se décomposent sans déverser de contenu nocif dans les tissus environnants. À l'aide d'un test par cytométrie en flux basé sur des colorants, ils ont montré que les deux molécules augmentaient fortement la fraction de cellules en phases précoces et tardives d'apoptose dans les lignées de cancer du sein et du côlon. Les niveaux de protéines clés liées à cette voie ont évolué de façon coordonnée : les signaux pro‑mort ont augmenté, les protéines protectrices ont diminué et les enzymes appelées caspases se sont activées, des schémas cohérents avec une voie mitochondriale de l'apoptose.
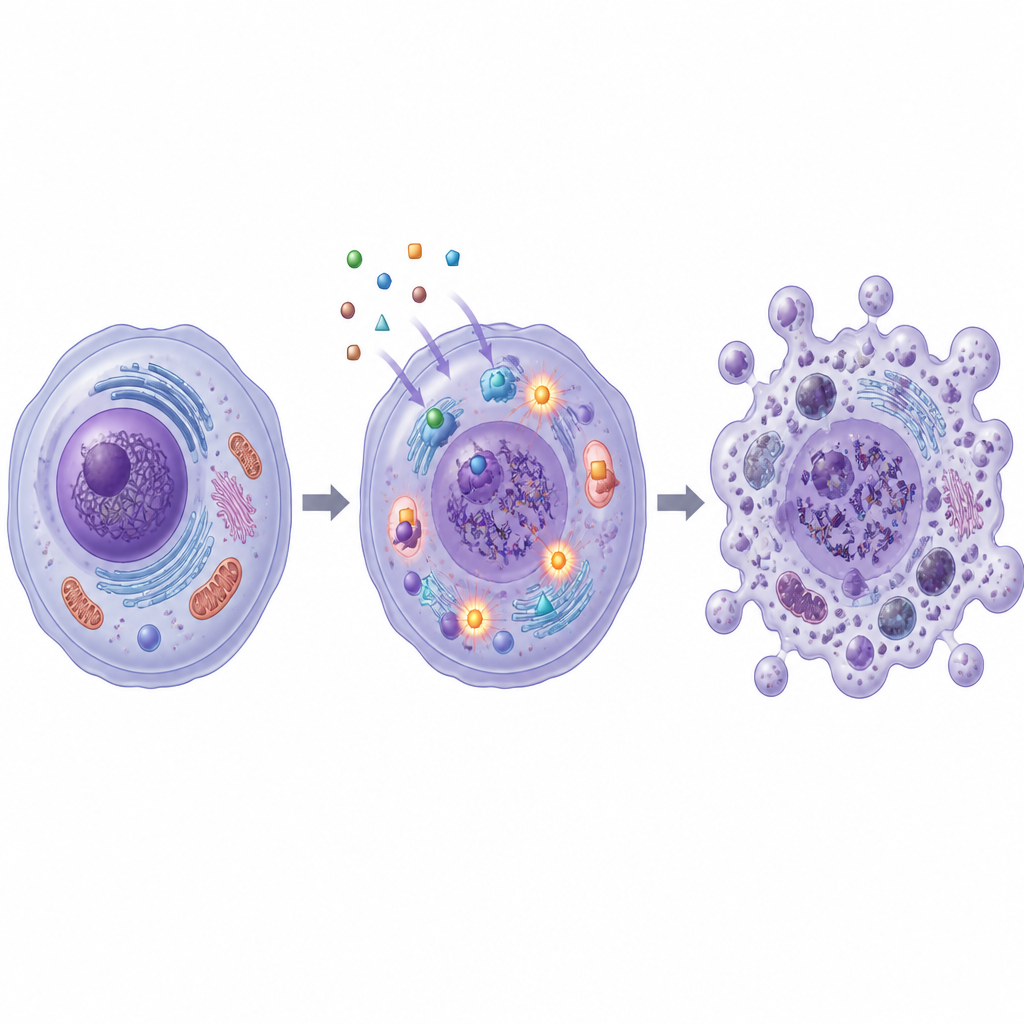
Stress sur l'ADN et enzymes vitales
L'étude a aussi sondé comment ces molécules endommagent les cellules cancéreuses de l'intérieur. SB1 et SB2 ont augmenté la production d'espèces réactives de l'oxygène, des molécules instables qui peuvent détériorer les structures cellulaires et l'ADN. Un test colorimétrique des fragments d'ADN a montré que les cellules cancéreuses traitées présentaient beaucoup plus de matériel génétique fragmenté, surtout avec SB2. Parallèlement, les deux composés ont réduit l'activité d'enzymes appelées topoisomérases I et II, qui gèrent l'enroulement et le déroulement de l'ADN lors de la réplication et de la réparation. Des simulations informatiques ont corroboré ces résultats expérimentaux, indiquant que SB1 et SB2 peuvent s'insérer de manière ajustée dans les poches de liaison de la topoisomérase II et d'une autre protéine liée au cancer, l'anhydrase carbonique XII.
Le rôle d'un seul atome
Bien que SB1 et SB2 ne diffèrent que par la présence d'un seul atome de brome sur SB2, cette petite modification chimique a eu un impact net. Dans la plupart des tests, SB2 a montré une capacité plus forte à arrêter la croissance des cellules cancéreuses, augmenter le stress oxydatif, fragmenter l'ADN et bloquer l'activité des topoisomérases. L'atome de brome supplémentaire modifie probablement la façon dont la molécule interagit avec les membranes cellulaires et les cibles protéiques, améliorant son entrée dans les cellules et son ancrage sur des sites critiques. Ceci illustre comment des changements subtils dans la conception moléculaire peuvent profondément remodeler le comportement biologique.
Quelles perspectives
Dans l'ensemble, les résultats suggèrent que ces bases de Schiff à base de sulfadiazine, et en particulier SB2, peuvent pousser les cellules cancéreuses vers une voie de destruction contrôlée tout en étant moins nocives pour les cellules normales en culture. Elles semblent agir par une combinaison d'augmentation du stress oxydatif, de dommage à l'ADN et de blocage d'enzymes dont les cellules cancéreuses dépendent pour croître et se diviser. Bien que ces composés ne soient pas prêts à être utilisés comme médicaments, ils fournissent des points de départ prometteurs, ou molécules mères, que les chimistes pourront affiner pour concevoir de futurs agents anticancéreux dotés d'une meilleure stabilité et d'un meilleur profil de sécurité.
Citation: Nasr, E., Moustafa, A.H., El-Sayed, A.S.A. et al. Synthesis, characterization, and anticancer potency of sulfadiazine salicylaldehyde-based Schiff bases. Sci Rep 16, 15047 (2026). https://doi.org/10.1038/s41598-026-51752-z
Mots-clés: Bases de Schiff, composés anticancéreux, apoptose, espèces réactives de l'oxygène, inhibition de la topoisomérase