Clear Sky Science · zh
内源性蛋白标记结合CRISPR筛选方法鉴定UBE3C为潜在的MYC致癌基因调节因子
这项研究为何重要
癌症医生长期以来知道,一个名为MYC的强大“主开关”蛋白有助于肿瘤细胞生长、分裂并抵抗治疗。在产生抗体的血细胞癌——多发性骨髓瘤中,MYC常常处于“开启”状态。但直接阻断MYC在技术上非常困难。这项研究采取了不同路径:研究者没有直接针对MYC本身下药,而是系统性地搜索控制骨髓瘤细胞产生多少MYC的其他基因。他们的工作揭示了新的分子调控杠杆——特别是名为UBE3C的蛋白——这些可能比直接针对MYC更容易成为未来治疗的靶点。
将MYC变成一个活体荧光传感器
为了在不扰动细胞正常调控的情况下观察癌细胞中的MYC,研究团队工程化了一种多发性骨髓瘤细胞系,使其内源性MYC蛋白带有内建的绿色荧光标签。在这些细胞中,绿色信号越亮,MYC含量越多。因为标签与细胞的天然MYC融合,其活性和调控尽可能接近真实疾病生物学。作者仔细验证了这个荧光MYC仍然像原始蛋白一样表现:它对已知的降低MYC的药物有反应,可通过基因编辑工具切除MYC基因而被降低,并继续与其在细胞核中的常见结合伙伴相互作用。这个经验证的细胞系成为他们大规模筛选的基础。
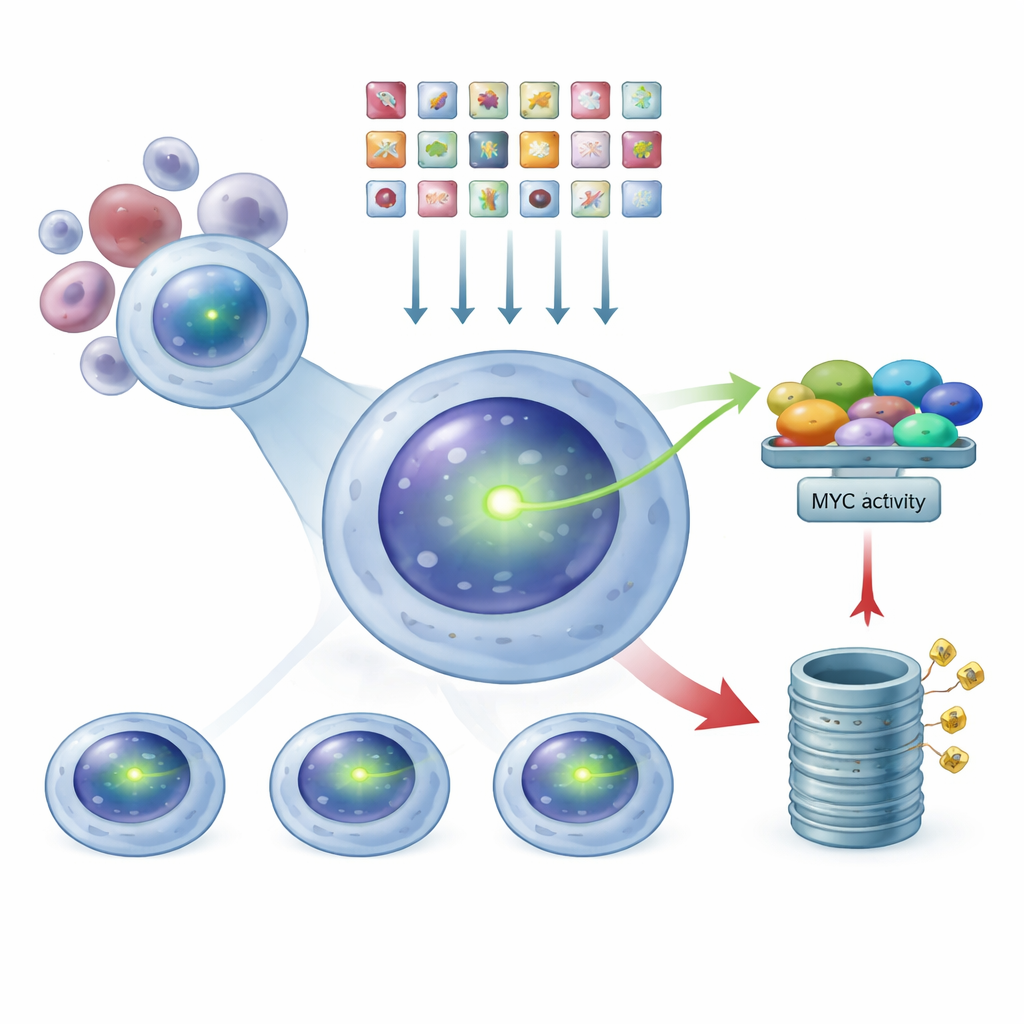
将CRISPR用作全基因组的亮度调节器
借助这一发光报告系统,研究者将CRISPR技术用作一种全基因组的亮度调节器。他们将包含数万条向导RNA的文库导入带有MYC标签的骨髓瘤细胞中,每条向导RNA设计用于敲除一个人类基因。每个细胞平均仅接受一个基因“打击”。在给予编辑生效的时间后,他们使用细胞分选仪根据绿色亮度将细胞群体分为三组:MYC低、 中等和高。通过测序每组中富集的向导RNA,他们可以反推哪些被敲除的基因导致MYC水平下降或上升。
两个主要控制枢纽:转录和蛋白质处置
该筛选显示出两类主要的MYC调节因子。当一个称为Mediator的巨大分子复合体的组成部分被破坏时,MYC水平下降,将这些因子归入“激活子”阵营——它们通常帮助细胞开启MYC基因。相反,当细胞的蛋白质“粉碎”机器——蛋白酶体的部分或负责附加或去除小型降解标签的酶丢失时,MYC水平上升。这表明MYC通常不仅靠调控合成量来控制,也通过主动降解被维持在合适水平。已知的参与者如增强MYC的IRF4和促进其降解的FBXW7都出现在预期的位置,这增加了筛选结果反映真实生物学而非噪声的信心。
聚焦UBE3C作为特定的MYC制动器
在众多候选基因中,UBE3C格外突出:它是一种帮助标记蛋白以便降解并与蛋白酶体短暂结合的酶。敲除UBE3C在报告细胞中引起了显著的MYC水平上升,远强于相关酶UBE3A和UBE3B,后者几乎没有影响。作者随后在未修饰的多发性骨髓瘤细胞系中检验,发现禁用UBE3C同样提高了天然未标记的MYC蛋白水平。这表明UBE3C是在骨髓瘤细胞中对MYC进行负向调控的特别重要因子。与此同时,研究表明MYC的丰度受转录机器推动其基因表达的力度与蛋白被标记并送入细胞“回收箱”这一主动降解过程共同塑造。
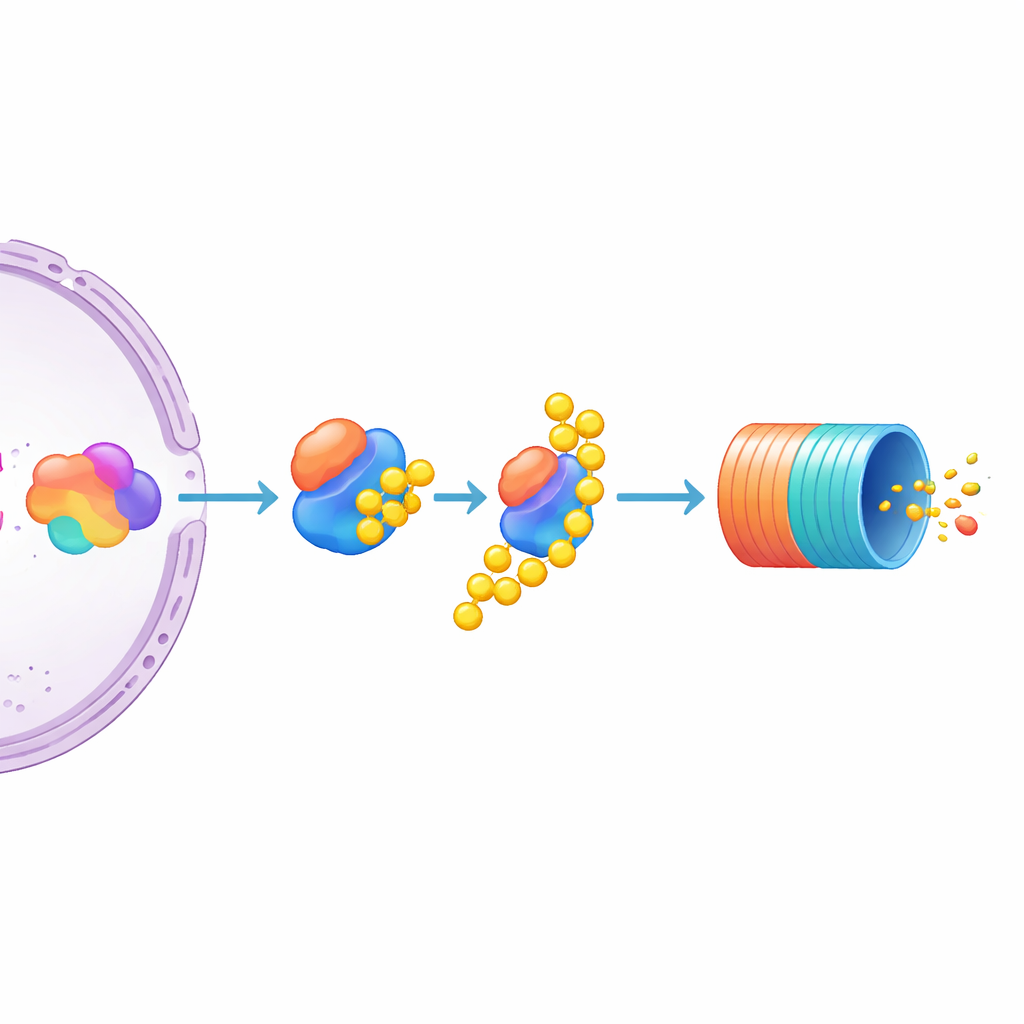
这对未来癌症治疗意味着什么
对非专业读者来说,关键结论是:MYC本身可能依然是一个难以直接下药的目标,但控制它的网络正变得更加清晰。通过将MYC转换为荧光报告器并将其与全基因组CRISPR筛选结合,作者绘制出一张强有力的基因图谱,显示哪些基因会在多发性骨髓瘤细胞内将MYC上调或下调。他们的数据突出显示了Mediator组分作为驱动MYC产生的引擎的一部分,更引人注目的是,鉴定出UBE3C作为帮助防止MYC蛋白积累的可能开关。从长远看,调节像UBE3C这样的调控因子或MYC产生与处置过程中的其他步骤的药物,可能提供更精确的方式来抑制这一主开关,从而减缓MYC驱动的癌症,而无需直接针对MYC本体。
引用: Seibert, M., Kurrle, N., Kaleab, S. et al. Endogenous protein tagging coupled with a CRISPR screening approach identifies UBE3C as a potential MYC oncogene regulator. Sci Rep 16, 12194 (2026). https://doi.org/10.1038/s41598-026-47974-w
关键词: MYC 调控, 多发性骨髓瘤, CRISPR 筛选, 泛素蛋白酶体, UBE3C