Clear Sky Science · pl
Endogenne znakowanie białek w połączeniu z podejściem przesiewowym CRISPR identyfikują UBE3C jako potencjalnego regulatora onkogenu MYC
Dlaczego to badanie jest istotne
Onkolodzy od dawna wiedzą, że potężne „główne wyłącznik” białko o nazwie MYC pomaga komórkom nowotworowym rosnąć, dzielić się i opierać leczeniu. W szpiczaku mnogim, nowotworze komórek produkujących przeciwciała, MYC często pozostaje w pozycji „włączonej”. Jednak bezpośrednie blokowanie MYC okazało się technicznie trudne. To badanie idzie inną drogą: zamiast próbować leczyć sam MYC, badacze systematycznie przeszukali inne geny, które kontrolują, ile MYC produkuje komórka szpiczakowa. Ich praca ujawnia nowe molekularne dźwignie — w szczególności białko UBE3C — które mogą być łatwiejsze do celu dla przyszłych terapii.
Przekształcenie MYC w żywy czujnik światła
Aby obserwować MYC w komórkach nowotworowych bez zaburzania ich naturalnych powiązań, zespół zmodyfikował linię komórkową szpiczaka mnogiego tak, by jej własne białko MYC nosiło wbudowany zielony znacznik fluorescencyjny. W tych komórkach im jaśniejszy zielony sygnał, tym więcej MYC jest obecne. Ponieważ znacznik jest złączony z naturalnym MYC komórki, jego aktywność i regulacja pozostają jak najbliżej biologii choroby. Autorzy dokładnie sprawdzili, że ten fluorescencyjny MYC nadal zachowuje się jak oryginalne białko: reaguje na znany lek obniżający poziom MYC, można go zmniejszyć przycinając gen MYC narzędziami edycji genów, i nadal wchodzi w interakcję ze swoim zwykłym partnerem wiążącym w jądrze. Ta zwalidowana linia komórkowa stała się podstawą ich szeroko zakrojonego badania.
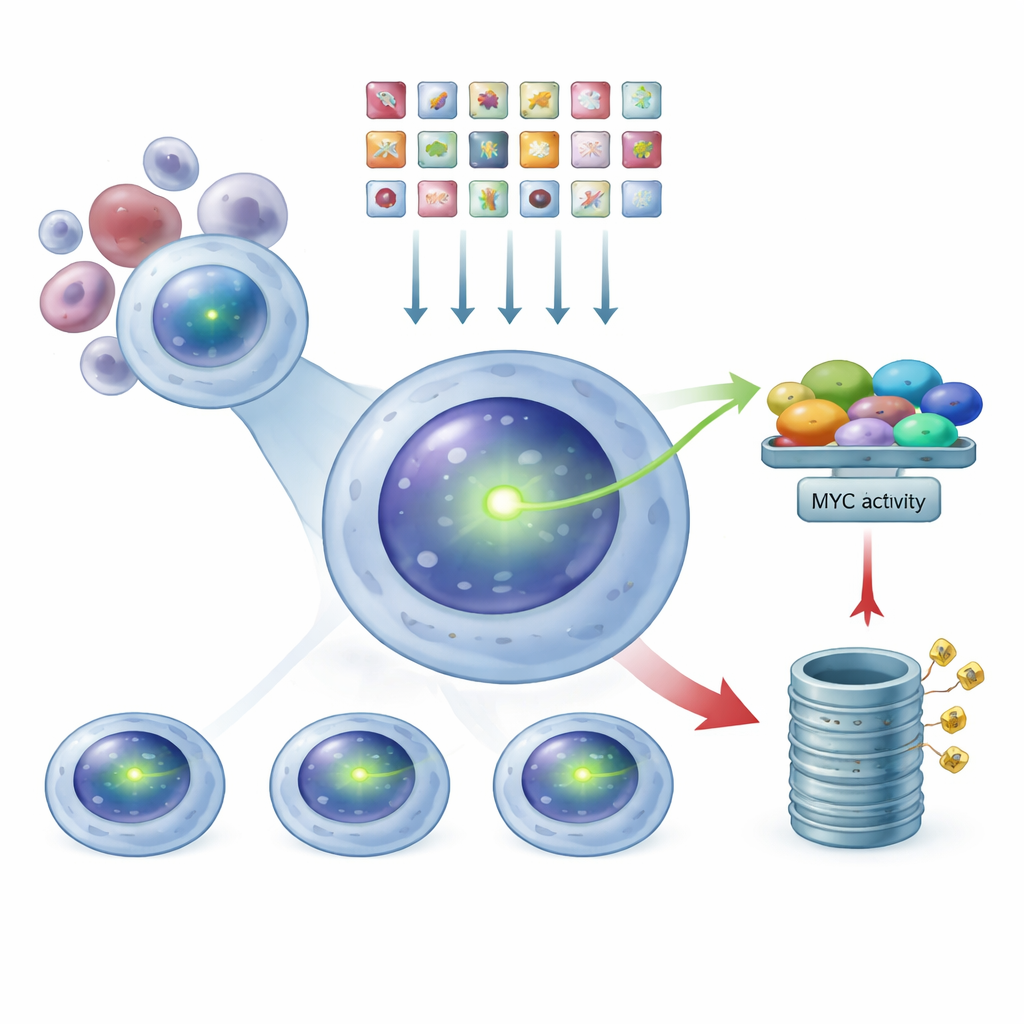
Wykorzystanie CRISPR jako ogólnogenomowego ściemniacza
Wyposażeni w ten świecący system reporterowy, badacze użyli technologii CRISPR jako rodzaju ogólnogenomowego ściemniacza. Wprowadzili bibliotekę dziesiątek tysięcy RNA przewodników, z których każdy zaprojektowano do wyłączenia jednego ludzkiego genu, do komórek szpiczakowych z znakowanym MYC. Każda komórka otrzymała średnio tylko jedno uderzenie genetyczne. Po odczekaniu czasu na zajście tych edycji użyli sortera komórek, aby rozdzielić populację na trzy grupy w oparciu o jasność zieleni: niskie, pośrednie i wysokie poziomy MYC. Sekwencjonując, które RNA przewodniki były wzbogacone w każdej grupie, mogli odtworzyć, które wyłączone geny powodowały spadek lub wzrost poziomów MYC.
Dwa główne centra kontroli: transkrypcja i utylizacja białek
Wzorzec wyłaniający się z tego przesiewu ujawnił dwa główne klasy regulatorów MYC. Gdy zaburzono składniki dużego zespołu molekularnego zwanego kompleksem Mediator, poziomy MYC spadały, plasując te czynniki w obozie „aktywatorów” — normalnie pomagają one w włączaniu genu MYC. W przeciwieństwie do tego, gdy utracono części maszyny rozdrabniającej białka komórki, proteasomu, lub enzymy przyłączające bądź usuwające małe znaczniki degradacji, poziomy MYC rosły. To wskazuje, że MYC jest zwykle kontrolowany przez aktywny rozkład, a nie tylko przez to, ile jest wytwarzane. Znane graczy, takich jak IRF4, które zwiększa MYC, oraz FBXW7, które sprzyja jego zniszczeniu, pojawiły się dokładnie tam, gdzie należało się ich spodziewać, co daje pewność, że przesiew wykrywa prawdziwą biologię, a nie szum.
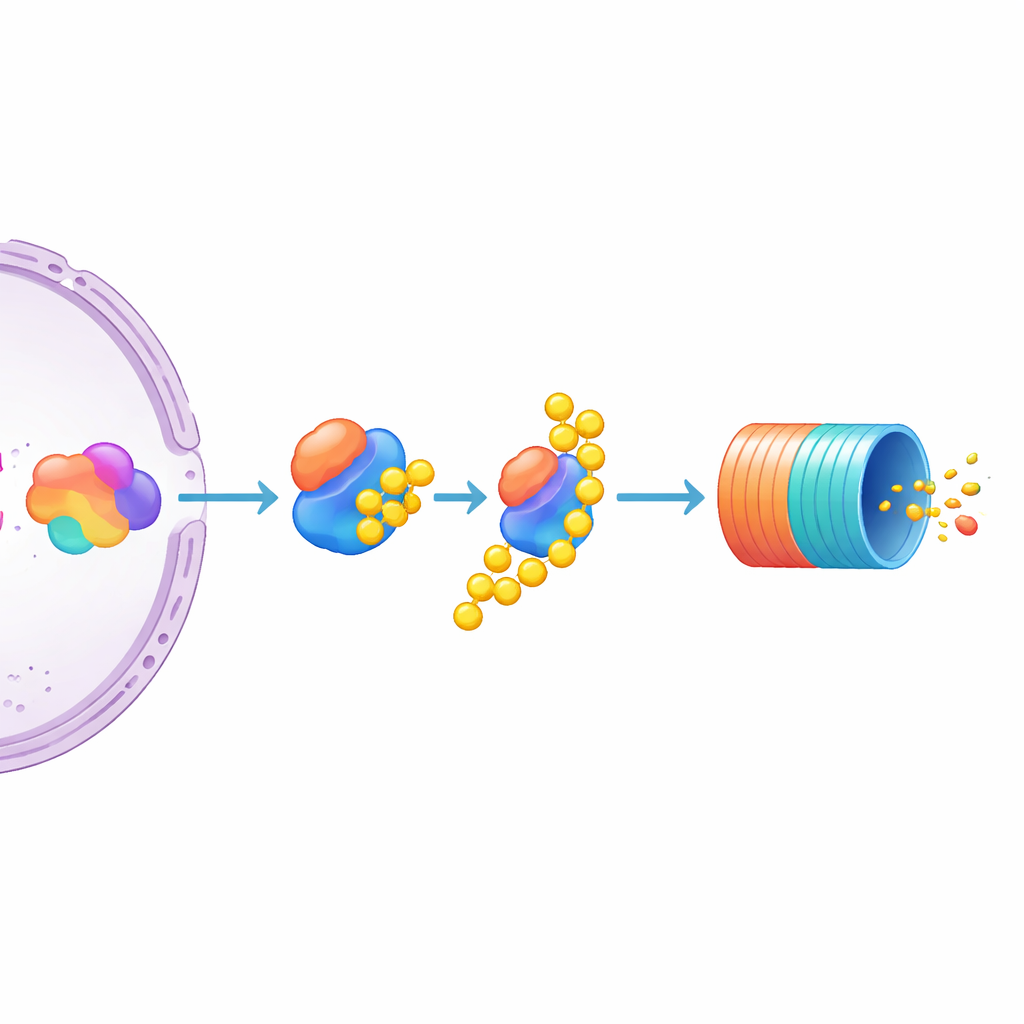
Zbliżenie na UBE3C jako konkretny hamulec MYC
Wśród wielu kandydatów jeden wyróżniał się szczególnie: UBE3C, enzym pomagający oznaczać białka do zniszczenia i przejściowo wiążący się z proteasomem. Wyłączenie UBE3C spowodowało uderzający wzrost poziomów MYC w komórkach reporterowych, znacznie silniejszy niż w przypadku pokrewnych enzymów UBE3A i UBE3B, które miały niewielki efekt. Autorzy następnie przetestowali niemodyfikowane linie komórkowe szpiczaka mnogiego i stwierdzili, że unieruchomienie UBE3C tam także podniosło natywne, nienaznaczone białko MYC. To wskazuje, że UBE3C jest szczególnie istotnym negatywnym regulatorem MYC w komórkach szpiczakowych. Jednocześnie badanie sugeruje, że obfitość MYC kształtowana jest wspólnie przez to, jak mocno maszyny transkrypcyjne napędzają jego gen oraz jak aktywnie białko jest znakowane i kierowane do komórkowego „kosza na recykling”.
Co to oznacza dla przyszłych terapii przeciwnowotworowych
Dla osób niebędących specjalistami kluczowy wniosek jest taki, że sam MYC może pozostać trudnym celem lekowym, ale sieć, która go kontroluje, staje się coraz jaśniejsza. Przekształcając MYC w reporter fluorescencyjny i łącząc go z ogólnogenomowym przesiewem CRISPR, autorzy stworzyli potężną mapę genów, które w komórkach szpiczaka mnogiego albo zwiększają, albo zmniejszają MYC. Ich dane podkreślają składniki kompleksu Mediator jako część silnika napędzającego produkcję MYC i, co bardziej uderzające, identyfikują UBE3C jako prawdopodobny przełącznik pomagający zapobiegać nagromadzeniu białka MYC. W dłuższej perspektywie leki modulujące regulatorów takich jak UBE3C — lub inne etapy produkcji i utylizacji MYC — mogłyby oferować bardziej precyzyjne sposoby przyciszenia tego głównego wyłącznika i spowolnienia nowotworów napędzanych przez MYC, bez konieczności bezpośredniego atakowania samego MYC.
Cytowanie: Seibert, M., Kurrle, N., Kaleab, S. et al. Endogenous protein tagging coupled with a CRISPR screening approach identifies UBE3C as a potential MYC oncogene regulator. Sci Rep 16, 12194 (2026). https://doi.org/10.1038/s41598-026-47974-w
Słowa kluczowe: Regulacja MYC, szpiczak mnogi, przesiew CRISPR, ubikwitynowo‑proteasomowy, UBE3C