Clear Sky Science · nl
Endogeen eiwit-tagging gecombineerd met een CRISPR‑screeningbenadering identificeert UBE3C als potentiële regulator van het oncogen MYC
Waarom deze studie ertoe doet
Kankerdocenten weten al langer dat een krachtige "master switch"‑eiwit genaamd MYC tumorcellen helpt groeien, delen en therapieresistent te worden. Bij multipel myeloom, een kanker van antilichaamproducerende bloedcellen, staat MYC vaak permanent in de "aan"‑stand. Directe remming van MYC blijkt technisch moeilijk. Deze studie kiest een andere benadering: in plaats van te proberen MYC zelf te remmen, zochten de onderzoekers systematisch naar andere genen die bepalen hoeveel MYC een myeloomcel aanmaakt. Hun werk onthult nieuwe moleculaire knoppen — in het bijzonder een eiwit genaamd UBE3C — die mogelijk eenvoudiger met toekomstige therapieën zijn te richten.
MYC veranderen in een levende lichtsensor
Om MYC in kankercellen te volgen zonder hun normale regeling te verstoren, bouwde het team een multipel‑myeloom‑cellijn zo om dat het eigen MYC‑eiwit een ingebouwde groene fluorescente tag draagt. In deze cellen geldt: hoe feller het groene signaal, hoe meer MYC aanwezig is. Omdat de tag is gefuseerd aan het natuurlijke MYC van de cel, blijven activiteit en regulatie zoveel mogelijk gelijk aan de echte ziektebiologie. De auteurs controleerden zorgvuldig dat dit fluorescente MYC zich nog als het oorspronkelijke eiwit gedraagt: het reageert op een bekend MYC‑verlagend medicijn, kan worden verminderd door het MYC‑gen met genbewerkingsmiddelen te knippen, en blijft interacteren met zijn gebruikelijke bindingspartner in de kern. Deze gevalideerde cellijn werd de basis voor hun grootschalige zoektocht.
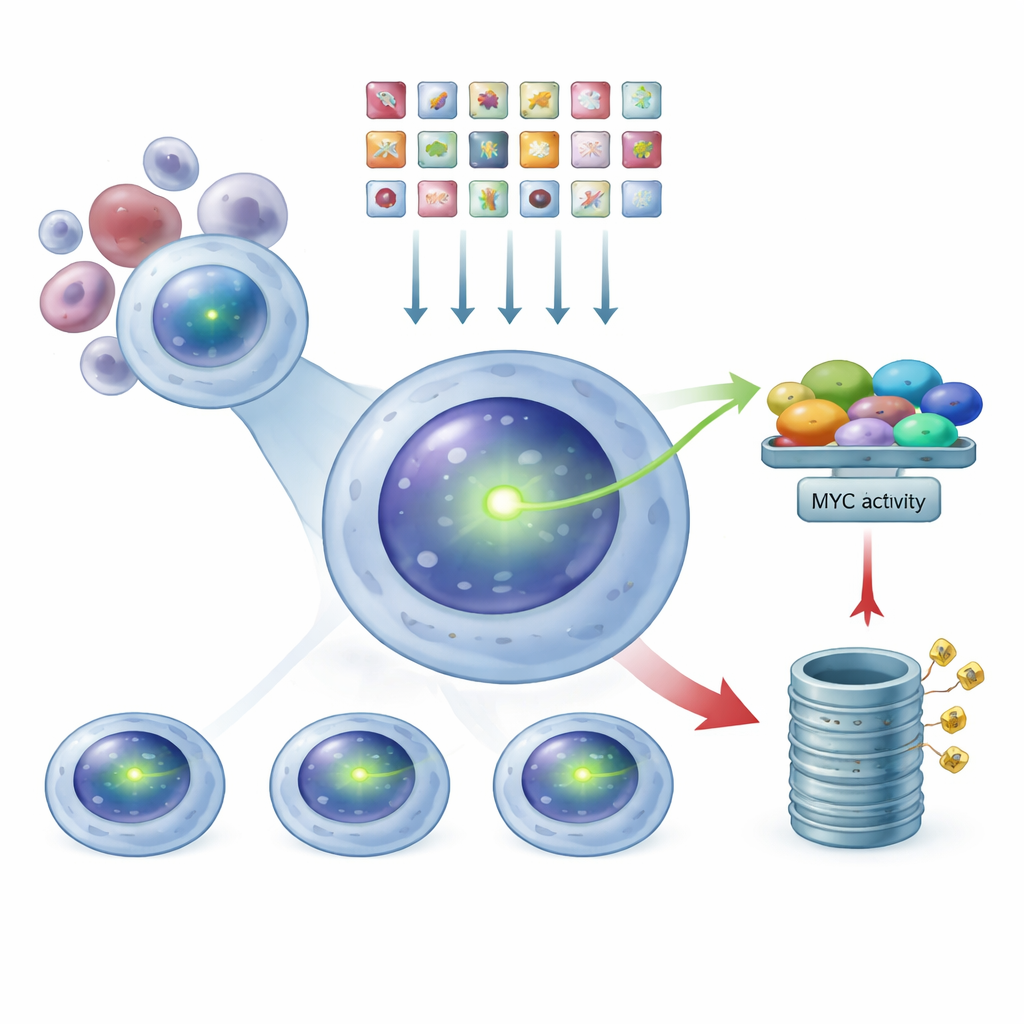
CRISPR gebruiken als een genoom‑wijd dimmer‑schakelaar
Met dit lichtgevende reportsysteem zetten de onderzoekers CRISPR‑technologie in als een soort genoom‑brede dimmer. Ze brachten een bibliotheek van tienduizenden gids‑RNA’s in, elk ontworpen om één menselijk gen uit te schakelen, in de MYC‑getagde myeloomcellen. Elke cel kreeg gemiddeld slechts één genetische treffer. Nadat er tijd was gegeven voor deze bewerkingen om effect te krijgen, gebruikten ze een celsorteermachine om de populatie op basis van groene helderheid in drie groepen te scheiden: MYC‑laag, intermediair en MYC‑hoog. Door te sequencen welke gids‑RNA’s in elke groep verrijkt waren, konden ze terugredeneren welke uitgeschakelde genen ervoor zorgden dat MYC‑niveaus daalden of stegen.
Twee hoofdregiecentra: transcriptie en eiwitafbraak
Het patroon dat uit dit screen naar voren kwam, onthulde twee grote klassen van MYC‑regulatoren. Wanneer componenten van een groot moleculair complex genaamd het Mediator‑complex werden verstoord, daalden de MYC‑niveaus, waarmee deze factoren in de categorie "activator" vallen — zij helpen normaal gesproken de aanzet van het MYC‑gen. Daarentegen, wanneer delen van de eiwitversnellende machinerie van de cel, het proteasoom, of enzymen die kleine afbraaksignalen aanbrengen of verwijderen, verloren gingen, stegen de MYC‑niveaus. Dit duidt erop dat MYC normaal gesproken onder controle wordt gehouden door actieve afbraak, niet alleen door te reguleren hoeveel wordt gemaakt. Bekende spelers zoals IRF4, dat MYC versterkt, en FBXW7, dat diens afbraak bevordert, kwamen precies op de verwachte plaatsen naar voren, wat vertrouwen geeft dat het screen echte biologische signalen en geen ruis vastlegde.
Inzoomen op UBE3C als specifieke MYC‑rem
Onder de vele kandidaten stak er één uit: UBE3C, een enzym dat helpt eiwitten te labelen voor afbraak en tijdelijk met het proteasoom associeert. Het uitschakelen van UBE3C veroorzaakte een opvallende stijging van MYC‑niveaus in de reporterscellen, veel sterker dan verwante enzymen UBE3A en UBE3B, die weinig effect hadden. De auteurs testten daarna ongewijzigde multipel‑myeloom‑cellijnen en vonden dat het uitschakelen van UBE3C daar ook het native, niet‑getagde MYC‑eiwit verhoogde. Dit wijst erop dat UBE3C een bijzonder belangrijke negatieve regulator van MYC is in myeloomcellen. Tegelijk suggereert de studie dat de hoeveelheid MYC wordt bepaald door zowel de kracht waarmee het transcriptiemachinerie het gen aandrijft als door hoe actief het eiwit wordt gemarkeerd en naar het cellulaire "recycling‑station" wordt gevoerd.
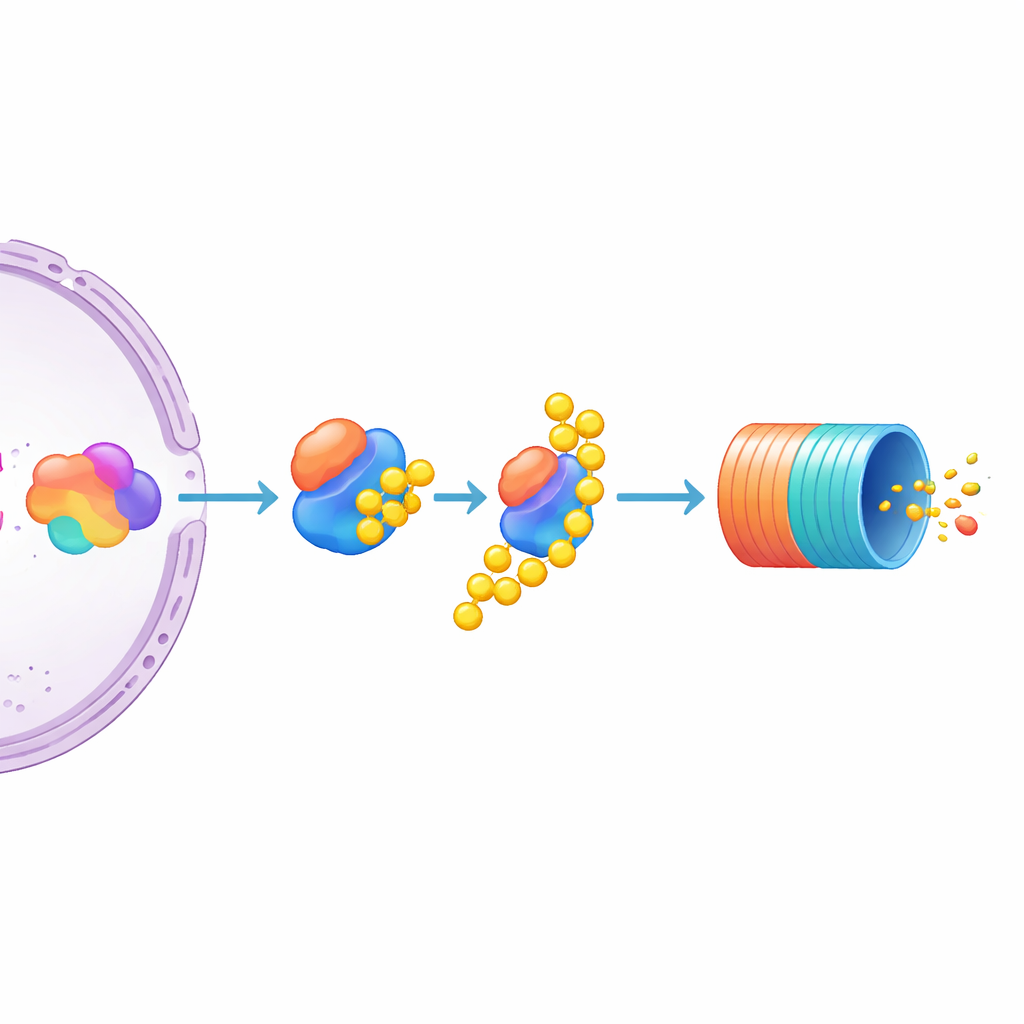
Wat dit betekent voor toekomstige kankerbehandelingen
Voor niet‑specialisten is de belangrijkste conclusie dat MYC zelf wellicht een lastige medicijnendoelwit blijft, maar dat het netwerk dat het reguleert duidelijker wordt. Door MYC om te zetten in een fluorescerende reporter en dit te combineren met een genoom‑wijd CRISPR‑screen, bouwden de auteurs een krachtig overzicht van genen die MYC in multipel‑myeloomcellen omhoog of omlaag brengen. Hun gegevens benadrukken Mediator‑componenten als deel van het mechanisme dat MYC‑productie aandrijft en identificeren, opvallender nog, UBE3C als een waarschijnlijke schakel die voorkomt dat MYC‑eiwit zich ophoopt. Op de lange termijn zouden geneesmiddelen die regulatoren zoals UBE3C moduleren — of andere stappen in MYC’s productie en afbraak — meer precieze manieren kunnen bieden om deze master switch te dempen en MYC‑gedreven kankers af te remmen zonder direct MYC te moeten raken.
Bronvermelding: Seibert, M., Kurrle, N., Kaleab, S. et al. Endogenous protein tagging coupled with a CRISPR screening approach identifies UBE3C as a potential MYC oncogene regulator. Sci Rep 16, 12194 (2026). https://doi.org/10.1038/s41598-026-47974-w
Trefwoorden: MYC‑regulatie, multipel myeloom, CRISPR‑screen, ubiquitine‑proteasoom, UBE3C