Clear Sky Science · it
Tagging endogeno delle proteine accoppiato a uno screening CRISPR identifica UBE3C come potenziale regolatore oncogenico di MYC
Perché questo studio è importante
I clinici oncologi sanno da tempo che una potente proteina “interruttore maestro” chiamata MYC aiuta le cellule tumorali a crescere, dividersi e resistere ai trattamenti. Nel mieloma multiplo, un tumore delle cellule produttrici di anticorpi, MYC è spesso bloccata nella posizione “accesa”. Ma bloccare direttamente MYC si è rivelato tecnicamente difficile. Questo studio adotta un approccio diverso: invece di cercare di colpire MYC in modo diretto, i ricercatori hanno cercato sistematicamente altri geni che controllano quanto MYC produce una cellula di mieloma. Il loro lavoro rivela nuove leve molecolari — in particolare una proteina chiamata UBE3C — che potrebbero essere più semplici da modulare con future terapie.
Trasformare MYC in un sensore luminoso vivente
Per osservare MYC all’interno delle cellule tumorali senza alterarne il circuito naturale, il gruppo ha modificato una linea cellulare di mieloma multiplo in modo che la sua proteina MYC portasse un’etichetta fluorescente verde integrata. In queste cellule, più il segnale verde è intenso, maggiore è la quantità di MYC presente. Poiché l’etichetta è fusa alla MYC naturale della cellula, la sua attività e il suo controllo rimangono il più possibile fedeli alla biologia della malattia reale. Gli autori hanno verificato con cura che questa MYC fluorescente si comporta ancora come la proteina originale: risponde a un farmaco noto per ridurre MYC, può essere abbassata tagliando il gene MYC con strumenti di editing genetico e continua a interagire con il suo consueto partner di legame nel nucleo. Questa linea cellulare convalidata è diventata la base della loro ricerca su larga scala.
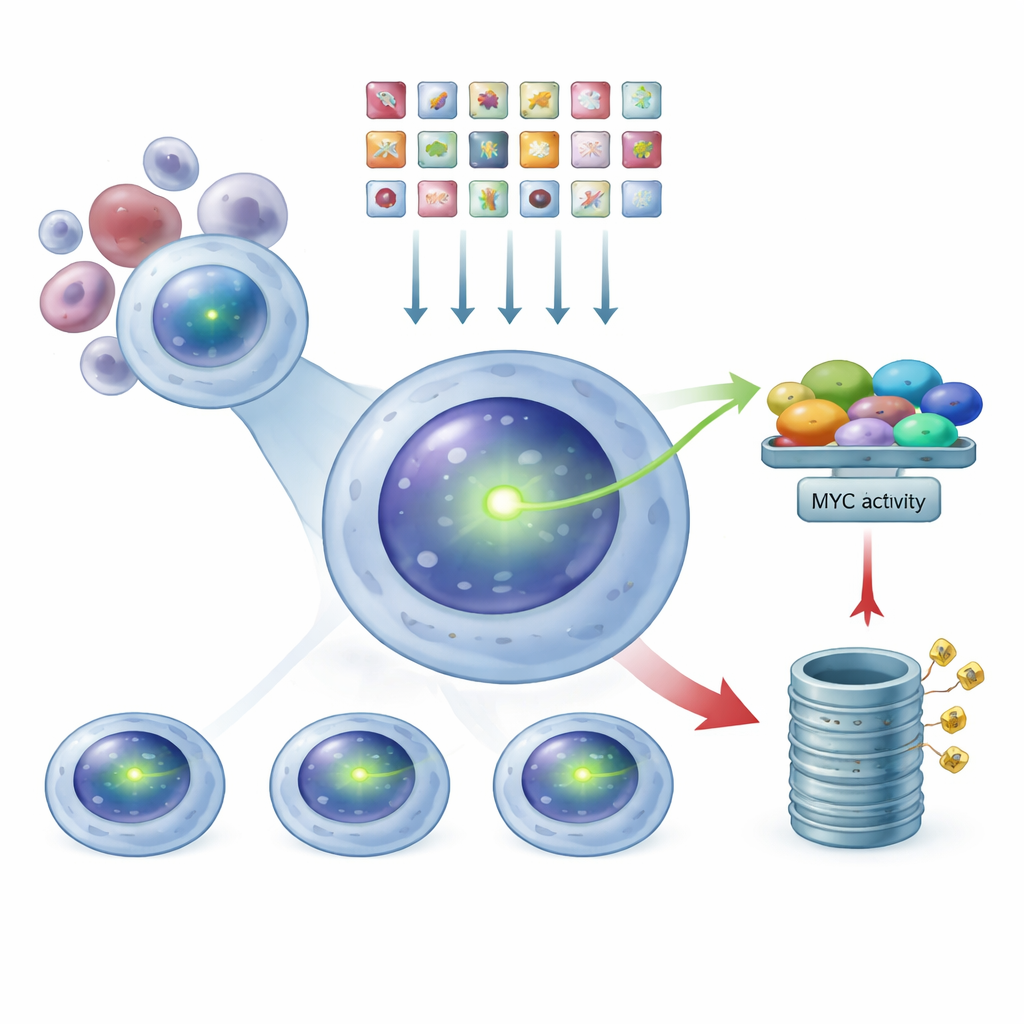
Usare CRISPR come un dimmer genomico
Dotati di questo sistema reporter luminoso, i ricercatori hanno usato la tecnologia CRISPR come una sorta di dimmer genomico. Hanno introdotto una libreria di decine di migliaia di guide RNA, ciascuna progettata per inattivare un gene umano, nelle cellule di mieloma con MYC taggata. Ogni cellula ha ricevuto, in media, un solo colpo genetico. Dopo aver dato il tempo agli effetti di manifestarsi, hanno separato la popolazione in tre gruppi in base all’intensità del verde tramite un dispositivo di separazione cellulare: MYC‑bassa, intermedia e MYC‑alta. Sequenziando quali guide erano arricchite in ciascun gruppo, hanno potuto risalire ai geni la cui inattivazione faceva scendere o salire i livelli di MYC.
Due hub di controllo principali: trascrizione e smaltimento delle proteine
Il quadro emerso dallo screening ha rivelato due grandi classi di regolatori di MYC. Quando componenti di un ampio complesso molecolare chiamato Mediator venivano disturbati, i livelli di MYC diminuivano, collocando questi fattori nel campo degli “attivatori” — in condizioni normali aiutano le cellule ad accendere il gene MYC. Al contrario, quando venivano persi elementi della macchina cellulare che smonta le proteine, il proteasoma, o enzimi che aggiungono o rimuovono piccoli tag di degradazione, i livelli di MYC aumentavano. Questo indica che MYC è normalmente controllata non solo da quanto viene prodotta, ma anche da un processo attivo di distruzione. Attori già noti come IRF4, che potenzia MYC, e FBXW7, che ne promuove la distruzione, sono ricomparsi esattamente dove atteso, dando fiducia che lo screening stesse catturando biologia reale e non rumore.
Focalizzarsi su UBE3C come freno specifico di MYC
Tra i molti candidati, uno ha spiccato: UBE3C, un enzima che aiuta a etichettare le proteine per la distruzione e che si associa in modo transitorio al proteasoma. L’inattivazione di UBE3C ha causato un marcato aumento dei livelli di MYC nelle cellule reporter, molto più pronunciato rispetto agli enzimi correlati UBE3A e UBE3B, che avevano scarso effetto. Gli autori hanno poi testato linee di mieloma multiplo non modificate e hanno trovato che disabilitare UBE3C lì aumentava anche la MYC nativa, non taggata. Ciò indica che UBE3C è un regolatore negativo particolarmente importante di MYC nelle cellule di mieloma. Contemporaneamente, lo studio suggerisce che l’abbondanza di MYC è modellata congiuntamente da quanto forte sia la spinta trascrizionale sul suo gene e da quanto attivamente la proteina venga etichettata e indirizzata al “bidone del riciclo” cellulare.
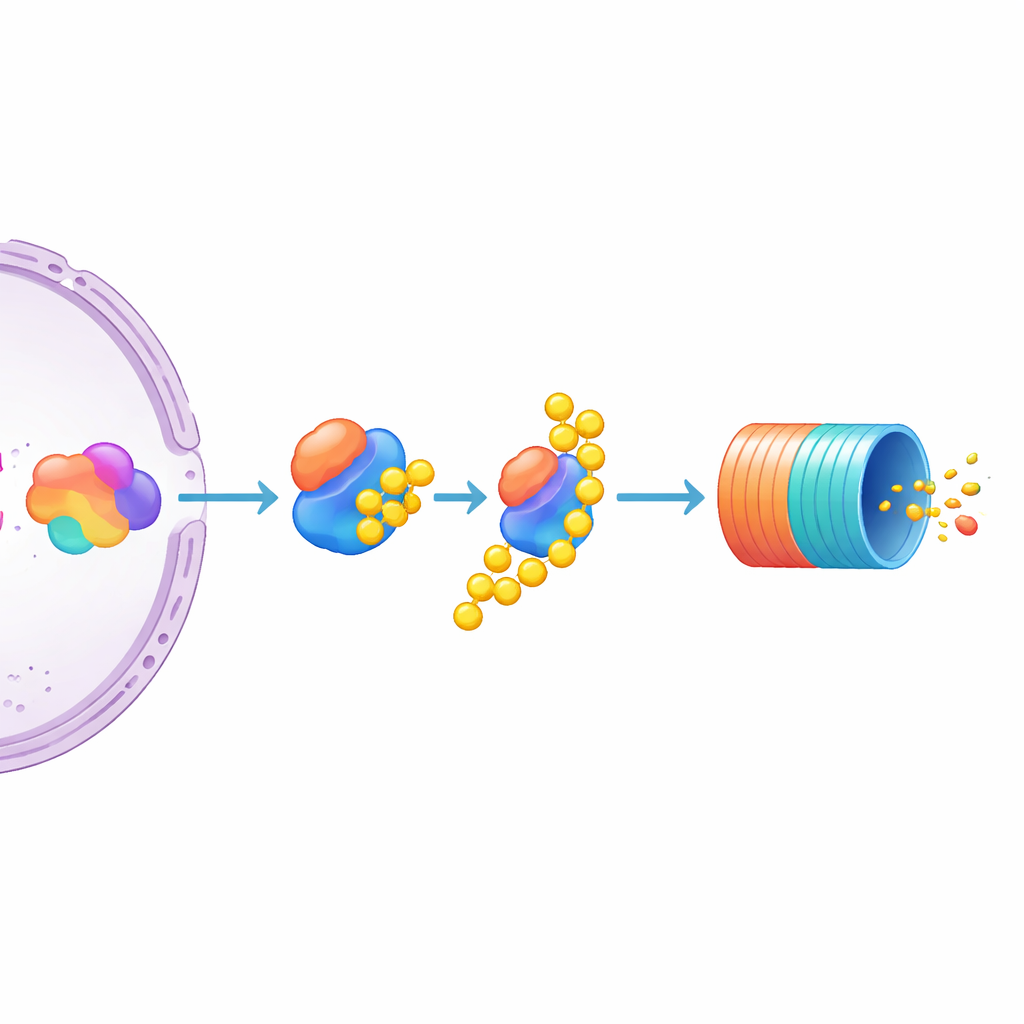
Cosa significa questo per i futuri trattamenti contro il cancro
Per i non specialisti, il punto chiave è che MYC stessa può rimanere un bersaglio farmacologico scivoloso, ma la rete che la controlla sta diventando più chiara. Convertendo MYC in un reporter fluorescente e abbinandolo a una ricerca CRISPR su tutto il genoma, gli autori hanno costruito una mappa potente di geni che accendono o spengono MYC all’interno delle cellule di mieloma multiplo. I loro dati evidenziano i componenti del Mediator come parte del motore che guida la produzione di MYC e, in modo più significativo, identificano UBE3C come un possibile interruttore che aiuta a impedire l’accumulo della proteina MYC. A lungo termine, farmaci che modulano regolatori come UBE3C — o altri passaggi nella produzione e nello smaltimento di MYC — potrebbero offrire modi più precisi per ammansire questo interruttore maestro e rallentare i tumori guidati da MYC senza dover colpire MYC direttamente.
Citazione: Seibert, M., Kurrle, N., Kaleab, S. et al. Endogenous protein tagging coupled with a CRISPR screening approach identifies UBE3C as a potential MYC oncogene regulator. Sci Rep 16, 12194 (2026). https://doi.org/10.1038/s41598-026-47974-w
Parole chiave: Regolazione di MYC, Mieloma multiplo, Screening CRISPR, Ubiquitina proteasoma, UBE3C