Clear Sky Science · ja
内因性タンパク質タグ付けとCRISPRスクリーニング法の併用によりUBE3CがMYCオンコジーンの潜在的制御因子として同定される
この研究が重要な理由
がん医療では、MYCと呼ばれる強力な“マスタースイッチ”タンパク質が腫瘍細胞の増殖、分裂、治療抵抗性に寄与することが長く知られています。抗体産生血球のがんである多発性骨髄腫では、MYCがしばしば“オン”の状態に固定されています。しかし、直接MYCを阻害することは技術的に困難でした。本研究は別のアプローチを取ります:MYC自体を薬で抑えるのではなく、骨髄腫細胞がどれだけのMYCを作るかを制御する他の遺伝子を体系的に探索したのです。その作業により、将来の治療で標的にしやすい可能性のある分子調節因子、特にUBE3Cというタンパク質が明らかになりました。
MYCを生きた光センサーに変える
正常な細胞機構を乱さずにがん細胞内のMYCを観察するため、研究チームは多発性骨髄腫の細胞株を改変し、細胞自身のMYCタンパク質に緑色蛍光タグを組み込みました。これらの細胞では、緑の信号が明るいほどMYCが多く存在することを示します。タグが細胞の自然なMYCに融合しているため、その活性や制御は実際の病態生物学にできるだけ近いままです。著者らは、この蛍光MYCが元のタンパク質と同様に振る舞うことを慎重に検証しました:既知のMYC低下薬に反応すること、遺伝子編集でMYC遺伝子を切断すると減少すること、そして核内で通常の結合パートナーと相互作用し続けることを確認しています。この検証済みの細胞株が大規模探索の基盤となりました。
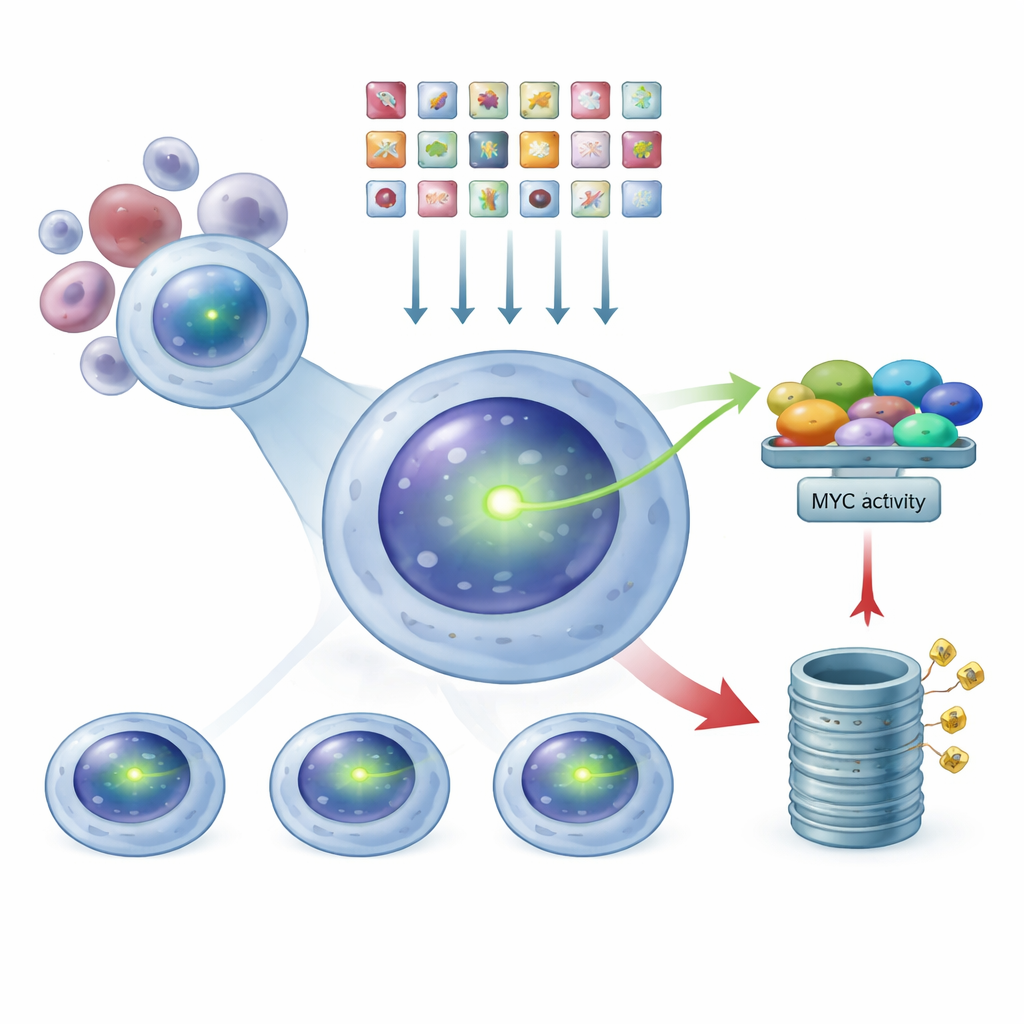
CRISPRを全ゲノムの調光スイッチとして使う
この発光レポーターシステムを用い、研究者らはCRISPR技術を全ゲノム規模の調光スイッチのように使いました。数万種類のガイドRNAライブラリを導入し、それぞれが1つのヒト遺伝子をノックアウトするよう設計されたものをMYCタグ付き骨髄腫細胞に投入しました。各細胞は平均してほぼ1つの遺伝学的変化を受けます。編集の効果が現れるのを待った後、セルソーターで緑の明るさに基づき集団をMYC低、中央値、MYC高の3つのグループに分離しました。各グループでどのガイドRNAが濃縮されているかをシーケンスすることで、どの遺伝子のノックアウトがMYCレベルの低下または上昇を引き起こしたかを逆算できます。
2つの主な制御ハブ:転写とタンパク質処分
スクリーニングから浮かび上がったパターンは、MYC制御因子の主に2つのクラスを示しました。Mediator複合体と呼ばれる大規模分子集合体の構成要素が破壊されるとMYCレベルが低下し、これらの因子は通常MYC遺伝子の転写を助ける“活性化因子”に分類されました。一方で、プロテアソームという細胞のタンパク質分解機構や、分解タグを付け外しする酵素の一部が失われるとMYCレベルは上昇しました。これはMYCが単に生成量で制御されるだけでなく、積極的な分解によって抑えられていることを示します。MYCを増強するIRF4や、その破壊を促すFBXW7のような既知の因子が期待通りに検出され、スクリーニングがノイズではなく実際の生物学を捉えていることに信頼性を与えました。
特定のMYCブレーキとしてのUBE3Cに注目
多数の候補の中で際立っていたのがUBE3Cです。UBE3Cはタンパク質に破壊の印を付けるのを助け、プロテアソームと一時的に結合する酵素です。UBE3Cをノックアウトすると、レポーター細胞でMYCレベルが顕著に上昇し、関連するUBE3AやUBE3Bと比べてもはるかに強い影響を示しました。著者らは修飾されていない多発性骨髄腫細胞株でもUBE3Cを無効化してみて、同様にネイティブな(タグのない)MYCタンパク質が増加することを確認しました。これにより、UBE3Cは骨髄腫細胞におけるMYCの重要な負の制御因子であることが示唆されます。同時に本研究は、MYCの量が転写機構による遺伝子の押し上げと、タンパク質が標識されて細胞内の“リサイクル箱”に送られる活発さの両方によって形作られていることを示しています。
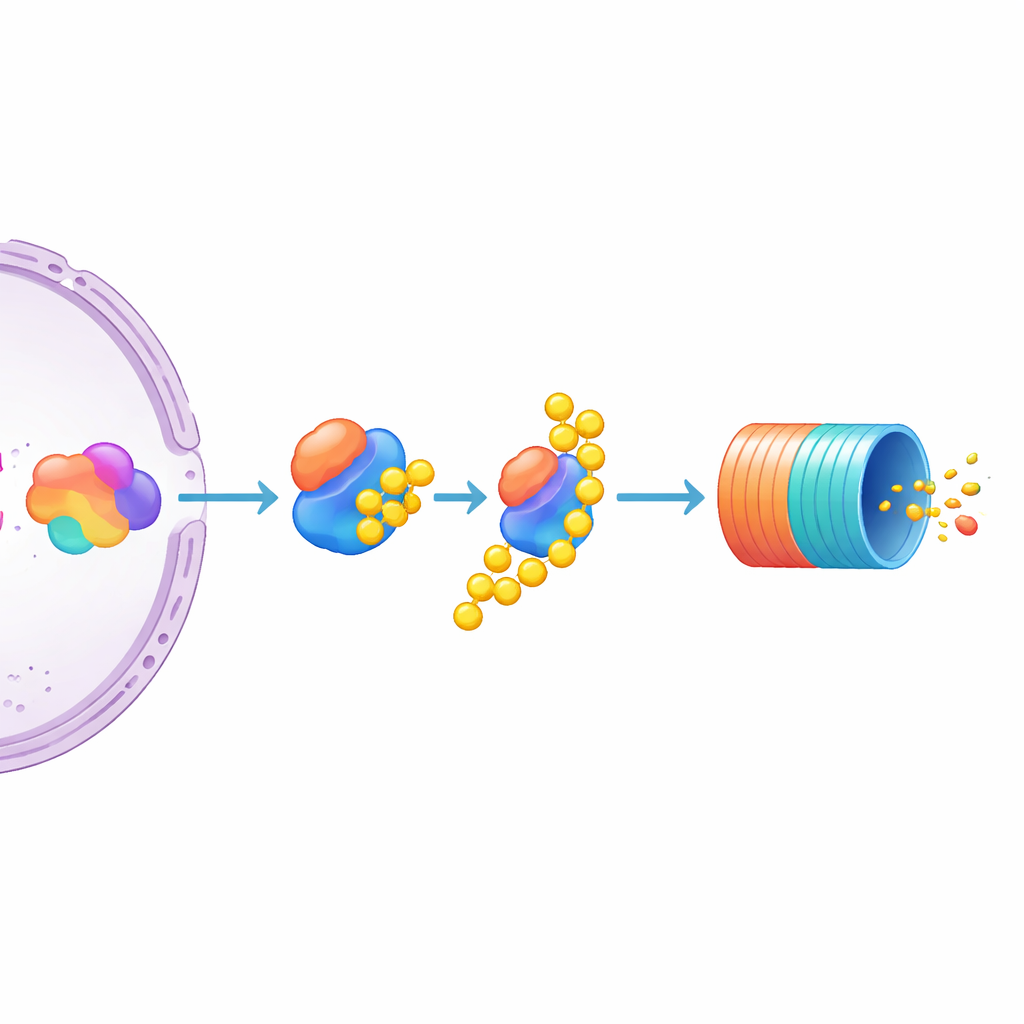
今後のがん治療への意味
専門外の方への要点は、MYC自体は依然として薬剤ターゲットとして扱いにくいかもしれませんが、それを制御するネットワークはますます明らかになってきているということです。MYCを蛍光レポーターに変え、全ゲノムCRISPRスクリーニングと組み合わせることで、著者らは多発性骨髄腫細胞内でMYCを上げるか下げるかする遺伝子群の強力なマップを作りました。データは、MYC産生を駆動するエンジンの一部としてのMediator構成要素を浮き彫りにし、より注目すべきはMYCタンパク質の蓄積を防ぐスイッチとしてUBE3Cを同定した点です。長期的には、UBE3Cのような調節因子やMYCの産生・処分の他の過程を調節する薬剤が、MYCそのものに直接対峙することなくこのマスタースイッチを静め、MYC駆動性のがんの進行を遅らせるより精密な方法を提供する可能性があります。
引用: Seibert, M., Kurrle, N., Kaleab, S. et al. Endogenous protein tagging coupled with a CRISPR screening approach identifies UBE3C as a potential MYC oncogene regulator. Sci Rep 16, 12194 (2026). https://doi.org/10.1038/s41598-026-47974-w
キーワード: MYC調節, 多発性骨髄腫, CRISPRスクリーニング, ユビキチン・プロテアソーム, UBE3C