Clear Sky Science · ru
Внутреннее мечение белка в сочетании с CRISPR‑скринингом выявляет UBE3C как потенциального регулятора онкогена MYC
Почему это исследование важно
Онкологи давно знают, что мощный «главный переключатель» — белок MYC — способствует росту, делению опухолевых клеток и их устойчивости к лечению. При множественной миеломе, раке клеток, производящих антитела, MYC часто оказывается постоянно «включённым». Но прямое блокирование MYC технически сложно. В этом исследовании применён иной подход: вместо попытки прямо «поддеть» MYC авторы системно искали другие гены, которые контролируют количество MYC в клетке миеломы. Их работа выявляет новые молекулярные рычаги — в особенности белок UBE3C — которые в будущем может быть легче нацелить лекарствами.
Преобразование MYC в живой световой сенсор
Чтобы наблюдать MYC внутри раковых клеток, не нарушая их естественной регуляции, исследователи создали линию клеток множественной миеломы, в которой собственный белок MYC несёт встроенный зелёный флуоресцентный метку. В этих клетках ярче‑зелёный сигнал означает больше MYC. Поскольку метка слита с природным MYC клетки, его активность и регуляция остаются максимально приближенными к реальной биологии болезни. Авторы тщательно проверили, что флуоресцентный MYC ведёт себя как исходный белок: он реагирует на известный препарат, снижающий MYC, может уменьшаться при вырезании гена MYC инструментами редактирования и продолжает взаимодействовать со своим обычным партнёром в ядре. Эта валидация сделала клеточную линию основой для их широкомасштабного поиска.
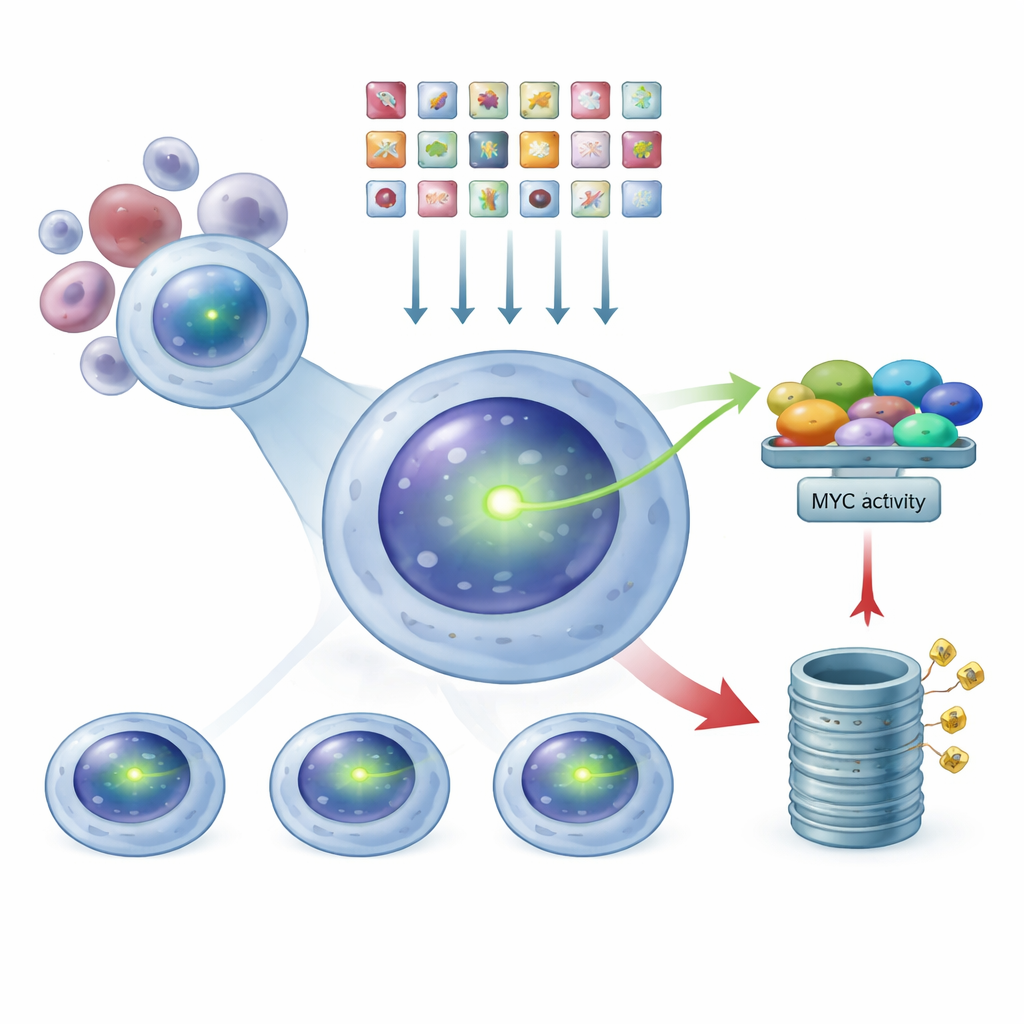
Использование CRISPR как диммера для всего генома
Вооружившись этой светящейся системой‑репортёром, исследователи применили технологию CRISPR как некий диммер на уровне всего генома. Они ввели библиотеку из десятков тысяч направляющих РНК, каждая из которых нацелена на выключение одного человеческого гена, в клетки миеломы с меченым MYC. В среднем каждая клетка получила лишь одно генетическое «попадание». После времени, необходимого для реализации этих правок, их распределили с помощью сортировщика клеток на три группы по уровню зелёной яркости: низкий, средний и высокий MYC. Секвенируя, какие направляющие были обогащены в каждой группе, они смогли восстановить, какие выключенные гены приводили к снижению или повышению уровней MYC.
Два основных узла контроля: транскрипция и утилизация белка
Шаблон, выявленный скринингом, показал две крупные категории регуляторов MYC. При нарушении компонентов большого молекулярного комплекса Mediator уровни MYC падали — эти факторы попадают в группу «активаторов», поскольку обычно помогают включать ген MYC. Напротив, при утрате частей протеасомы — клеточного механизма «измельчения» белков — или ферментов, присоединяющих или снимающих метки для деградации, уровни MYC повышались. Это указывает на то, что MYC обычно контролируется активным разрушением, а не только регуляцией его синтеза. Известные участники, такие как IRF4, усиливающий MYC, и FBXW7, способствующий его уничтожению, проявились там, где ожидалось, что добавляет уверенности: скрининг фиксирует настоящую биологию, а не шум.
Сужение фокуса на UBE3C как специфическом тормозе MYC
Среди множества кандидатов выделился один: UBE3C — фермент, который помогает помечать белки для разрушения и временно ассоциируется с протеасомой. Выключение UBE3C вызывало заметное увеличение уровней MYC в репортерных клетках, гораздо сильнее, чем при потере родственных ферментов UBE3A и UBE3B, которые практически не влияли. Авторы затем проверили немодифицированные линии клеток множественной миеломы и обнаружили, что подавление UBE3C там также повышало уровень нативного, немеченого белка MYC. Это указывает на UBE3C как на особенно важный отрицательный регулятор MYC в клетках миеломы. Одновременно исследование показывает, что количество MYC формируется совместным действием транскрипционного «нажатия» на ген и активного помечания белка для утилизации в клеточную «перерабатывающую систему».
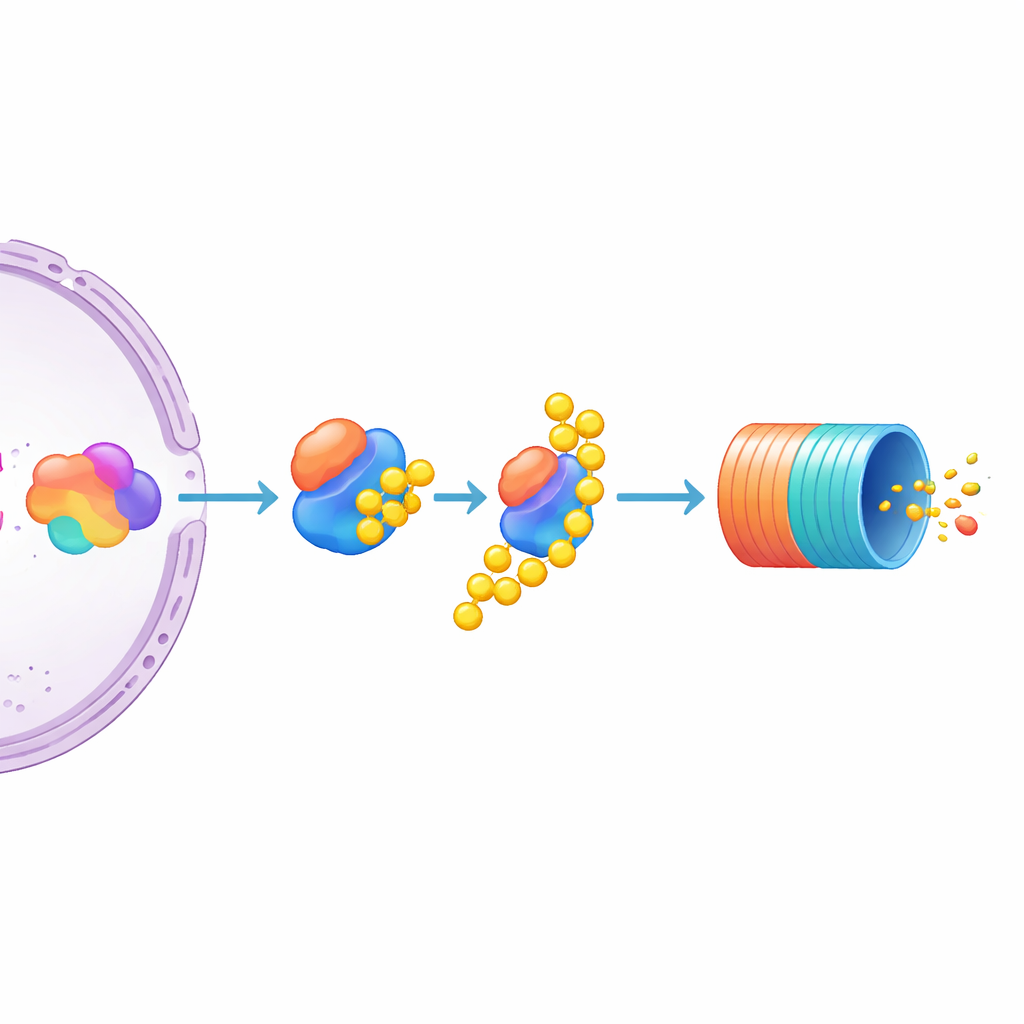
Что это значит для будущих противораковых терапий
Для неспециалистов ключевая мысль в том, что сам MYC по‑прежнему может оставаться труднодоступной мишенью, но сеть, которая его контролирует, проясняется. Превратив MYC в флуоресцентный репортёр и сочетая это с геномно‑масштабным CRISPR‑поиском, авторы составили мощную карту генов, которые либо усиливают, либо подавляют MYC в клетках множественной миеломы. Их данные выделяют компоненты Mediator как часть механизма, задающего производство MYC, и, что более примечательно, идентифицируют UBE3C как вероятный переключатель, препятствующий накоплению белка MYC. В долгосрочной перспективе лекарства, модулирующие регуляторы вроде UBE3C — либо другие шаги в пути синтеза и утилизации MYC — могут предложить более точные способы «приглушить» этот главный переключатель и замедлить развитие опухолей, обусловленных MYC, без необходимости напрямую атаковать сам MYC.
Цитирование: Seibert, M., Kurrle, N., Kaleab, S. et al. Endogenous protein tagging coupled with a CRISPR screening approach identifies UBE3C as a potential MYC oncogene regulator. Sci Rep 16, 12194 (2026). https://doi.org/10.1038/s41598-026-47974-w
Ключевые слова: Регуляция MYC, множественная миелома, CRISPR‑скрининг, убиквитин‑протеасомная система, UBE3C