Clear Sky Science · ar
وَسْم البروتين الداخلي المقترَن بمنهجية فحص CRISPR يحدد UBE3C كمنظم محتمل لمُسرطِن MYC
لماذا تهم هذه الدراسة
يعلم أطباء السرطان منذ زمن طويل أن بروتينًا قويًا يُشبه "مفتاح التشغيل الرئيسي" يُدعَى MYC يساعد خلايا الورم على النمو والانقسام ومقاومة العلاج. في المَيَيَّة المتعددة، وهو سرطان يصيب خلايا الدم المبتَعدة بإنتاج الأجسام المضادة، يكون MYC غالبًا في وضع "تشغيل" مستمر. لكن تعطيل MYC مباشرةً ثبت أنه صعب تقنيًا. تتبنى هذه الدراسة نهجًا مختلفًا: بدلًا من محاولة استهداف MYC نفسه بعقاقير، بحث الباحثون بشكل منظّم عن جينات أخرى تتحكم في مقدار MYC الذي تصنعه خلية المَيَيَّة. تكشف أعمالهم عن رافعات جزيئية جديدة — لا سيما بروتين يُسمى UBE3C — قد تكون أسهل لاستهدافها بعلاجات مستقبلية.
تحويل MYC إلى مستشعر ضوئي حي
لمراقبة MYC داخل خلايا السرطان من دون إزعاج داراتها الطبيعية، مهّد الفريق خط خَلَوي من المَيَيَّة المتعددة بحيث يحمل بروتين MYC نفسه وسمًا فلوريًا أخضر مدمجًا. في هذه الخلايا، كلما ازداد إشعاع اللون الأخضر ازداد وجود MYC. وبما أن الوسم ملتحم بـMYC الطبيعي للخلية، تبقى نشاطاته وضوابطه قريبة قدر الإمكان من بيولوجيا المرض الحقيقية. تحقّق المؤلفون بعناية من أن هذا MYC المفلور لم يفقد سلوكه الأصلي: يستجيب لدواء معروف يخفض MYC، يمكن تقليله بقطع جين MYC باستخدام أدوات التحرير الجيني، ويستمر في التفاعل مع شريكه الاعتيادي في النواة. أصبح هذا الخط الخَلَوي المُثبت أساس بحثهم واسع النطاق.
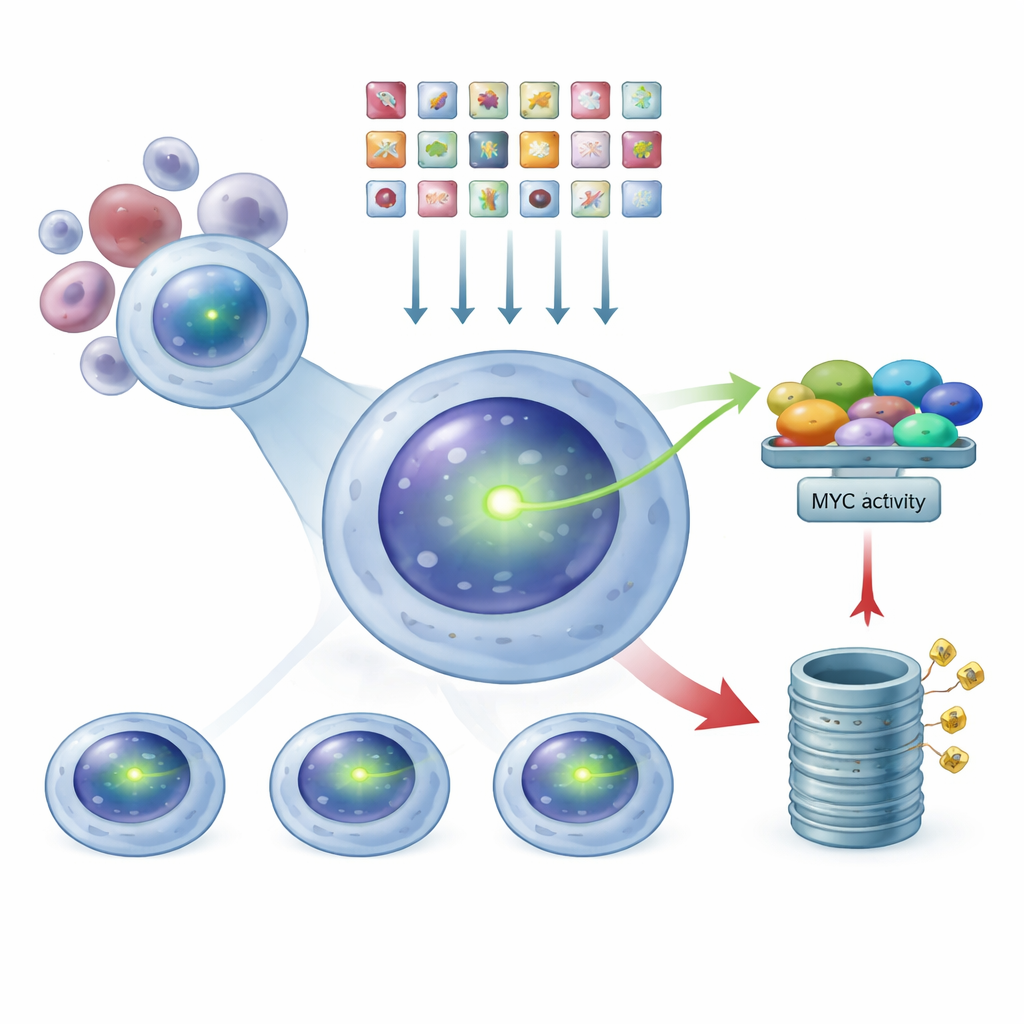
استخدام CRISPR كمفتاح تعتيم على مستوى الجينوم
مسلّحين بهذا النظام المبلّغ المتوهج، استخدم الباحثون تكنولوجيا CRISPR كنوع من مفتاح التعتيم على مستوى الجينوم. أدخلوا مكتبة مكوّنة من عشرات الآلاف من رهانات RNA المرشدة، صُممت كل منها لتعطيل جين بشري واحد، في خلايا المَيَيَّة الموسومة بـMYC. تلقت كل خلية، في المتوسط، ضربة جينية واحدة فقط. بعد منح الوقت لتترسخ هذه التعديلات، استخدموا جهاز فرز الخلايا لتقسيم السكان إلى ثلاث مجموعات بناءً على سطوع الأخضر: منخفضة MYC ومتوسطة وعالية MYC. من خلال تسلسل أي رهانات الدليل كانت مُثرية في كل مجموعة، استطاعوا الاستدلال بالعكس على أي الجينات المعطلة تسببت في انخفاض أو ارتفاع مستويات MYC.
محوران تحكميان رئيسيان: النسخ والتخلص من البروتين
أظهر النمط الناتج من هذا الفحص فئتين كبيرتين من منظمات MYC. عندما تعطلت مكوّنات هيئة جزيئية كبيرة تُسمى مركب الميدياتور (Mediator)، انخفضت مستويات MYC، مما يضع هذه العوامل في معسكر "المنَشِّطات" — إذ تساعد عادةً الخلايا على تشغيل جين MYC. بالمقابل، عندما فُقِدت أجزاء من آلية تفتيت البروتين في الخلية، البروتيازوم، أو إنزيمات تُلصق أو تزيل وِشَحَات التحلّل الصغيرة، ارتفعت مستويات MYC. هذا يشير إلى أن MYC يُحافظ عليه عادةً بتفكيكٍ نشط، وليس فقط بالتحكم في مقدار تصنيعه. ظهرت عوامل معروفة مثل IRF4، التي تعزز MYC، وFBXW7، التي تشجّع على تدميره، في المواقع المتوقعة تمامًا، مما يعزز الثقة بأن الفحص كان يلتقط بيولوجيا حقيقية بدلًا من ضوضاء.
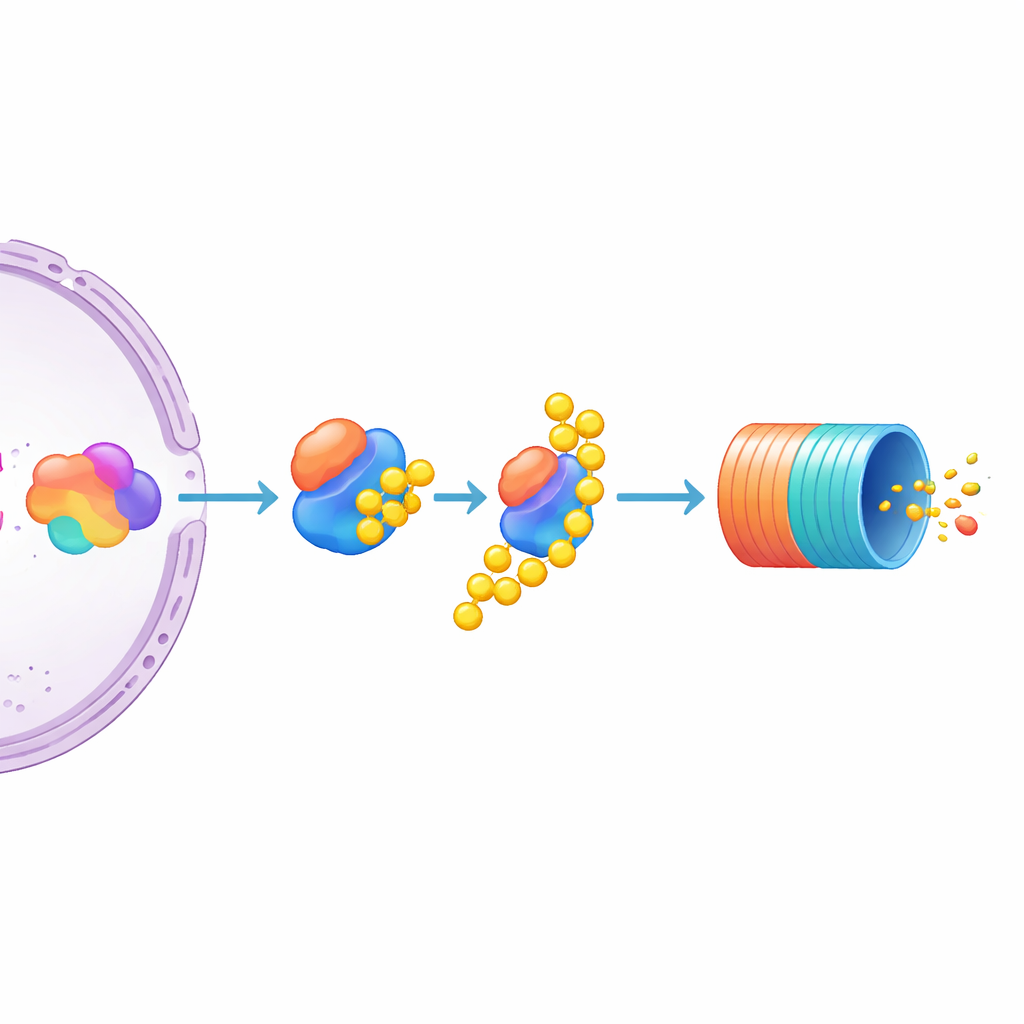
التركيز على UBE3C كفرملة محددة لـMYC
من بين العديد من المرشَّحين، برز واحد: UBE3C، إنزيم يساعد في وسم البروتينات للتحلل ويرتبط مؤقتًا بالبروتيازوم. أدى تعطيل UBE3C إلى ارتفاع لافت في مستويات MYC في الخلايا المبلّغة، وكان أقوى بكثير من الإنزيمات القريبة UBE3A وUBE3B، اللتين لم تُظهِرا تأثيرًا يذكر. بعد ذلك اختبر المؤلفون خطوط خلايا مَيَيَّة غير مُعدَّلة ووجدوا أن تعطيل UBE3C فيها عزّز أيضًا بروتين MYC الأصلي غير الموسوم. يشير هذا إلى أن UBE3C منظم سلبي مهم بشكل خاص لـMYC في خلايا المَيَيَّة. في الوقت نفسه، توحي الدراسة بأن وفرة MYC تتشكل بالاشتراك بين مدى ضغط جهاز النسخ على جينه ومدى وسم البروتين ونقله إلى "سلة إعادة التدوير" الخلوية.
ما الذي يعنيه هذا لعلاجات السرطان المستقبلية
لغير المتخصصين، الخلاصة الأساسية هي أن MYC نفسه قد يظل هدفًا دوائيًا زلقًا، لكن الشبكة التي تتحكم فيه أصبحت أوضح. من خلال تحويل MYC إلى مرسل فلوري وربطه ببحث CRISPR على مستوى الجينوم، بنى المؤلفون خريطة قوية للجينات التي ترفع أو تخفض MYC داخل خلايا المَيَيَّة. تبرز بياناتهم مكونات الميدياتور كجزء من المحرك الذي يقود إنتاج MYC وبشكل أكثر لفتًا تُحدّد UBE3C كمفتاح محتمل يساعد على منع تراكم بروتين MYC. على المدى الطويل، قد توفر أدوية تستهدف منظمات مثل UBE3C — أو خطوات أخرى في تصنيع MYC والتخلص منه — طرقًا أدق لإسكات هذا المفتاح الرئيسي وإبطاء السرطانات المدفوعة بـMYC من دون الحاجة لضرب MYC مباشرة.
الاستشهاد: Seibert, M., Kurrle, N., Kaleab, S. et al. Endogenous protein tagging coupled with a CRISPR screening approach identifies UBE3C as a potential MYC oncogene regulator. Sci Rep 16, 12194 (2026). https://doi.org/10.1038/s41598-026-47974-w
الكلمات المفتاحية: تنظيم MYC, المَيَيَّة المتعددة (Multiple myeloma), فحص CRISPR, نِظام يوبِيكوتين وبروتيازوم, UBE3C