Clear Sky Science · pt
Marcação endógena de proteína aliada a uma triagem CRISPR identifica UBE3C como potencial regulador oncogênico de MYC
Por que este estudo importa
Médicos oncologistas sabem há muito tempo que uma poderosa proteína “chave mestra” chamada MYC ajuda células tumorais a crescer, se dividir e resistir a tratamentos. No mieloma múltiplo, um câncer de células produtoras de anticorpos, o MYC frequentemente fica preso na posição “ligado”. Mas bloquear diretamente o MYC tem se mostrado tecnicamente difícil. Este estudo segue um caminho diferente: em vez de tentar atingir o MYC em si, os pesquisadores buscaram sistematicamente outros genes que controlam quanto MYC uma célula de mieloma produz. O trabalho revela novas alavancas moleculares — especialmente uma proteína chamada UBE3C — que podem ser mais fáceis de direcionar com terapias futuras.
Transformando o MYC em um sensor luminoso vivo
Para observar o MYC dentro de células cancerosas sem perturbar sua regulação natural, a equipe modificou uma linhagem celular de mieloma múltiplo para que sua própria proteína MYC carregasse uma etiqueta fluorescente verde embutida. Nessas células, quanto mais intenso o sinal verde, maior a quantidade de MYC presente. Como a etiqueta está fundida ao MYC natural da célula, sua atividade e controle permanecem o mais próximo possível da biologia da doença real. Os autores verificaram cuidadosamente que esse MYC fluorescente ainda se comporta como a proteína original: responde a um fármaco conhecido por reduzir o MYC, pode ser diminuído cortando o gene MYC com ferramentas de edição gênica e continua a interagir com seu parceiro habitual no núcleo. Essa linhagem validada tornou‑se a base para a busca em larga escala.
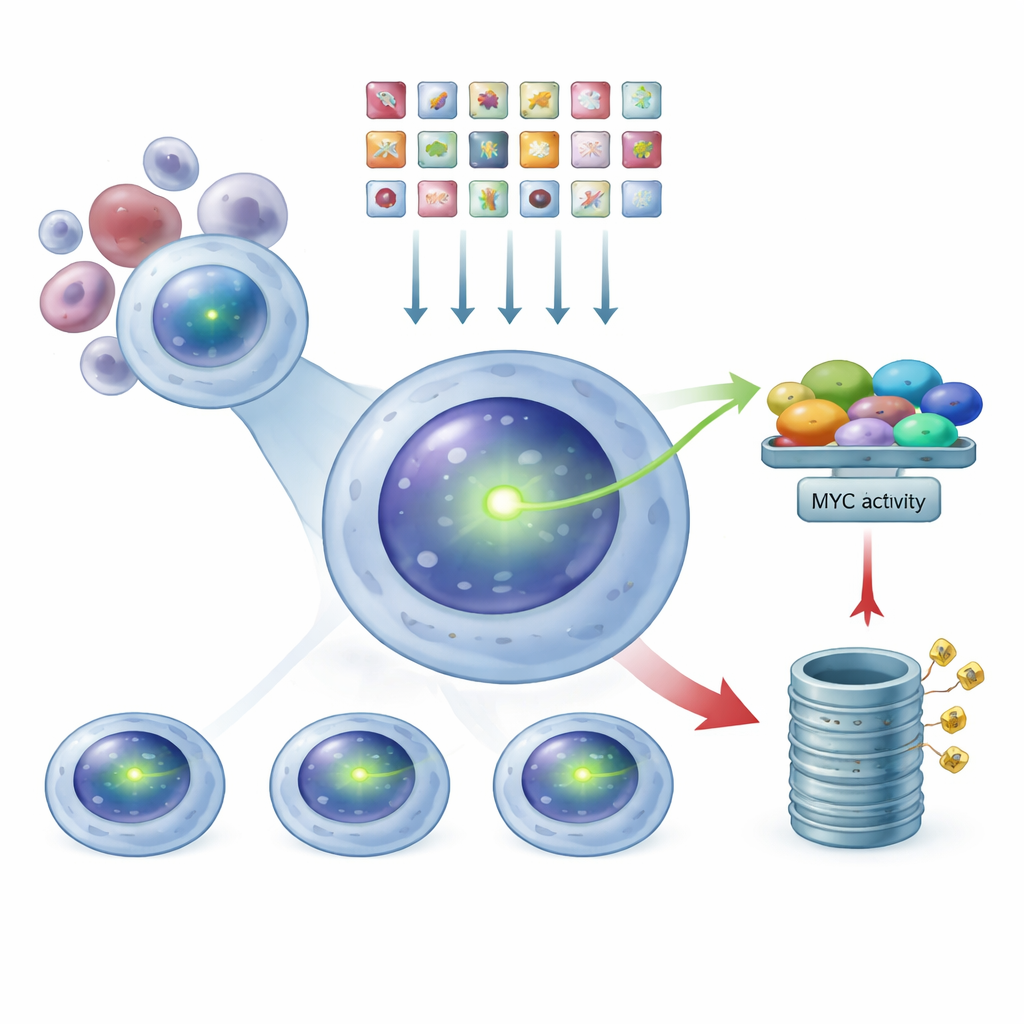
Usando CRISPR como um dimmer genômico
Com esse sistema repórter brilhante, os pesquisadores usaram a tecnologia CRISPR como uma espécie de dimmer genômico. Introduziram uma biblioteca com dezenas de milhares de RNAs guia, cada um projetado para nocaute de um gene humano, nas células de mieloma marcadas com MYC. Cada célula recebeu, em média, apenas uma alteração genética. Após o tempo necessário para que essas edições fizessem efeito, utilizaram um classificador celular para separar a população em três grupos com base na intensidade do verde: MYC‑baixo, intermediário e MYC‑alto. Ao sequenciar quais RNAs guia estavam enriquecidos em cada grupo, puderam inferir retroativamente quais genes nocauteados causaram queda ou aumento dos níveis de MYC.
Dois principais centros de controle: transcrição e descarte de proteínas
O padrão emergente dessa triagem revelou duas grandes classes de reguladores de MYC. Quando componentes de um grande complexo molecular chamado Mediator foram perturbados, os níveis de MYC caíram, colocando esses fatores na categoria de “ativadores” — eles normalmente ajudam a ligar o gene MYC. Em contraste, quando partes da máquina de degradação de proteínas da célula, o proteassoma, ou enzimas que adicionam ou removem pequenas marcas de degradação foram perdidas, os níveis de MYC aumentaram. Isso indica que o MYC é normalmente controlado por degradação ativa, não apenas pelo controle de quanto é produzido. Jogadores conhecidos como IRF4, que aumenta o MYC, e FBXW7, que promove sua destruição, apareceram exatamente onde esperado, dando confiança de que a triagem capturou biologia genuína em vez de ruído.
Focando em UBE3C como um freio específico do MYC
Entre os muitos candidatos, um se destacou: UBE3C, uma enzima que ajuda a marcar proteínas para destruição e que se associa de forma transitória ao proteassoma. O nocaute de UBE3C causou um aumento notável nos níveis de MYC nas células repórter, muito mais forte do que as enzimas relacionadas UBE3A e UBE3B, que tiveram pouco efeito. Os autores então testaram linhagens de mieloma múltiplo não modificadas e descobriram que desativar UBE3C lá também elevava a proteína MYC nativa, sem etiqueta. Isso aponta UBE3C como um regulador negativo particularmente importante do MYC em células de mieloma. Ao mesmo tempo, o estudo sugere que a abundância de MYC é moldada conjuntamente por quanto a maquinaria transcricional estimula seu gene e por quão ativamente a proteína é marcada e encaminhada ao “lixo” celular.
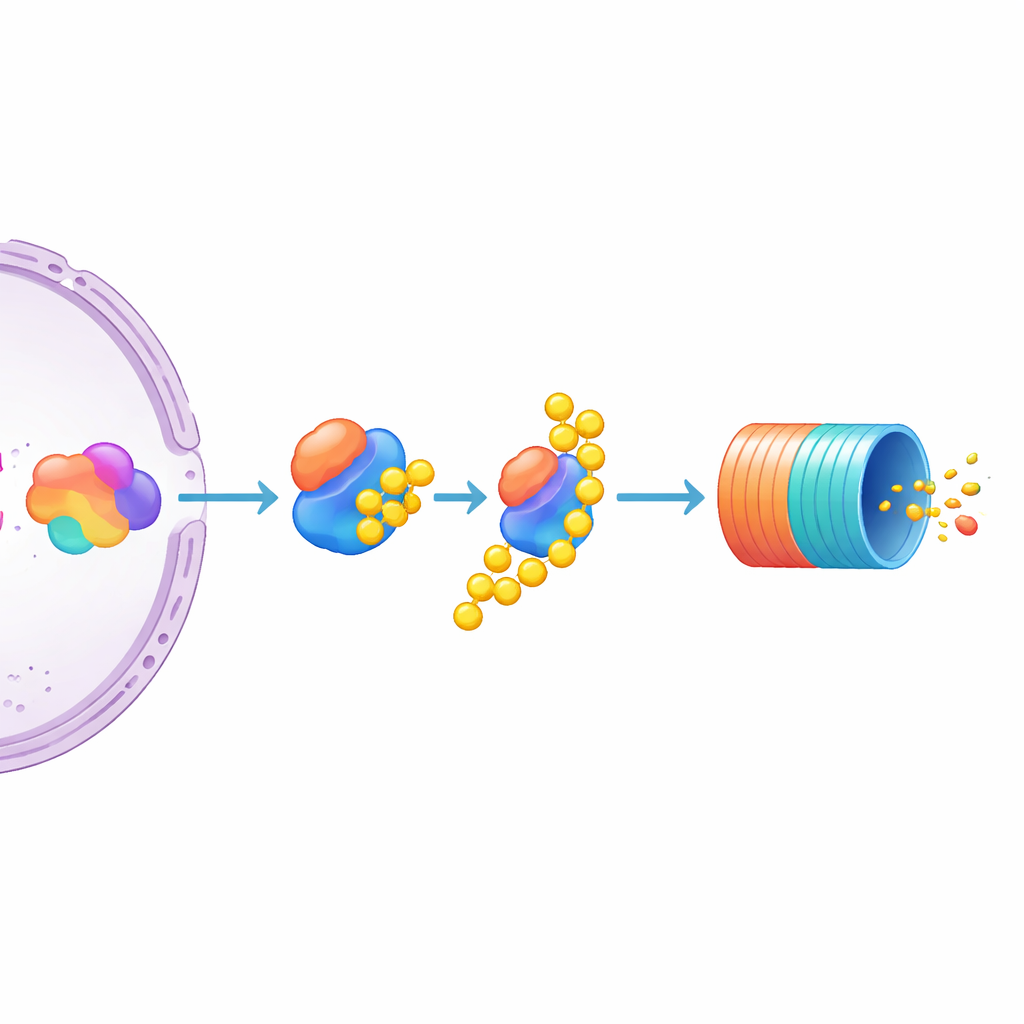
O que isso significa para tratamentos futuros do câncer
Para não especialistas, a conclusão principal é que o próprio MYC pode continuar sendo um alvo farmacológico escorregadio, mas a rede que o controla está se tornando mais clara. Ao converter o MYC em um repórter fluorescente e combiná‑lo com uma triagem CRISPR em todo o genoma, os autores construíram um mapa poderoso de genes que aumentam ou diminuem o MYC dentro de células de mieloma múltiplo. Seus dados destacam componentes do Mediator como parte do motor que impulsiona a produção de MYC e, de forma mais marcante, identificam UBE3C como um provável interruptor que ajuda a impedir o acúmulo da proteína MYC. A longo prazo, drogas que modulem reguladores como UBE3C — ou outras etapas na produção e no descarte do MYC — podem oferecer maneiras mais precisas de silenciar essa chave mestra e desacelerar cânceres dirigidos por MYC sem precisar atingir diretamente o MYC.
Citação: Seibert, M., Kurrle, N., Kaleab, S. et al. Endogenous protein tagging coupled with a CRISPR screening approach identifies UBE3C as a potential MYC oncogene regulator. Sci Rep 16, 12194 (2026). https://doi.org/10.1038/s41598-026-47974-w
Palavras-chave: Regulação de MYC, mieloma múltiplo, triagem CRISPR, ubiquitina proteassoma, UBE3C