Clear Sky Science · es
Etiquetado proteico endógeno acoplado a una estrategia de cribado CRISPR identifica a UBE3C como posible regulador oncogénico de MYC
Por qué importa este estudio
Los oncólogos llevan tiempo sabiendo que una potente proteína «interruptor maestro» llamada MYC ayuda a las células tumorales a crecer, dividirse y resistir los tratamientos. En el mieloma múltiple, un cáncer de las células productoras de anticuerpos en sangre, MYC suele quedar en la posición de «encendido». Pero bloquear MYC directamente ha resultado técnicamente difícil. Este estudio toma un enfoque distinto: en lugar de intentar dirigir fármacos contra MYC mismo, los investigadores buscaron sistemáticamente otros genes que controlan cuánto MYC produce una célula de mieloma. Su trabajo revela nuevas palancas moleculares —especialmente una proteína llamada UBE3C— que podrían ser más fáciles de dirigir con terapias futuras.
Convertir a MYC en un sensor luminoso vivo
Para observar MYC dentro de las células cancerosas sin alterar su cableado habitual, el equipo modificó una línea celular de mieloma múltiple para que su propia proteína MYC llevara una etiqueta fluorescente verde integrada. En estas células, cuanto más intensa es la señal verde, más MYC hay. Como la etiqueta está fusionada a la MYC natural de la célula, su actividad y su regulación permanecen lo más cercanas posible a la biología de la enfermedad real. Los autores comprobaron cuidadosamente que esta MYC fluorescente se comporta igual que la proteína original: responde a un fármaco conocido que reduce MYC, puede disminuirse cortando el gen MYC con herramientas de edición genética y sigue interaccionando con su pareja habitual en el núcleo. Esta línea celular validada se convirtió en la base para su búsqueda a gran escala.
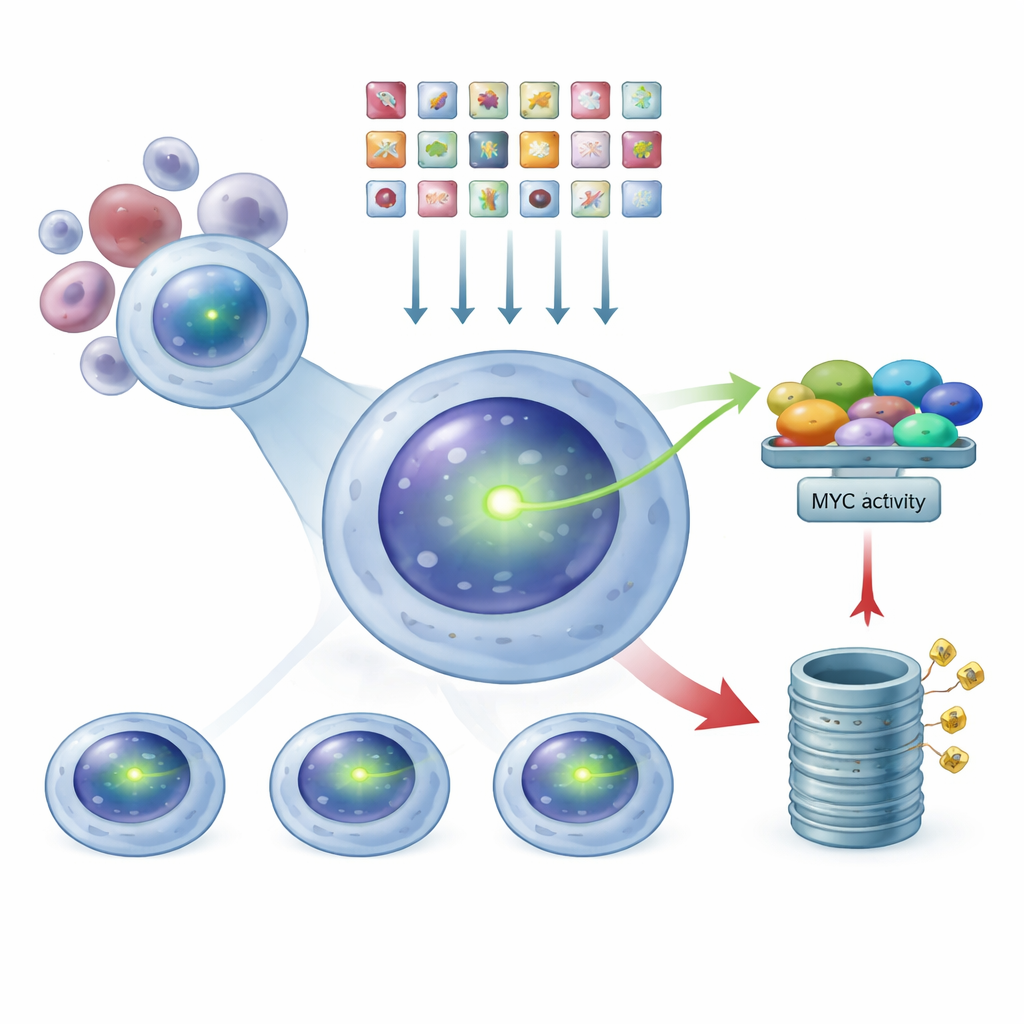
Usar CRISPR como un regulador atenuador a escala del genoma
Con este sistema reportero luminoso, los investigadores emplearon la tecnología CRISPR como una especie de atenuador genómico de amplio alcance. Introdujeron una biblioteca de decenas de miles de ARN guía, cada uno diseñado para eliminar un gen humano, en las células de mieloma con MYC etiquetada. Cada célula recibió, de media, solo un impacto genético. Tras permitir que estas ediciones hicieran efecto, emplearon una máquina de clasificación celular para separar la población en tres grupos según la intensidad del verde: MYC‑baja, intermedia y MYC‑alta. Secuenciando qué ARN guía estaban enriquecidos en cada grupo, pudieron inferir hacia atrás qué genes suprimidos causaban que los niveles de MYC bajaran o subieran.
Dos focos de control principales: transcripción y eliminación de proteínas
El patrón que emergió de este cribado reveló dos grandes clases de reguladores de MYC. Cuando se interrumpían componentes de un gran ensamblaje molecular llamado complejo Mediador, los niveles de MYC caían, situando a estos factores en el bando de los «activadores»: normalmente ayudan a que se active el gen MYC. En contraste, cuando se perdían partes de la maquinaria celular de trituración de proteínas, el proteasoma, o enzimas que añaden o quitan etiquetas de degradación, los niveles de MYC aumentaban. Esto indica que MYC se mantiene habitualmente bajo control mediante su descomposición activa, no solo regulando cuánto se sintetiza. Jugadores ya conocidos, como IRF4, que potencia MYC, y FBXW7, que favorece su destrucción, aparecieron exactamente donde se esperaba, lo que da confianza de que el cribado capturó biología real y no ruido.
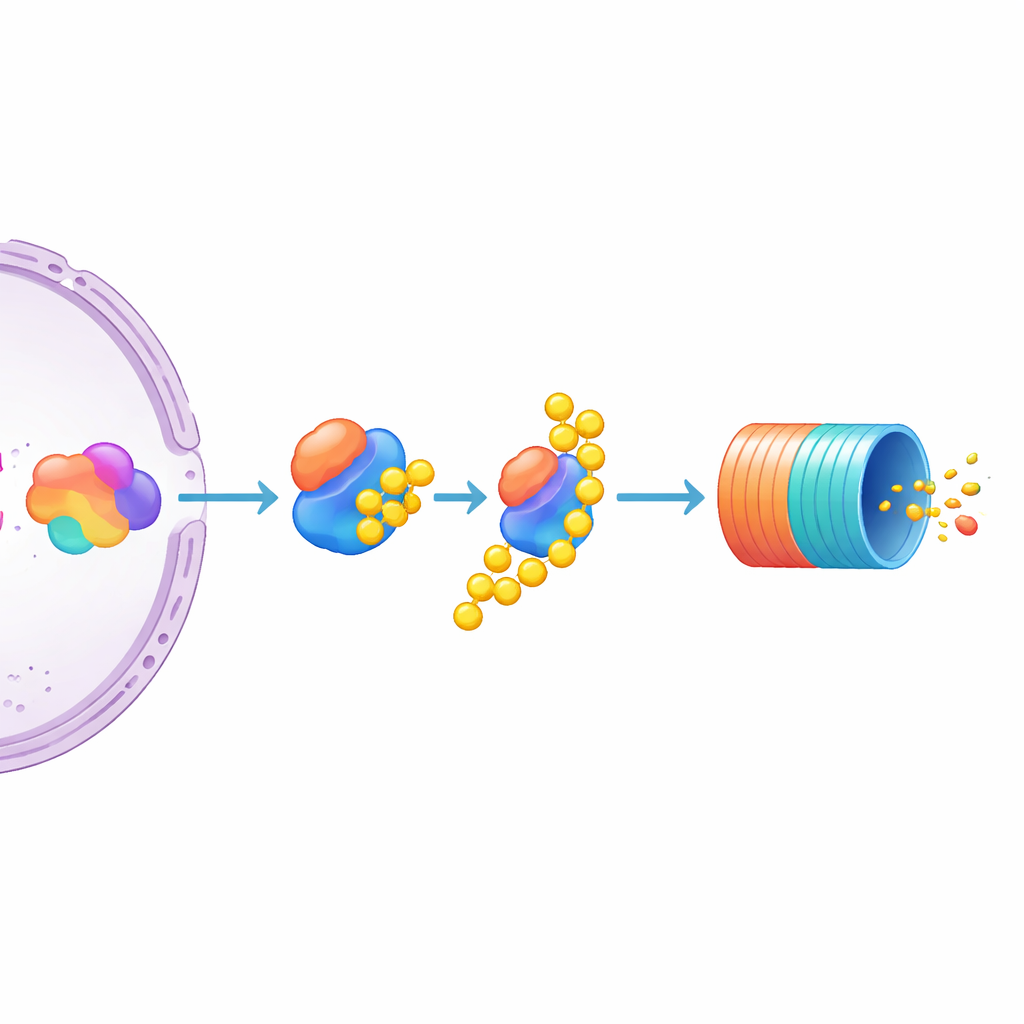
Enfoque en UBE3C como freno específico de MYC
Entre los muchos candidatos, destacó uno: UBE3C, una enzima que ayuda a marcar proteínas para su destrucción y se asocia de forma transitoria con el proteasoma. Eliminar UBE3C provocó un aumento llamativo de los niveles de MYC en las células reporteras, mucho más pronunciado que el de enzimas relacionadas UBE3A y UBE3B, que tuvieron poco efecto. Los autores probaron luego líneas de mieloma múltiple no modificadas y encontraron que desactivar UBE3C allí también incrementaba la proteína MYC nativa y sin etiqueta. Esto apunta a UBE3C como un regulador negativo particularmente importante de MYC en células de mieloma. Al mismo tiempo, el estudio sugiere que la abundancia de MYC viene determinada conjuntamente por la fuerza con que la maquinaria transcripcional impulsa su gen y por la actividad con que la proteína es marcada e introducida en la «papelera de reciclaje» celular.
Qué significa esto para futuros tratamientos contra el cáncer
Para el público no especializado, la idea clave es que MYC puede seguir siendo un objetivo farmacológico esquivo, pero la red que lo controla se está aclarando. Al convertir MYC en un reportero fluorescente y combinarlo con un cribado CRISPR a escala genómica, los autores construyeron un mapa potente de genes que aumentan o disminuyen MYC dentro de las células de mieloma múltiple. Sus datos destacan a componentes del Mediador como parte del motor que impulsa la producción de MYC y, de forma más llamativa, identifican a UBE3C como un interruptor probable que ayuda a evitar la acumulación de la proteína MYC. A largo plazo, fármacos que modulen reguladores como UBE3C —u otras etapas en la producción y eliminación de MYC— podrían ofrecer formas más precisas de silenciar este interruptor maestro y frenar los cánceres impulsados por MYC sin necesidad de atacar MYC directamente.
Cita: Seibert, M., Kurrle, N., Kaleab, S. et al. Endogenous protein tagging coupled with a CRISPR screening approach identifies UBE3C as a potential MYC oncogene regulator. Sci Rep 16, 12194 (2026). https://doi.org/10.1038/s41598-026-47974-w
Palabras clave: Regulación de MYC, mieloma múltiple, cribado CRISPR, ubiquitina proteasoma, UBE3C