Clear Sky Science · sv
Endogen märkning av proteiner tillsammans med en CRISPR-skärm identifierar UBE3C som en potentiell regulator av onkogena MYC
Varför denna studie är viktig
Onkologer har länge känt till att ett kraftfullt "huvudströmbrytare"-protein kallat MYC hjälper tumörceller att växa, dela sig och motstå behandling. Vid multipelt myelom, en cancer i antikroppsproducerande blodceller, sitter MYC ofta fast i "på"-läge. Att blockera MYC direkt har visat sig tekniskt svårt. Denna studie väljer en annan väg: i stället för att försöka droga MYC själv systematiskt söker forskarna efter andra gener som styr hur mycket MYC en myelomcell producerar. Deras arbete avslöjar nya molekylära reglage—särskilt ett protein kallat UBE3C—som kan vara lättare att rikta mot med framtida terapier.
Göra MYC till en levande ljussensor
För att kunna följa MYC inne i cancerceller utan att rubba deras normala kopplingar konstruerade teamet en multipelt myelom-cellinje så att dess egna MYC-protein bär en inbyggd grön fluorescerande etikett. I dessa celler gäller: ju starkare det gröna signalen är, desto mer MYC finns. Eftersom etiketten är fusionerad med cellens naturliga MYC förblir dess aktivitet och reglering så nära verklig sjukdomsbiologi som möjligt. Författarna kontrollerade noggrant att detta fluorescerande MYC fortfarande beter sig som det ursprungliga proteinet: det svarar på ett känt MYC-sänkande läkemedel, kan minskas genom att klippa MYC-genen med genredigeringsverktyg, och fortsätter interagera med sin vanliga bindningspartner i kärnan. Denna validerade cellinje blev grunden för deras storskaliga sökning.
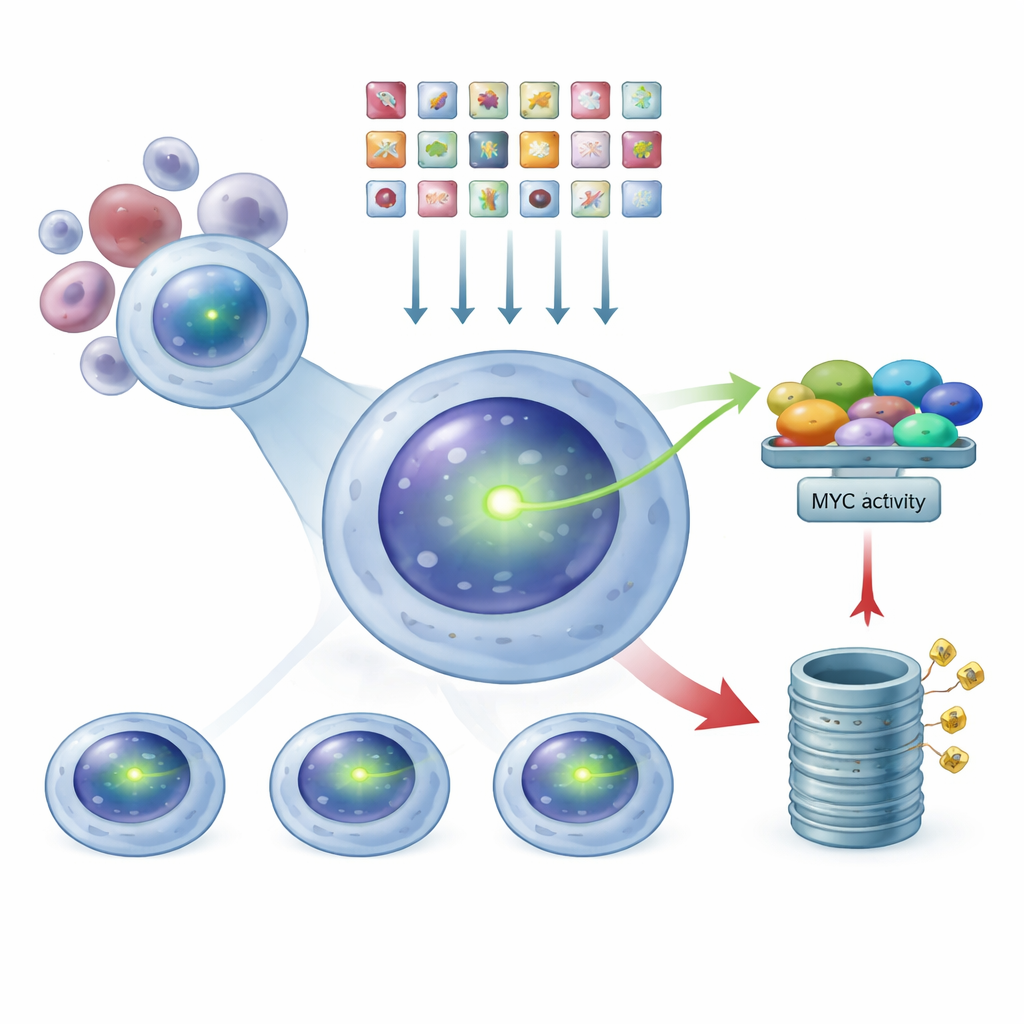
Använda CRISPR som en genomomfattande dimmer
Utrustade med detta glödande rapportörsystem använde forskarna CRISPR-teknik som en slags genomomfattande dimmer. De införde ett bibliotek med tiotusentals guide-RNA, vardera utformat för att slå ut en mänsklig gen, i MYC-märkta myelomceller. Varje cell mottog i genomsnitt bara en genetisk träff. Efter att ha gett tid för dessa redigeringar att slå igenom använde de en cellsorterare för att dela populationen i tre grupper baserat på grön ljusstyrka: MYC-låg, intermediär och MYC-hög. Genom att sekvensera vilka guide-RNA som var berikade i varje grupp kunde de arbeta baklänges för att härleda vilka utslagna gener som fick MYC-nivåerna att sjunka eller stiga.
Två huvudsakliga kontrollnav: transkription och proteinnedbrytning
Mönstret som framträdde från denna skärm visade två stora klasser av MYC-regulatorer. När komponenter i en stor molekylär sammansättning kallad Mediator-komplexet stördes sjönk MYC-nivåerna, vilket placerar dessa faktorer i "aktivator"-lägret—de hjälper normalt celler att slå på MYC-genen. I kontrast, när delar av cellens proteinmalningsmaskineri, proteasomen, eller enzymer som fäster eller tar bort små nedbrytningsmärken förlorades, steg MYC-nivåerna. Detta tyder på att MYC normalt hålls i schack genom aktiv nedbrytning, inte bara genom att kontrollera hur mycket som produceras. Kända aktörer såsom IRF4, som ökar MYC, och FBXW7, som främjar dess nedbrytning, dök upp precis där förväntat, vilket ger förtroende för att skärmen fångade verklig biologi snarare än brus.
Fokusering på UBE3C som en specifik MYC-broms
Bland de många kandidaterna utmärkte sig en: UBE3C, ett enzym som hjälper till att märka proteiner för nedbrytning och tillfälligt associerar med proteasomen. Att slå ut UBE3C orsakade en påtaglig ökning av MYC-nivåerna i rapportörcellerna, mycket starkare än relaterade enzymer UBE3A och UBE3B, som hade liten effekt. Författarna testade sedan omodifierade multipelt myelom-cellinjer och fann att inaktivering av UBE3C där också ökade det inhemska, omärkta MYC-proteinet. Detta pekar på UBE3C som en särskilt viktig negativ regulator av MYC i myelomceller. Samtidigt antyder studien att MYC:s mängd formas gemensamt av hur hårt transkriptionsmaskineriet driver dess gen och hur aktivt proteinet märks och matas in i cellens "återvinningsfack."
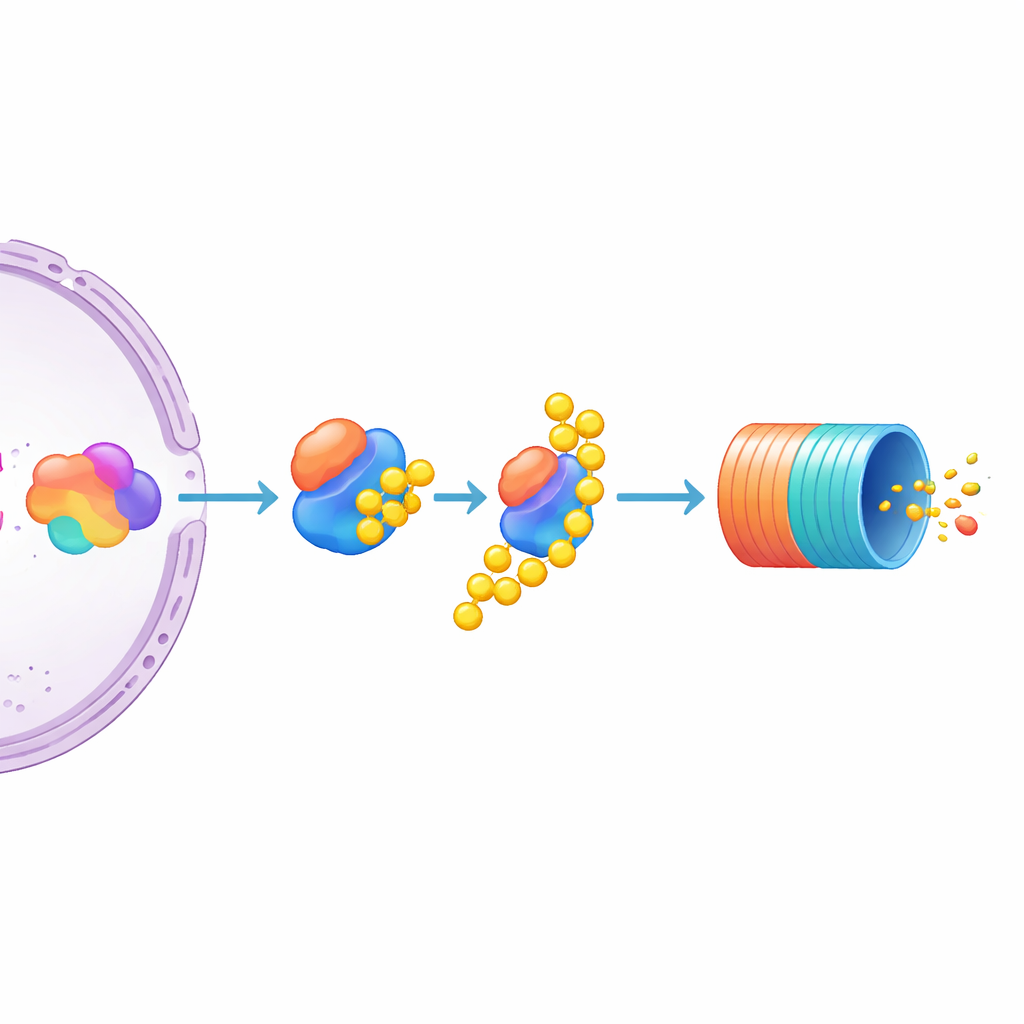
Vad detta betyder för framtida cancerbehandlingar
För icke-specialister är huvudslutsatsen att MYC själv kan förbli ett svårfångat läkemedelsmål, men nätverket som kontrollerar det blir tydligare. Genom att omvandla MYC till en fluorescerande rapportör och para ihop det med en genomomfattande CRISPR-sökning byggde författarna en kraftfull karta över gener som antingen höjer eller sänker MYC inne i multipelt myelom-celler. Deras data framhåller Mediator-komponenter som en del av motorn som driver MYC-produktionen och, mer iögonfallande, identifierar UBE3C som en sannolik brytare som hjälper till att förhindra att MYC-protein ansamlas. I längden skulle läkemedel som modulerar regulatorer som UBE3C—or andra steg i MYC:s produktion och bortforsling—kunna erbjuda mer precisa sätt att tysta denna huvudströmbrytare och sakta ner MYC-drivna cancerformer utan att behöva rikta MYC direkt.
Citering: Seibert, M., Kurrle, N., Kaleab, S. et al. Endogenous protein tagging coupled with a CRISPR screening approach identifies UBE3C as a potential MYC oncogene regulator. Sci Rep 16, 12194 (2026). https://doi.org/10.1038/s41598-026-47974-w
Nyckelord: Reglering av MYC, Multipelt myelom, CRISPR-skärm, Ubiquitin–proteasom, UBE3C