Clear Sky Science · fr
Marquage endogène des protéines couplé à une approche de criblage CRISPR identifie UBE3C comme un régulateur potentiel de l’oncoprotéine MYC
Pourquoi cette étude est importante
Les cancérologues savent depuis longtemps qu’une puissante protéine « interrupteur maître » appelée MYC aide les cellules tumorales à croître, se diviser et résister aux traitements. Dans le myélome multiple, un cancer des cellules sanguines productrices d’anticorps, MYC est souvent maintenu en position « activée ». Mais bloquer directement MYC s’est avéré techniquement difficile. Cette étude adopte une autre stratégie : plutôt que d’essayer de cibler MYC lui‑même, les chercheurs ont recherché systématiquement d’autres gènes qui contrôlent la quantité de MYC produite par une cellule de myélome. Leur travail révèle de nouveaux leviers moléculaires — en particulier une protéine appelée UBE3C — qui pourraient être plus faciles à cibler avec de futures thérapies.
Transformer MYC en capteur lumineux vivant
Pour observer MYC à l’intérieur des cellules cancéreuses sans perturber leur régulation naturelle, l’équipe a modifié une lignée cellulaire de myélome multiple de sorte que la protéine MYC porte une étiquette fluorescente verte intégrée. Dans ces cellules, plus le signal vert est intense, plus MYC est présent. Parce que l’étiquette est fusionnée à MYC naturel de la cellule, son activité et son contrôle restent aussi proches que possible de la biologie de la maladie. Les auteurs ont vérifié avec soin que ce MYC fluorescent se comporte toujours comme la protéine d’origine : il répond à un médicament connu pour diminuer MYC, peut être réduit en coupant le gène MYC avec des outils d’édition génique, et continue d’interagir avec son partenaire habituel dans le noyau. Cette lignée validée est devenue la base de leur recherche à grande échelle.
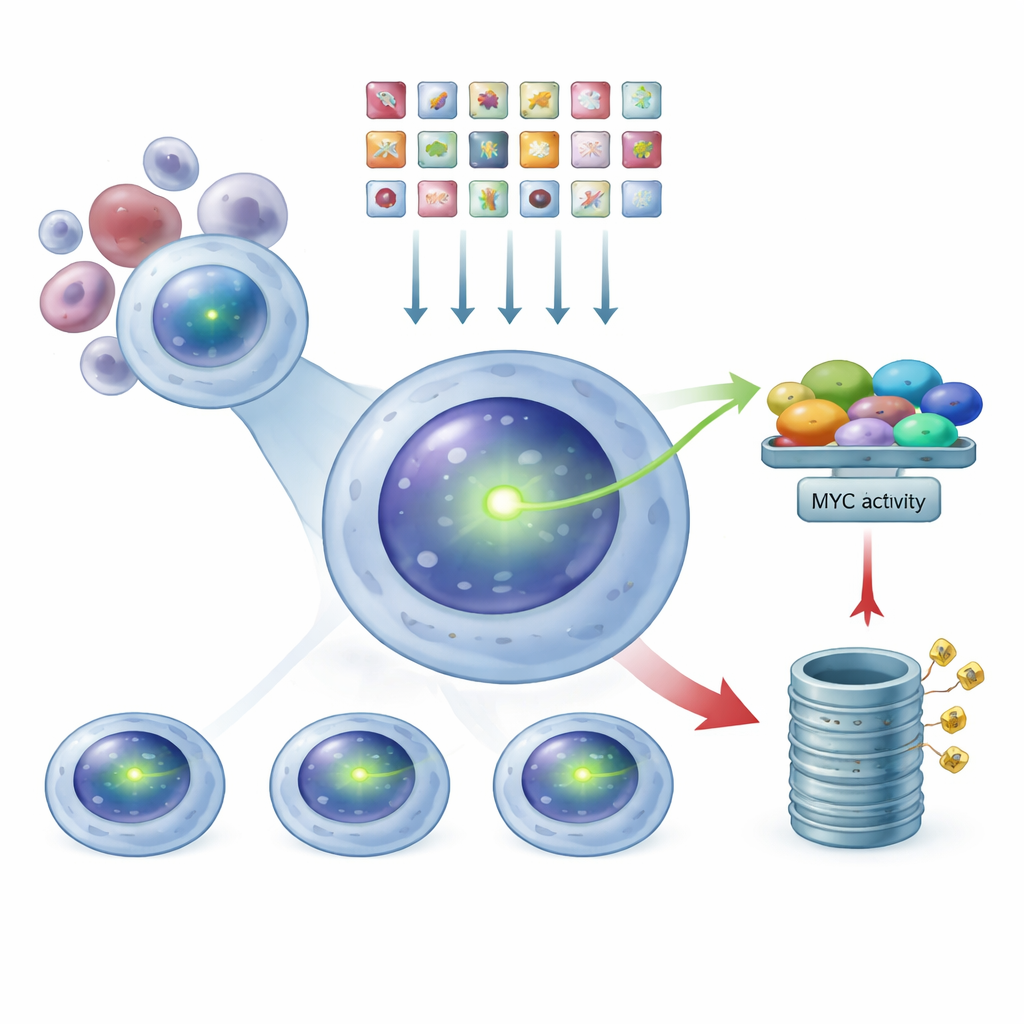
Utiliser CRISPR comme variateur génomique
Grâce à ce système rapporteur lumineux, les chercheurs ont utilisé la technologie CRISPR comme une sorte de variateur à l’échelle du génome. Ils ont introduit une bibliothèque de dizaines de milliers d’ARN guides, chacun conçu pour inactiver un gène humain, dans les cellules de myélome marquées pour MYC. Chaque cellule a reçu, en moyenne, une seule modification génétique. Après avoir laissé le temps à ces modifications de produire leurs effets, ils ont utilisé un trieur cellulaire pour séparer la population en trois groupes selon la luminosité verte : MYC faible, intermédiaire et élevé. En séquençant les ARN guides enrichis dans chaque groupe, ils ont pu remonter aux gènes dont l’inactivation entraînait une baisse ou une hausse de MYC.
Deux principaux pôles de contrôle : la transcription et l’élimination des protéines
Le schéma qui a émergé de ce criblage a révélé deux grandes classes de régulateurs de MYC. Lorsque des composants d’un vaste assemblage moléculaire appelé complexe Mediator étaient perturbés, les niveaux de MYC diminuaient, plaçant ces facteurs dans le camp des « activateurs » — ils aident normalement à activer le gène MYC. En revanche, lorsque des éléments de la machinerie d’élimination des protéines de la cellule, le protéasome, ou des enzymes qui ajoutent ou retirent de petites étiquettes de dégradation étaient perdus, les niveaux de MYC augmentaient. Cela indique que MYC est normalement maintenu sous contrôle par une dégradation active, et pas seulement par la régulation de sa synthèse. Des acteurs connus tels qu’IRF4, qui stimule MYC, et FBXW7, qui favorise sa destruction, sont apparus exactement là où attendu, ce qui donne confiance dans le fait que le criblage capte une biologie réelle plutôt que du bruit.
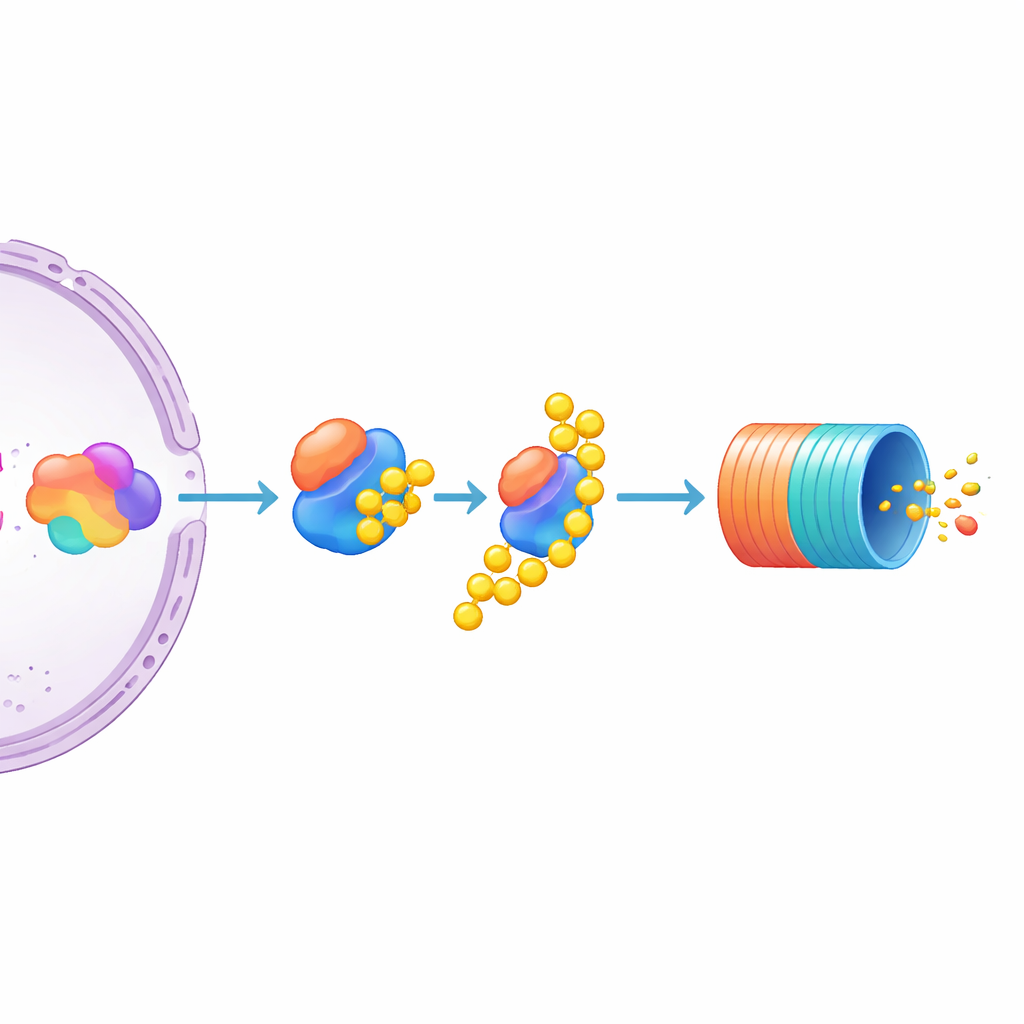
Se focaliser sur UBE3C comme frein spécifique de MYC
Parmi les nombreux candidats, un s’est détaché : UBE3C, une enzyme qui aide à marquer les protéines pour destruction et qui s’associe de façon transitoire au protéasome. L’inactivation de UBE3C a entraîné une augmentation frappante des niveaux de MYC dans les cellules rapporteurs, beaucoup plus marquée que pour les enzymes apparentées UBE3A et UBE3B, qui ont eu peu d’effet. Les auteurs ont ensuite testé des lignées de myélome multiple non modifiées et ont constaté que la désactivation de UBE3C y augmentait également la protéine MYC native, non étiquetée. Cela pointe UBE3C comme un régulateur négatif particulièrement important de MYC dans les cellules de myélome. Simultanément, l’étude suggère que l’abondance de MYC est façonnée conjointement par la poussée de la machinerie transcriptionnelle sur son gène et par l’activité avec laquelle la protéine est marquée puis acheminée vers le « bac de recyclage » cellulaire.
Ce que cela signifie pour les traitements anticancéreux futurs
Pour les non‑spécialistes, la conclusion clé est que MYC lui‑même peut rester une cible médicamenteuse difficile, mais le réseau qui le contrôle devient plus clair. En convertissant MYC en un rapporteur fluorescent et en le combinant à un criblage CRISPR à l’échelle du génome, les auteurs ont construit une carte puissante des gènes qui augmentent ou diminuent MYC dans les cellules de myélome multiple. Leurs données mettent en lumière les composants du Mediator comme partie du moteur qui stimule la production de MYC et, plus remarquablement, identifient UBE3C comme un interrupteur probable qui aide à empêcher l’accumulation de la protéine MYC. À long terme, des médicaments qui moduleraient des régulateurs comme UBE3C — ou d’autres étapes de la production et de l’élimination de MYC — pourraient offrir des moyens plus précis d’éteindre cet interrupteur maître et de ralentir les cancers entraînés par MYC sans avoir à cibler directement MYC.
Citation: Seibert, M., Kurrle, N., Kaleab, S. et al. Endogenous protein tagging coupled with a CRISPR screening approach identifies UBE3C as a potential MYC oncogene regulator. Sci Rep 16, 12194 (2026). https://doi.org/10.1038/s41598-026-47974-w
Mots-clés: Régulation de MYC, myélome multiple, criblage CRISPR, ubiquitine protéasome, UBE3C