Clear Sky Science · he
תיוג חלבון אנדוגני בשילוב עם מסגרת סריקה מבוססת CRISPR מזהה את UBE3C כמווסת פוטנציאלי של אונקוגן MYC
מדוע המחקר הזה חשוב
רופאי סרטן ידעו זמן רב כי חלבון "מפסיק ראשי" רב עוצמה בשם MYC מסייע לתאי גידול לגדול, להתחלק ולהתנגד לטיפול. במיאלומה נפוצה, סרטן של תאי דם שמייצרים נוגדנים, MYC לעתים קרובות תקוע במצב "דלוק". חסימת MYC ישירה התגלתה כאתגר טכני. המחקר הזה נוקט בגישה שונה: במקום לנסות לתקוף את MYC ישירות, החוקרים חיפשו באופן שיטתי גנים אחרים ששולטים בכמות ה‑MYC שתא מיאלומה מייצר. עבודתם חושפת מנופי מולקולריים חדשים — ובמיוחד חלבון בשם UBE3C — שעשויים להיות קלים יותר למיקוד בטיפולים עתידיים.
הפיכת MYC לחיישן אור חי
כדי לצפות ב‑MYC בתוך תאי סרטן מבלי להפריע לחיווט הייצורי שלהם, הצוות הנדס קו תאי מיאלומה כך שחלבון ה‑MYC הטבעי שלו נושא תג פלואורסצנטי ירוק מובנה. בתאים האלה, ככל שהאות הירוק בוהק יותר — כך יש יותר MYC. מאחר שהתג מחובר ל‑MYC הטבעי של התא, פעילותו והבקרה עליו נשארות קרובות ככל האפשר לביולוגיית המחלה האמיתית. המחברים בדקו בקפידה ש‑MYC הפלואורסצנטי הזה עדיין מתנהג כמו החלבון המקורי: הוא מגיב לתרופה ידועה שמפחיתה MYC, ניתן להורידו על‑ידי חיתוך גן ה‑MYC עם כלי עריכה גנומית, והוא ממשיך לאינטראקציה עם שותפו הקשור בגרעין. קו תאים מאומת זה הפך לבסיס לחיפוש הנרחב שלהם.
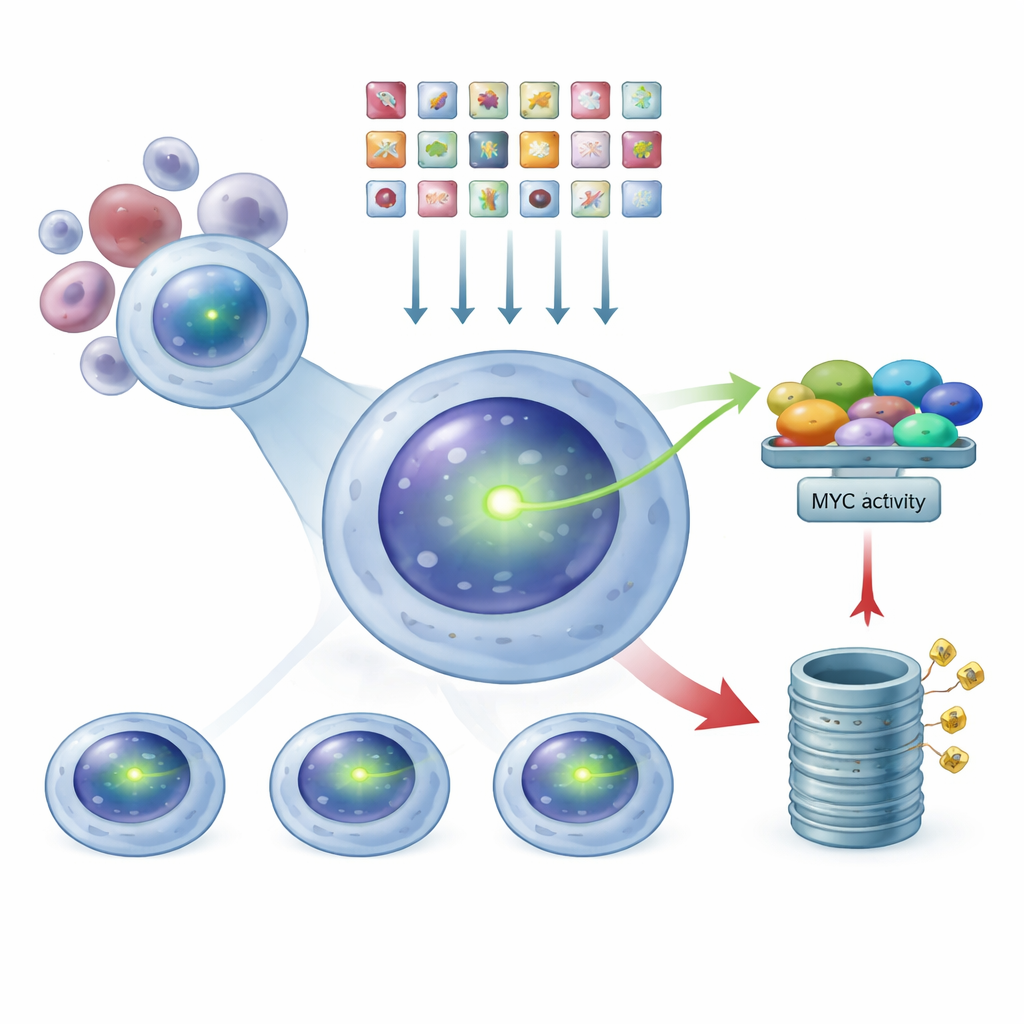
שימוש ב‑CRISPR כמחליש אור רחב‑היקף
מצוידים במערכת דיווח זוהרת זו, החוקרים השתמשו בטכנולוגיית CRISPR כסוג של מתג דימור (מחליש) ברמת הגנום כולו. הם הציגו ספרייה של עשרות אלפי מולקולות RNA מנחות, כל אחת מעוצבת להפיל ביטוי של גן אנושי אחד, לתאי המיאלומה המסומנים ב‑MYC. כל תא קיבל, בממוצע, פגיעה גנטית אחת בלבד. אחרי שזמנו שלפו להשלמת העריכות, הפרידו אותם באמצעות מיון תאים לשלוש קבוצות לפי בהירות הירוק: MYC‑נמוך, בינוני ו‑MYC‑גבוה. על‑ידי רצף של אילו RNA מנחות התרבו בכל קבוצה, הם יכלו להסיק אחורה אילו גנים שבוטלו גרמו לירידה או לעלייה ברמות MYC.
שני מרכזי בקרה עיקריים: שעתוק ופינוי חלבונים
התבנית שצצה מהסריקה חשפה שתי קטגוריות עיקריות של מווסתי MYC. כאשר רכיבים של מכלול מולקולרי גדול שנקרא Mediator הופרעו, רמות MYC ירדו, מה שממקם את אותם גורמים במחנה ה"מפעילים" — הם בדרך כלל מסייעים להפעלת גן ה‑MYC. לעומת זאת, כאשר חלקים ממכונת פירוק החלבונים של התא, הפרוטאוזום, או אנזימים שמצמידים או מסירים תגי פירוק קטנים הוסרו, רמות MYC עלו. זה מצביע על כך ש‑MYC בדרך כלל נשמר תחת שליטה על‑ידי פירוק פעיל, ולא רק על‑ידי בקרת ייצורו. שחקנים ידועים כגון IRF4, שמגבירה את MYC, ו‑FBXW7, שמעודדת את השחתתו, הופיעו בדיוק במקום המצופה, מה שמחזק את הביטחון שהסריקה תופסת ביולוגיה ממשית ולא רעש.
מיקוד ב‑UBE3C כבלם ספציפי של MYC
מבין המועמדים הרבים, אחד בלט: UBE3C, אנזים שמסייע לסמן חלבונים להשמדה ומתאסף לתקופות קצרות עם הפרוטאוזום. ניכוי UBE3C גרם לעלייה בולטת ברמות MYC בתאי הדיווח, הרבה יותר חזקה מההשפעה של אנזימים קרובים UBE3A ו‑UBE3B, שלמעשה השפעתם הייתה מועטה. המחברים בדקו גם קווי תאי מיאלומה לא‑ממוטגים ומצאו כי נטרול UBE3C שם גם מגביר את חלבון ה‑MYC הטבעי והלא‑מסומן. ממצא זה מצביע על UBE3C כמווסת שלילי חשוב של MYC בתאי מיאלומה. במקביל, המחקר מרמז כי שפעו של MYC מעוצב במשותף על‑ידי כמה גורמים — כמה חזק המכונה השעתוקית דוחפת את הגן וכמה פעיל המסלול המסמן ומזין את החלבון אל "פח המחזור" התאי.
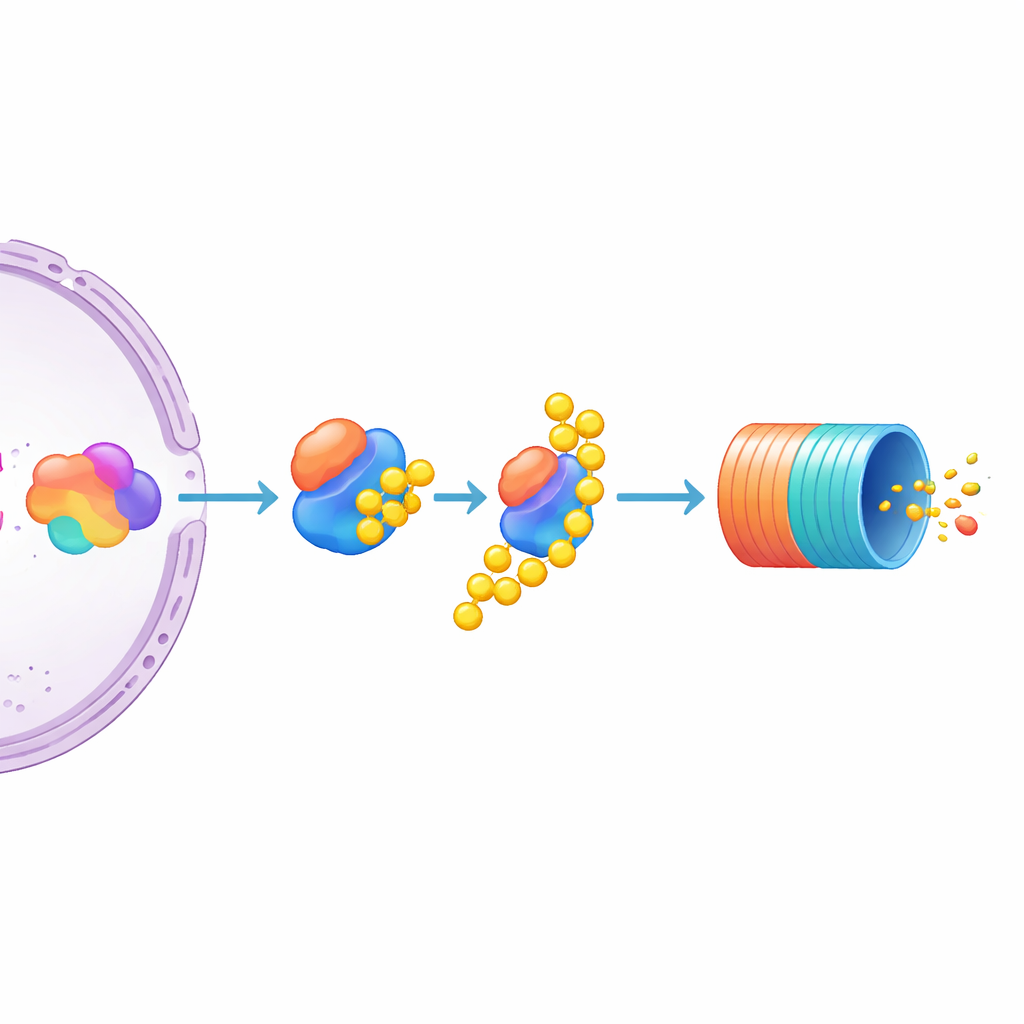
מה המשמעות לכך עבור טיפולי סרטן בעתיד
עבור קוראים שאינם מומחים, המסקנה המרכזית היא ש‑MYC עצמו עשוי להישאר מטרה קשה לתרופות, אבל הרשת השולטת בו נהיית ברורה יותר. בהפיכת MYC לדיווח פלואורסצנטי ושילובו עם סריקת CRISPR על‑רמת הגנום, המחברים בנו מפה עוצמתית של גנים שמגבירים או מפחיתים את רמות MYC בתוך תאי מיאלומה נפוצה. הנתונים שלהם מדגישים רכיבי Mediator כחלק מהמנוע שמניע את ייצור ה‑MYC ובאופן בולט מזהים את UBE3C כמפסק סביר שעוזר למנוע הצטברות חלבון MYC. בטווח הארוך, תרופות שמווסתות רגולטורים כמו UBE3C — או שלבים אחרים בייצור ובפינוי של MYC — יכולות להציע דרכים מדויקות יותר לדכא את המפסק הראשי הזה ולהאט סרטן מונעי MYC מבלי לצוד את MYC ישירות.
ציטוט: Seibert, M., Kurrle, N., Kaleab, S. et al. Endogenous protein tagging coupled with a CRISPR screening approach identifies UBE3C as a potential MYC oncogene regulator. Sci Rep 16, 12194 (2026). https://doi.org/10.1038/s41598-026-47974-w
מילות מפתח: ויסות MYC, מיאלומה נפוצה, סריקת CRISPR, אוביקוויטין‑פרוטאוזום, UBE3C