Clear Sky Science · de
Endogenes Protein‑Tagging gekoppelt mit einem CRISPR‑Screening‑Ansatz identifiziert UBE3C als potenziellen MYC‑Onkogenregulator
Warum diese Studie wichtig ist
Krebsärzte wissen seit Langem, dass ein mächtiges „Hauptschalter“-Protein namens MYC Tumorzellen beim Wachsen, Teilen und bei der Resistenz gegen Therapien unterstützt. Beim multiplen Myelom, einer Krebserkrankung der Antikörper produzierenden Blutzellen, befindet sich MYC häufig dauerhaft in der „Ein“-Position. MYC direkt zu blockieren erwies sich jedoch als technisch schwierig. Diese Studie wählt einen anderen Ansatz: Statt zu versuchen, MYC selbst zu binden, suchten die Forschenden systematisch nach anderen Genen, die steuern, wie viel MYC eine Myelomzelle produziert. Ihre Arbeit offenbart neue molekulare Hebel — insbesondere ein Protein namens UBE3C — die sich möglicherweise leichter mit künftigen Therapien ansprechen lassen.
MYC in einen lebenden Lichtsensor verwandeln
Um MYC in Krebszellen zu beobachten, ohne deren natürliche Signalwege zu stören, erzeugte das Team eine multiple‑Myelom‑Zelllinie, sodass das körpereigene MYC‑Protein ein eingebautes grünes Fluoreszenzsignal trägt. In diesen Zellen gilt: je heller das Grün, desto mehr MYC ist vorhanden. Weil das Tag an das natürliche MYC der Zelle gekoppelt ist, bleiben seine Aktivität und Kontrolle so nah wie möglich an der realen Krankheitsbiologie. Die Autoren überprüften sorgfältig, dass dieses fluoreszierende MYC sich wie das ursprüngliche Protein verhält: Es reagiert auf ein bekanntes MYC‑senkendes Medikament, kann durch Ausschalten des MYC‑Gens mit Geneditierung reduziert werden und interagiert weiterhin mit seinem üblichen Bindungspartner im Zellkern. Diese validierte Zelllinie bildete die Grundlage für ihre umfangreiche Suche.
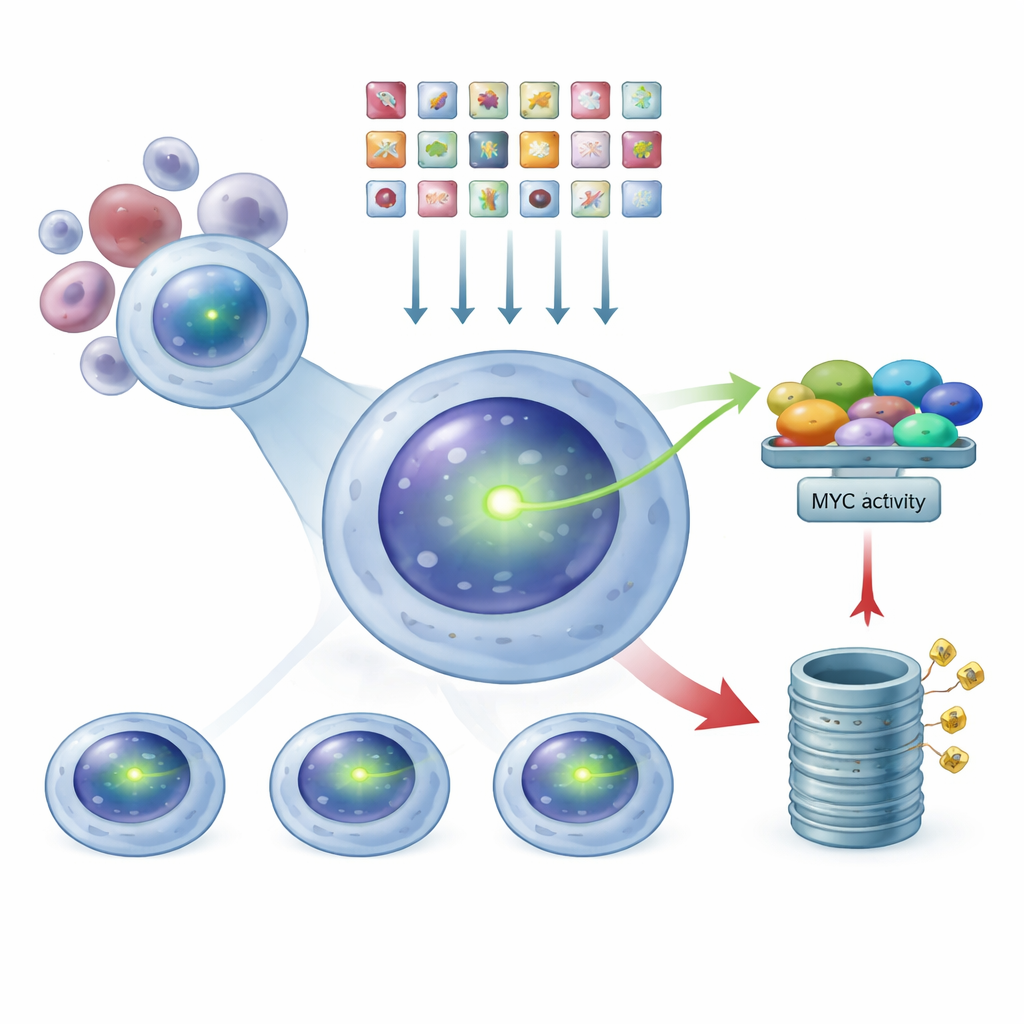
CRISPR als genomeweites Dimmer‑Schalter verwenden
Mit diesem leuchtenden Reportersystem setzten die Forschenden CRISPR‑Technologie als eine Art genomeweiten Dimmer ein. Sie führten eine Bibliothek mit Zehntausenden von Guide‑RNAs ein, von denen jede darauf ausgelegt war, ein menschliches Gen auszuschalten, in die MYC‑getaggten Myelomzellen. Jede Zelle erhielt im Mittel nur einen genetischen Treffer. Nachdem den Editierungen Zeit gegeben wurde, Wirkung zu entfalten, separierten sie die Population mit einer Zell‑Sortiermaschine in drei Gruppen nach Grünhelligkeit: MYC‑niedrig, intermediär und MYC‑hoch. Durch Sequenzierung der in jeder Gruppe angereicherten Guide‑RNAs konnten sie rückschließen, welche ausgeschalteten Gene zu sinkenden oder steigenden MYC‑Spiegeln führten.
Zwei Hauptsteuerzentren: Transkription und Protein‑Entsorgung
Das Muster, das aus diesem Screen hervorging, offenbarte zwei große Klassen von MYC‑Regulatoren. Wenn Komponenten eines großen molekularen Komplexes namens Mediator gestört wurden, sanken die MYC‑Spiegel — diese Faktoren gehören also zur Gruppe der „Aktivatoren“, die normalerweise helfen, das MYC‑Gen einzuschalten. Im Gegensatz dazu führten Verluste von Teilen der zellulären Protein‑Schredder‑Maschinerie, des Proteasoms, oder von Enzymen, die kleine Abbau‑Markierungen anheften oder entfernen, zu einem Anstieg von MYC. Das deutet darauf hin, dass MYC üblicherweise aktiv durch Abbau in Schach gehalten wird und nicht nur durch die Steuerung seiner Synthese. Bekannte Akteure wie IRF4, das MYC fördert, und FBXW7, das dessen Zerstörung unterstützt, erschienen genau dort, wo erwartet — ein Hinweis darauf, dass der Screen echte biologische Signale und kein Rauschen erfasste.
Fokussierung auf UBE3C als spezifische MYC‑Bremse
Unter den vielen Kandidaten stach einer hervor: UBE3C, ein Enzym, das Proteine für den Abbau markiert und zeitweise mit dem Proteasom assoziiert ist. Das Ausschalten von UBE3C führte in den Reporterzellen zu einem auffälligen Anstieg der MYC‑Spiegel, deutlich stärker als bei den verwandten Enzymen UBE3A und UBE3B, die kaum Effekt zeigten. Die Autoren prüften anschließend unveränderte multiple‑Myelom‑Zelllinien und fanden, dass die Deaktivierung von UBE3C dort ebenfalls das native, ungetaggte MYC‑Protein erhöhte. Das deutet darauf hin, dass UBE3C ein besonders wichtiger negativer Regulator von MYC in Myelomzellen ist. Gleichzeitig legt die Studie nahe, dass die MYC‑Menge gemeinsam davon bestimmt wird, wie stark die Transkriptionsmaschinerie sein Gen antreibt und wie aktiv das Protein markiert und dem zellulären „Recycling‑Behälter“ zugeführt wird.
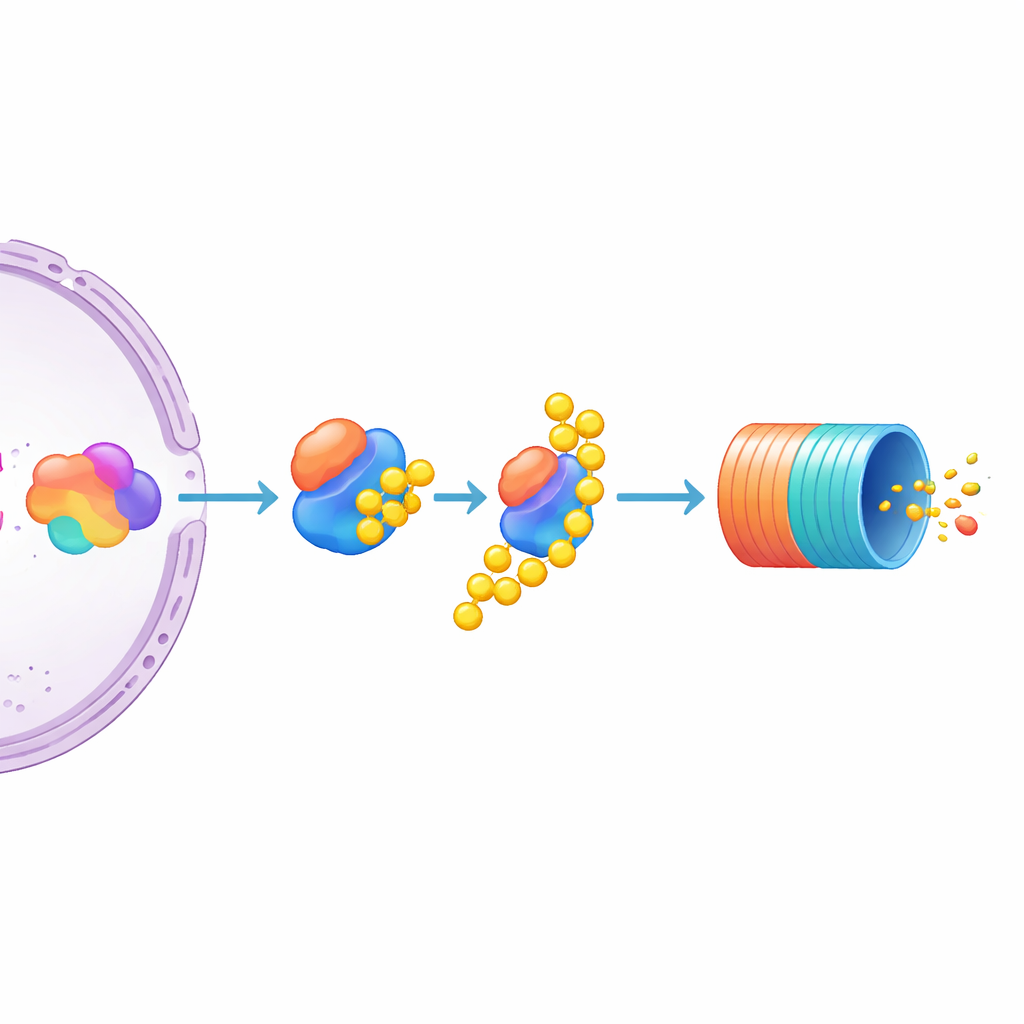
Was das für künftige Krebstherapien bedeutet
Für Nicht‑Spezialisten ist die zentrale Erkenntnis: MYC selbst bleibt vielleicht ein schwer zu treffendes Arzneimittelziel, aber das Netzwerk, das es kontrolliert, wird zunehmend klarer. Indem die Forschenden MYC in einen fluoreszenten Reporter verwandelten und ihn mit einer genomeweiten CRISPR‑Suche kombinierten, erstellten sie eine leistungsfähige Karte von Genen, die MYC in multiplen Myelomzellen entweder hoch- oder runterregulieren. Ihre Daten heben Mediator‑Komponenten als Teil des Motors hervor, der die MYC‑Produktion antreibt, und identifizieren noch deutlicher UBE3C als wahrscheinlichen Schalter, der verhindert, dass MYC‑Protein sich anhäuft. Langfristig könnten Wirkstoffe, die Regulatoren wie UBE3C modulieren — oder andere Schritte in MYCs Produktion und Entsorgung — präzisere Wege bieten, diesen Hauptschalter zu dämpfen und MYC‑getriebene Krebserkrankungen zu verlangsamen, ohne MYC direkt treffen zu müssen.
Zitation: Seibert, M., Kurrle, N., Kaleab, S. et al. Endogenous protein tagging coupled with a CRISPR screening approach identifies UBE3C as a potential MYC oncogene regulator. Sci Rep 16, 12194 (2026). https://doi.org/10.1038/s41598-026-47974-w
Schlüsselwörter: MYC‑Regulation, multiples Myelom, CRISPR‑Screen, Ubiquitin‑Proteasom, UBE3C