Clear Sky Science · tr
Endojen protein etiketleme ve CRISPR tarama yaklaşımının birleşimi UBE3C'yi potansiyel bir MYC onkogen regülatörü olarak tanımlıyor
Bu çalışma neden önemli
Kanser klinisyenleri uzun zamandır MYC adlı güçlü bir "anahtar" proteinin tümör hücrelerinin büyümesine, bölünmesine ve tedaviye direnç göstermesine yardımcı olduğunu biliyor. Antikor üreten kan hücrelerinin kanseri olan multipl miyelomda MYC sıklıkla "açık" pozisyonda kalır. Ancak MYC'yi doğrudan bloke etmek teknik olarak zor oldu. Bu çalışma farklı bir yol izliyor: araştırmacılar MYC'yi doğrudan hedeflemek yerine bir miyelom hücresinin ne kadar MYC ürettiğini kontrol eden diğer genleri sistematik olarak aradı. Yaptıkları çalışma, gelecekteki tedavilerle hedeflemesi daha kolay olabilecek yeni moleküler kollar—özellikle UBE3C adlı bir protein—gün ışığına çıkarıyor.
MYC'yi yaşayan bir ışık sensörüne dönüştürmek
MYC'yi kanser hücreleri içinde normal bağlantılarını bozmayacak biçimde izlemek için ekip, kendi MYC proteini içine yerleştirilmiş yeşil floresan bir etiket taşıyan bir multipl miyelom hücre hattı geliştirdi. Bu hücrelerde yeşil sinyal ne kadar parlaksa, o kadar çok MYC vardır. Etiket hücrenin doğal MYC'sine füzyonlandığı için aktivitesi ve kontrolü gerçek hastalık biyolojisine olabildiğince yakın kalır. Yazarlar bu floresanlı MYC'nin hâlâ orijinal protein gibi davrandığını dikkatle doğruladılar: bilinen bir MYC azaltıcı ilaca yanıt veriyor, gen düzenleme araçlarıyla MYC geni kesildiğinde azalabiliyor ve çekirdekteki alışılmış bağlanma ortağıyla etkileşimini sürdürüyor. Bu doğrulanmış hücre hattı onların geniş ölçekli aramasının temeli oldu.
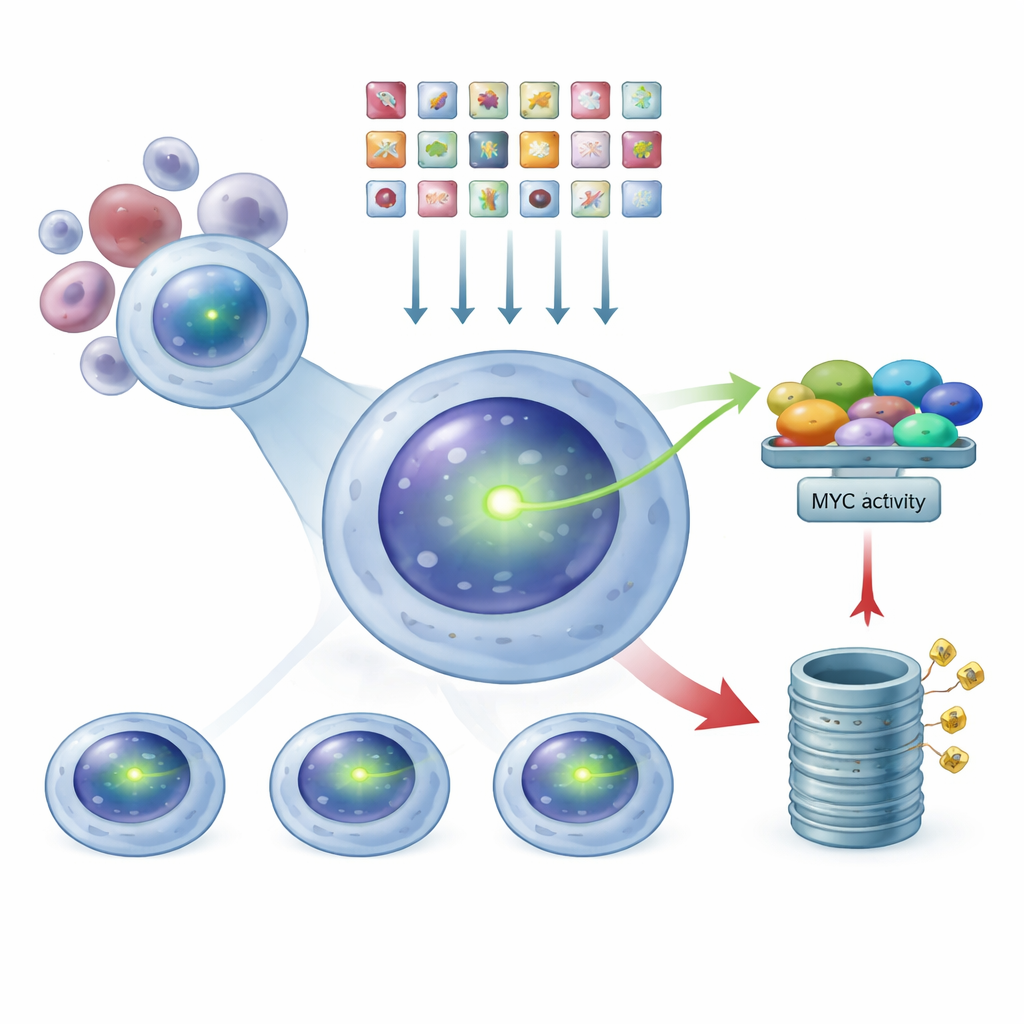
CRISPR'yi genom çapında bir karartma düğmesi olarak kullanmak
Bu parlayan rapor sistemiyle donanmış olarak araştırmacılar CRISPR teknolojisini bir tür genom‑çapında karartma düğmesi gibi kullandılar. Myc ile etiketlenmiş miyelom hücrelerine her biri bir insan genini yok edecek şekilde tasarlanmış on binlerce kılavuz RNA'dan oluşan bir kütüphane yerleştirdiler. Her hücre ortalama olarak yalnızca bir genetik vuruş aldı. Bu düzenlemelerin etkisini göstermesi için zaman tanıdıktan sonra, hücre ayırma makinesiyle popülasyonu yeşil parlaklığa göre üç gruba böldüler: MYC‑düşük, ara ve MYC‑yüksek. Hangi kılavuz RNA'ların hangi grupta zenginleştiğini dizileyerek, hangi genlerin yok edilmesinin MYC seviyelerinin düşmesine veya yükselmesine neden olduğunu geriye dönük çıkarabildiler.
İki ana kontrol merkezi: transkripsiyon ve protein tasfiyesi
Bu taramadan ortaya çıkan desen iki ana MYC düzenleyici sınıfını gösterdi. Mediator kompleksinin büyük bir moleküler bileşeninin öğeleri bozulduğunda MYC seviyeleri düştü; bunlar "aktif edici" grubuna giriyor—normalde MYC geninin açılmasına yardım ediyorlar. Buna karşılık, hücrenin protein öğütme makinası olan proteazomun parçaları veya küçük bozulma işaretleri takan/çıkaran enzimler kaybolduğunda MYC seviyeleri yükseldi. Bu, MYC'nin yalnızca üretiminin kontrol edilmesiyle değil, aktif olarak parçalanarak da dengelendiğini gösteriyor. MYC'yi artıran IRF4 ve yıkımını teşvik eden FBXW7 gibi bilinen oyuncular beklenildiği yerde belirdi; bu da taramanın gerçek biyolojiyi yakaladığına dair güven verdi.
UYBE3C'ye odaklanmak: spesifik bir MYC frenleyicisi
Birçok adayı arasında öne çıkan bir tanesi vardı: UBE3C, proteinleri yıkım için etiketlemeye yardım eden ve geçici olarak proteazomla ilişki kuran bir enzim. UBE3C'nin yok edilmesi raporör hücrelerinde MYC seviyelerinde çarpıcı bir artışa yol açtı; bu etki UBE3A ve UBE3B gibi ilişkili enzimlere göre çok daha güçlüydü ve bu ikisi ise çok az etki gösterdi. Yazarlar daha sonra değiştirilmemiş multipl miyelom hücre hatlarında da UBE3C'yi devre dışı bırakmanın doğal, etiketsiz MYC proteinini artırdığını buldular. Bu, UBE3C'yi miyelom hücrelerinde MYC'nin özellikle önemli bir negatif düzenleyicisi olarak işaretliyor. Aynı zamanda çalışma, MYC bolluğunun hem transkripsiyonel makinenin genine ne kadar baskı uyguladığı hem de proteinin hücresel "geri dönüşüm kutusu"na ne kadar aktif biçimde işaretlenip verildiği tarafından ortaklaşa şekillendirildiğini öne sürüyor.
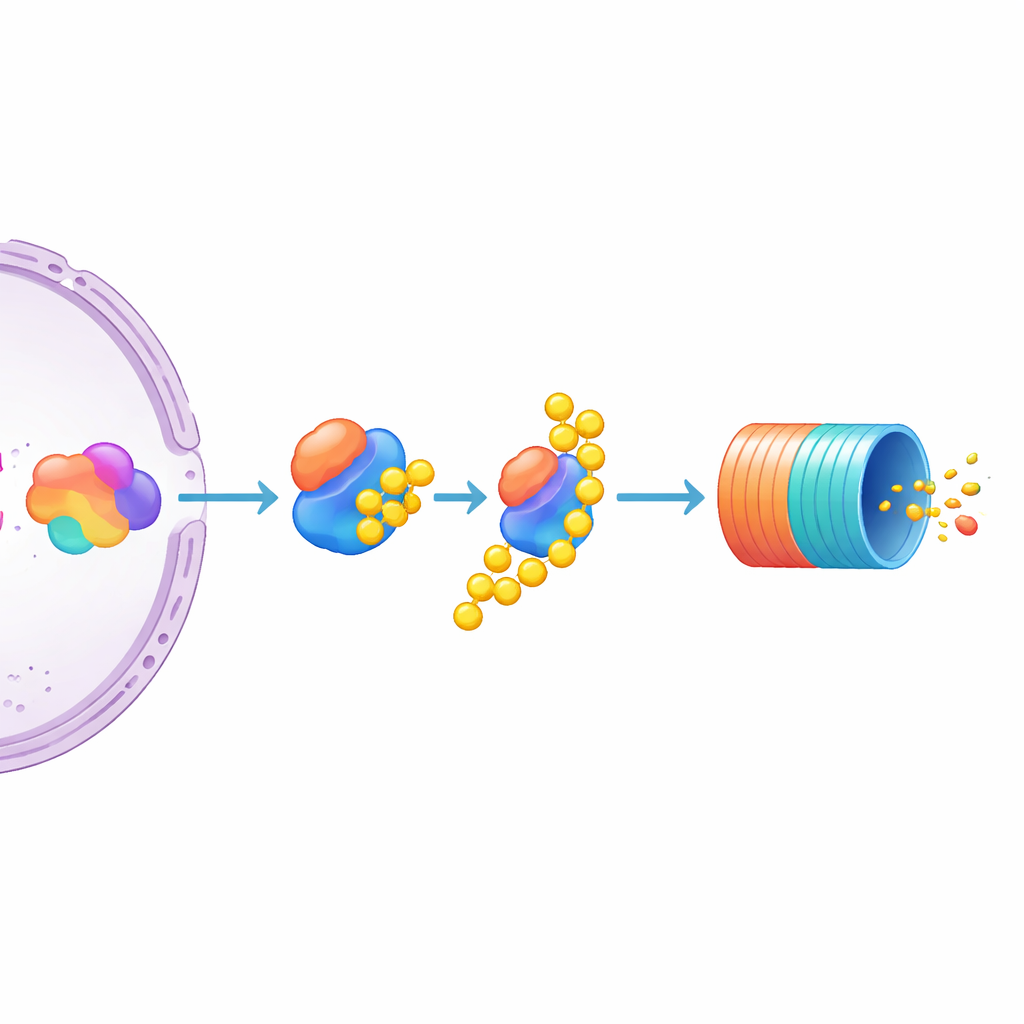
Gelecekteki kanser tedavileri için anlamı
Uzman olmayanlar için ana çıkarım şudur: MYC kendisi hâlâ hedeflenmesi zor bir ilaç hedefi olabilir, ancak onu kontrol eden ağ giderek daha netleşiyor. MYC'yi bir floresan raporöre dönüştürüp bunu genom‑çapında bir CRISPR aramasıyla eşleştirerek yazarlar, multipl miyelom hücreleri içinde MYC'yi ya açan ya da kapatan genlerin güçlü bir haritasını oluşturdular. Verileri, MYC üretimini sürükleyen motorun bir parçası olarak Mediator bileşenlerini vurguluyor ve daha da çarpıcı şekilde UBE3C'yi MYC proteininin birikmesini engellemeye yardımcı olan olası bir anahtar olarak tanımlıyor. Uzun vadede UBE3C gibi düzenleyicileri veya MYC'nin üretimi ve tasfiyesindeki diğer adımları modüle eden ilaçlar, bu anahtar proteini doğrudan hedeflemeye gerek kalmadan MYC kaynaklı kanserleri yavaşlatmak için daha hassas yollar sunabilir.
Atıf: Seibert, M., Kurrle, N., Kaleab, S. et al. Endogenous protein tagging coupled with a CRISPR screening approach identifies UBE3C as a potential MYC oncogene regulator. Sci Rep 16, 12194 (2026). https://doi.org/10.1038/s41598-026-47974-w
Anahtar kelimeler: MYC düzenlemesi, multipl miyelom, CRISPR taraması, ubiquitin proteazom, UBE3C