Clear Sky Science · zh
Pyra-metho-carnil通过结合KDEL受体扰乱癌细胞蛋白质稳态并诱导凋亡
将癌细胞的蛋白质工厂变为自己的敌人
癌细胞生长迅速,产生大量蛋白质,这些蛋白必须在细胞内被小心折叠并运输。这项研究探索了一种能扰乱这种内在运输系统的小分子,使癌细胞被受损蛋白过载直到自我毁灭,同时为靶向肿瘤提供了新的思路。
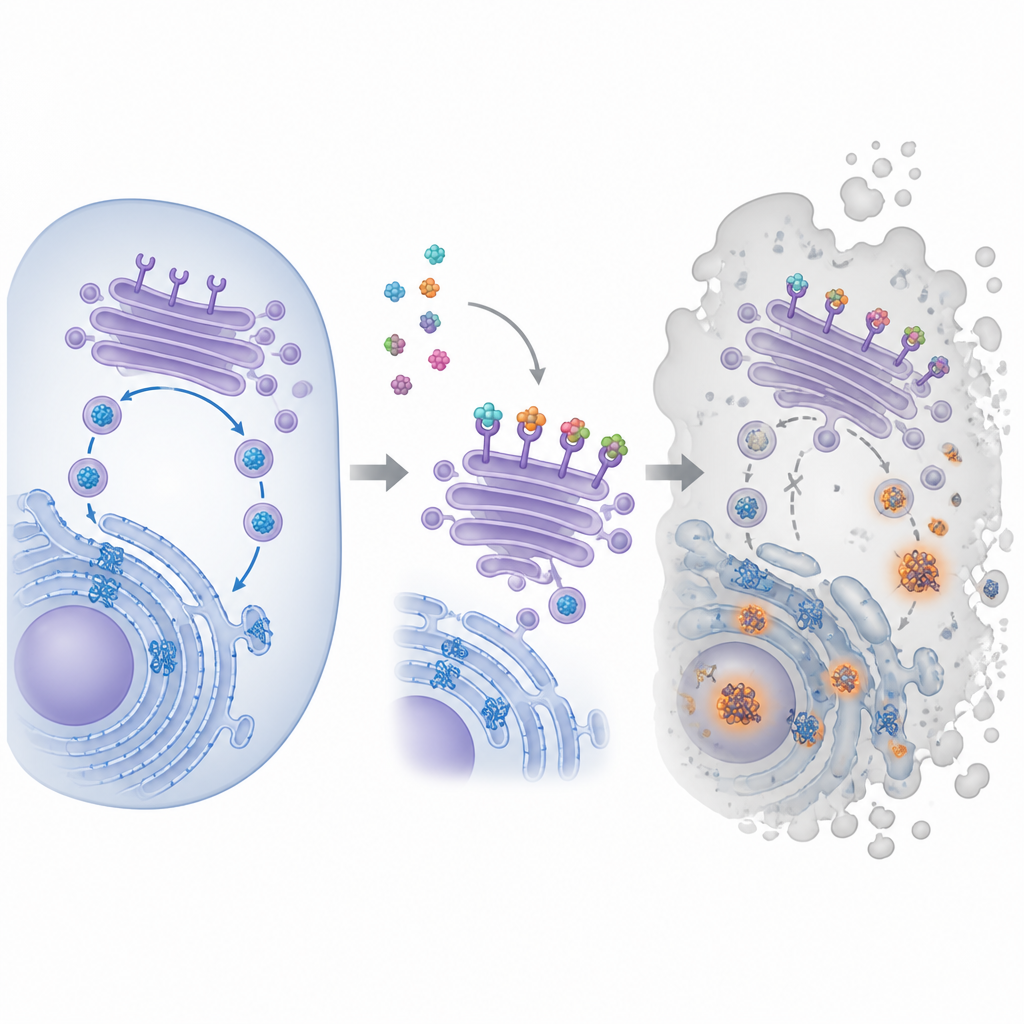
锁定大目标的小分子
这项工作的中心化合物称为pyra‑metho‑carnil,简称PMC,最初在天然产物库中被发现。早期研究显示PMC能抑制多种类型癌细胞的生长,即便这些细胞带有不同的基因突变或对其他药物有耐药性。但它在细胞内的主要靶点尚不清楚。为了解答这一点,研究者将PMC连接到磁性珠上,让其在癌细胞提取物中“钓”结合伙伴,随后鉴定被捕获的蛋白质。这一方法突出显示了一类称为KDEL受体的蛋白质家族,它们位于细胞的内部运输中心,帮助将某些伴侣蛋白检回到折叠区。
劫持细胞的回收通路
在细胞内,新合成的蛋白在被称为内质网的迷宫状结构中折叠,然后经过高尔基体——一组膜囊堆叠,用于分拣并将蛋白送往下游。KDEL受体在高尔基体巡逻,抓取尾部带有短标签的伴侣蛋白,将它们送回以便重复使用,从而维持折叠机械的能力。研究团队证明PMC能与人类已知的三种KDEL受体都结合,并改变它们在细胞中的定位。通过荧光标记,他们发现这些受体原本在高尔基体前侧聚集,但在PMC处理后错位。同时,一种特异染料显示出误折叠蛋白不断堆积,表明蛋白折叠与回收循环开始失效。
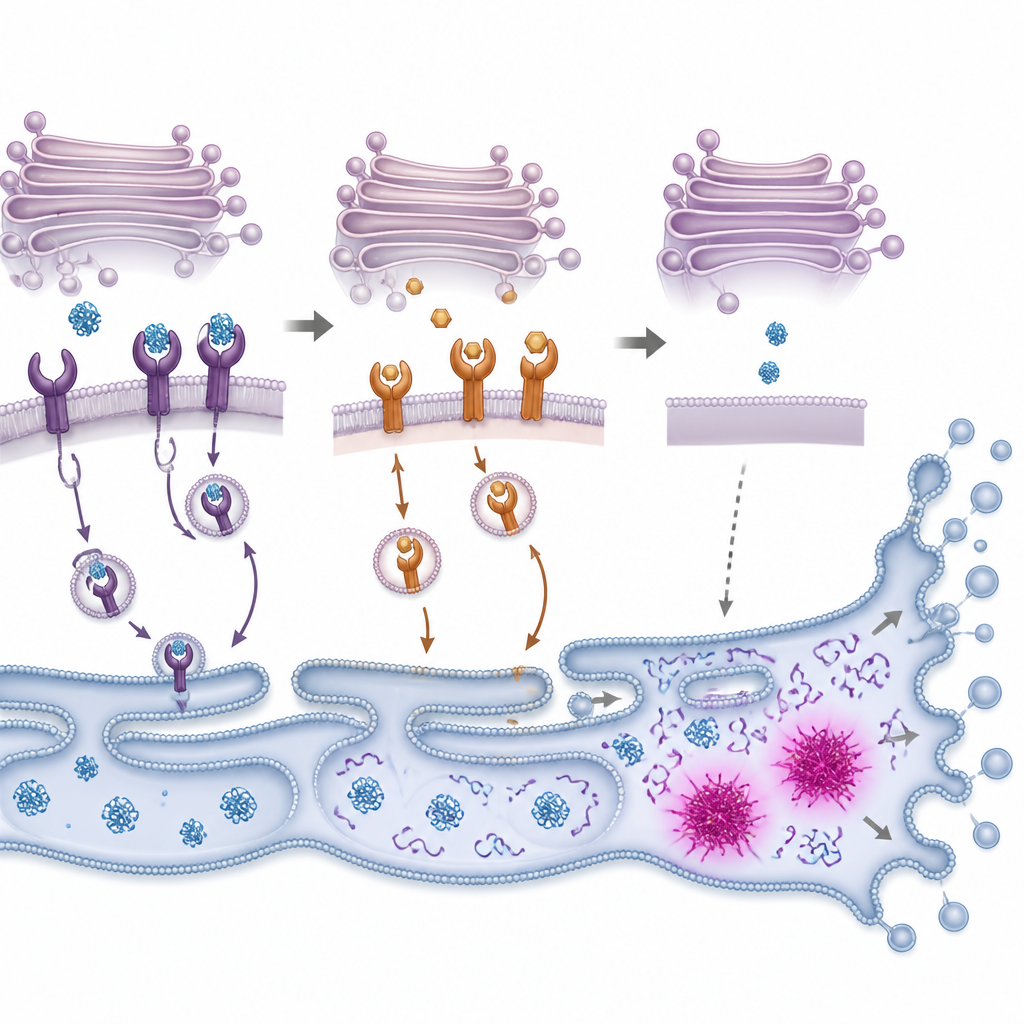
从蛋白质过载到细胞自杀
当误折叠蛋白积累时,细胞会启动一种通常称为未折叠蛋白反应的内部报警系统。该系统首先尝试通过减缓新蛋白合成并增强折叠与清除受损蛋白的能力来恢复平衡。研究人员观察到PMC在结肠癌细胞中迅速激活了该反应的关键部分,随后激活了在程序性细胞死亡过程中分解细胞组分的酶。阻断这些酶或降低一种名为CHOP的应激响应开关的水平,可使细胞在PMC暴露下更有可能存活,尽管并非完全存活。这表明PMC把细胞推过了一个临界点,使得应激缓解失败并启动自毁通路。
使癌细胞更易受应激攻击
团队还考察PMC是否能使癌细胞对其他形式的内部应激更加敏感。他们将低剂量、通常无害的PMC与扰乱钙稳态并常用于诱导内质网应激的化合物thapsigargin联合使用。两药合用比单用thapsigargin更强烈地抑制了细胞生长,应激标志物也升高,表明PMC降低了损伤阈值。为证明KDEL受体本身对该效应至关重要,科学家们使用小RNA分子直接下调这些受体。仅此操作就能触发应激反应并以类似方式减缓癌细胞生长。
这对未来癌症治疗意味着什么
总体而言,研究表明PMC通过结合KDEL受体、扰乱其定位与功能,从而破坏细胞维持其蛋白质清单的能力。癌细胞本已接近其蛋白质处理能力的极限,因而对这类干扰尤为敏感,容易被推向程序性死亡。尽管还需要在动物体内的进一步研究和安全性测试,结果表明KDEL受体及相关的蛋白质应激通路是开发新型抗癌药物以及与现有应激类疗法组合的有希望切入点。
引用: Yoshida, K., Nishi, K., Kitaguchi, T. et al. Pyra-metho-carnil disrupts cancer cell proteostasis and induces apoptosis by binding to KDEL receptors. Sci Rep 16, 15145 (2026). https://doi.org/10.1038/s41598-026-45604-z
关键词: 癌细胞, 蛋白质折叠, 内质网应激, KDEL受体, 凋亡