Clear Sky Science · tr
Pyra-metho-carnil, KDEL reseptörlerine bağlanarak kanser hücresi proteostasini bozar ve apoptozu indükler
Kanserin Protein Fabrikalarını Kendi Aleyhine Çevirmek
Kanser hücreleri hızla büyür ve hücre içinde dikkatle katlanıp taşınması gereken büyük miktarlarda protein üretir. Bu çalışma, iç taşıma sistemine bir taş koyan ve hasarlı proteinlerle kanser hücrelerini aşırı yükleyip kendilerini yok etmeye zorlayan küçük bir molekülü inceliyor; aynı zamanda tümörleri hedeflemede yeni bir yol işaret ediyor.
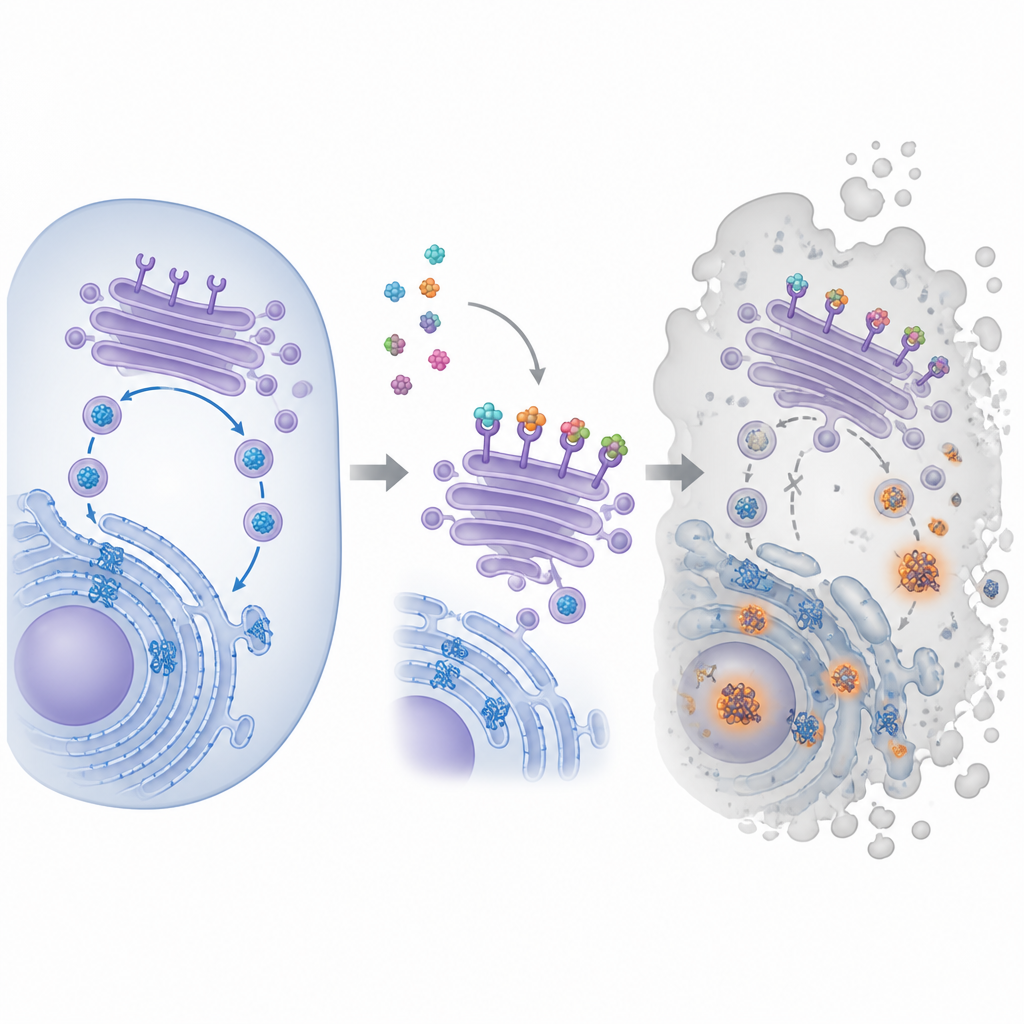
Büyük Hedefe Sahip Küçük Bir Molekül
Bu çalışmanın merkezindeki bileşik, pyra-metho-carnil veya kısaca PMC olarak adlandırılıyor ve doğal ürün kütüphanesinde keşfedilmiş. Daha önceki çalışmalar PMC'nin, farklı genetik değişikliklere sahip veya diğer ilaçlara dirençli olsa bile birçok kanser hücresinin büyümesini yavaşlattığını göstermişti. Ancak hücre içindeki başlıca hedefi bilinmiyordu. Bunu belirlemek için araştırmacılar PMC'yi manyetik boncuklara bağlayıp kanser hücresi özütlerinde bağlanan ortakları ‘avladılar’ ve yakalanan proteinleri tanımladılar. Bu yaklaşım, hücrenin iç taşıma merkezinde yer alan ve bazı yardımcı proteinleri katlanma bölmesine geri getirmeye yardımcı olan KDEL reseptörleri ailesini öne çıkardı.
Hücresel Geri Dönüşüm Yolunu Ele Geçirme
Hücre içinde yeni proteinler, endoplazmik retikulum adı verilen labirentimsi yapıda katlanır, sonra Golgi adı verilen zar ceplerinden oluşan istifin içinden geçip sınıflandırılır ve gönderilir. KDEL reseptörleri Golgi'yi devriye gezerek kuyruklarında kısa bir etiket taşıyan yardımcı proteinleri yakalar ve bunları yeniden kullanım için geri gönderir, böylece katlanma makinesi ayakta kalabilir. Araştırma ekibi PMC'nin bilinen üç insan KDEL reseptörünün tamamına bağlandığını ve bunların hücre içindeki yerleşimini değiştirdiğini gösterdi. Floresan etiketler kullanılarak, reseptörlerin normalde Golgi'nin ön yüzünde kümelendiği gözlenirken, PMC tedavisi sonrasında yerlerinin değiştiği bulundu. Aynı zamanda özel bir boya, katlanmamış protein kümelerinin büyüdüğünü ortaya koydu; bu da protein katlanma ve geri dönüşüm döngüsünün bozulmaya başladığını işaret etti.
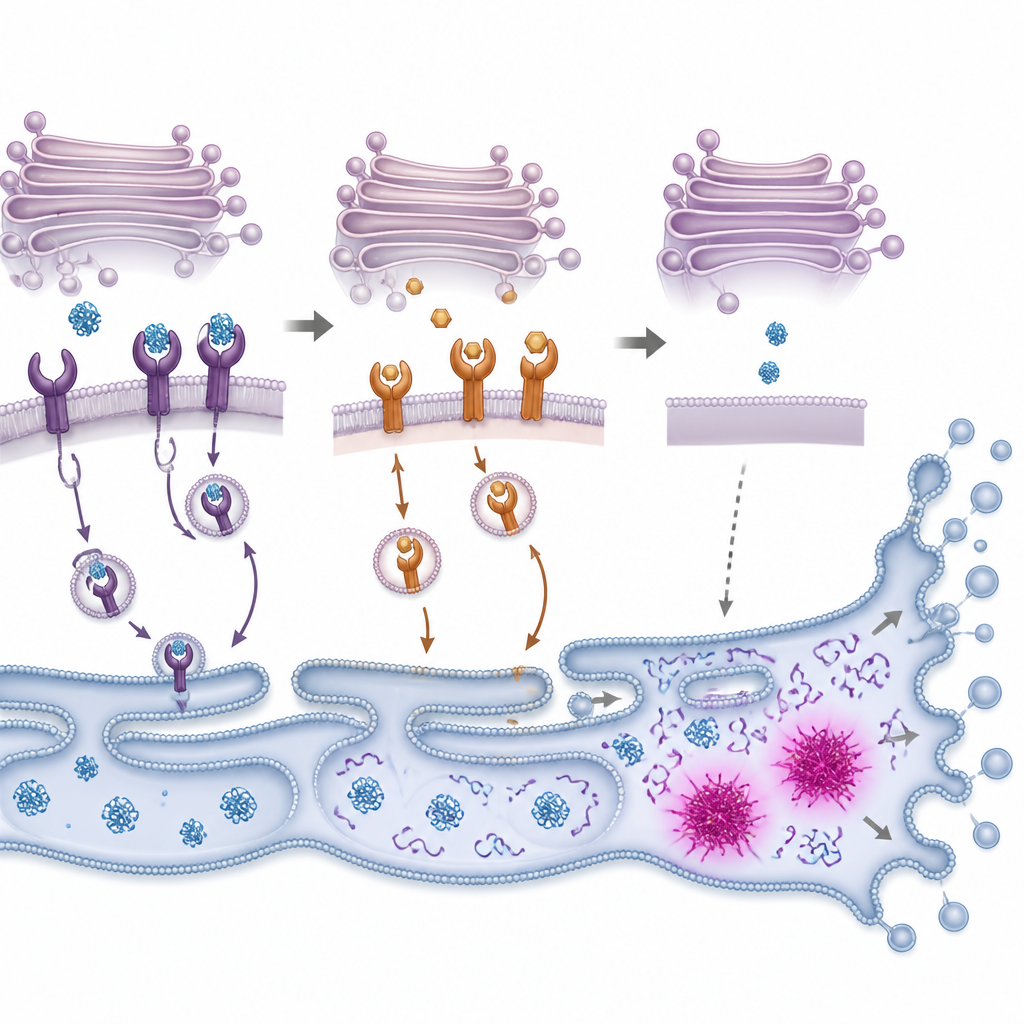
Protein Aşırı Yükünden Hücre İntiharına
Katlanmamış proteinler biriktiğinde, hücreler genellikle açığa çıkan protein yanıtı olarak adlandırılan içsel bir alarm sistemini devreye sokar. Bu sistem önce dengeyi yeniden sağlamak için yeni protein üretimini yavaşlatmaya ve hasarlı proteinleri katlayıp temizleme kapasitesini artırmaya çalışır. Araştırmacılar PMC'nin kolon kanseri hücrelerinde bu yanıtın kilit bileşenlerini hızla açtığını, ardından programlı hücre ölümünde hücresel bileşenleri parçalayan enzimlerin aktive olduğunu gözlemledi. Bu enzimleri engellemek veya CHOP adı verilen stres yanıtı anahtarını azaltmak, hücrelerin PMC'ye maruz kalınca hayatta kalma olasılığını artırdı, ancak tamamen kurtarmadı. Bu, PMC'nin hücreleri stresin giderilemediği ve kendi kendini yok etme yollarının devreye girdiği bir eşik noktasını aşmaya ittiğini gösteriyor.
Kanser Hücrelerini Strese Karşı Daha Kırılgan Hale Getirmek
Araştırmacılar ayrıca PMC'nin kanser hücrelerini diğer içsel stres türlerine karşı daha hassas hâle getirip getirmeyeceğini de sordular. Zararsız düzeyde düşük bir PMC dozu, kalsiyum düzenlemesini bozan ve protein katlanma bölmesinde stresi provake etmek için yaygın olarak kullanılan thapsigargin ile birlikte uygulandı. İki ilaç birlikte hücre büyümesini thapsigargin tek başına olduğundan daha güçlü şekilde baskıladı ve stres belirteçleri daha yüksek düzeye çıktı; bu, PMC'nin hasar için eşik değerini düşürdüğünü gösteriyor. Etkinin merkezinde gerçekten KDEL reseptörlerinin olduğunu göstermek için bilim insanları bu reseptörlerin düzeyini doğrudan azaltmak üzere küçük RNA molekülleri kullandı. Bu müdahale tek başına da benzer şekilde stres yanıtını tetikledi ve kanser hücresi büyümesini yavaşlattı.
Gelecekteki Kanser Tedavileri İçin Anlamı
Genel olarak çalışma, PMC'nin KDEL reseptörlerine bağlanarak bu reseptörlerin konumunu ve işlevini bozduğunu ve böylece hücrenin protein envanterini düzenleme yeteneğini sabote ettiğini öne sürüyor. Zaten protein işleme kapasitelerinin sınırına yakın çalışan kanser hücreleri, bu tür bir bozulmaya özellikle duyarlı görünmekte ve programlı hücre ölümüne itilebilmektedir. Hayvan çalışmalarına ve güvenlik testlerine ihtiyaç olmakla birlikte, bulgular KDEL reseptörlerini ve ilişkili protein stres yollarını yeni kanser ilaçları için ve mevcut stres temelli tedavileri daha etkili kılacak kombinasyonlar için umut verici hedefler olarak işaret ediyor.
Atıf: Yoshida, K., Nishi, K., Kitaguchi, T. et al. Pyra-metho-carnil disrupts cancer cell proteostasis and induces apoptosis by binding to KDEL receptors. Sci Rep 16, 15145 (2026). https://doi.org/10.1038/s41598-026-45604-z
Anahtar kelimeler: kanser hücreleri, protein katlanması, endoplazmik retikulum stresi, KDEL reseptörleri, apoptoz