Clear Sky Science · sv
Pyra-metho-carnil stör cancercellers proteostas och inducerar apoptos genom bindning till KDEL-receptorer
Att vända cancerens proteinfabriker mot sig själva
Cancerceller växer snabbt och producerar enorma mängder proteiner, som måste veckas och skickas vidare inne i cellen med stor omsorg. Denna studie undersöker en liten molekyl som sätter käppar i hjulet för det interna transport- och återvinningssystemet, överbelastar cancerceller med skadade proteiner tills de självdestruerar, och pekar samtidigt på en ny väg för att angripa tumörer.
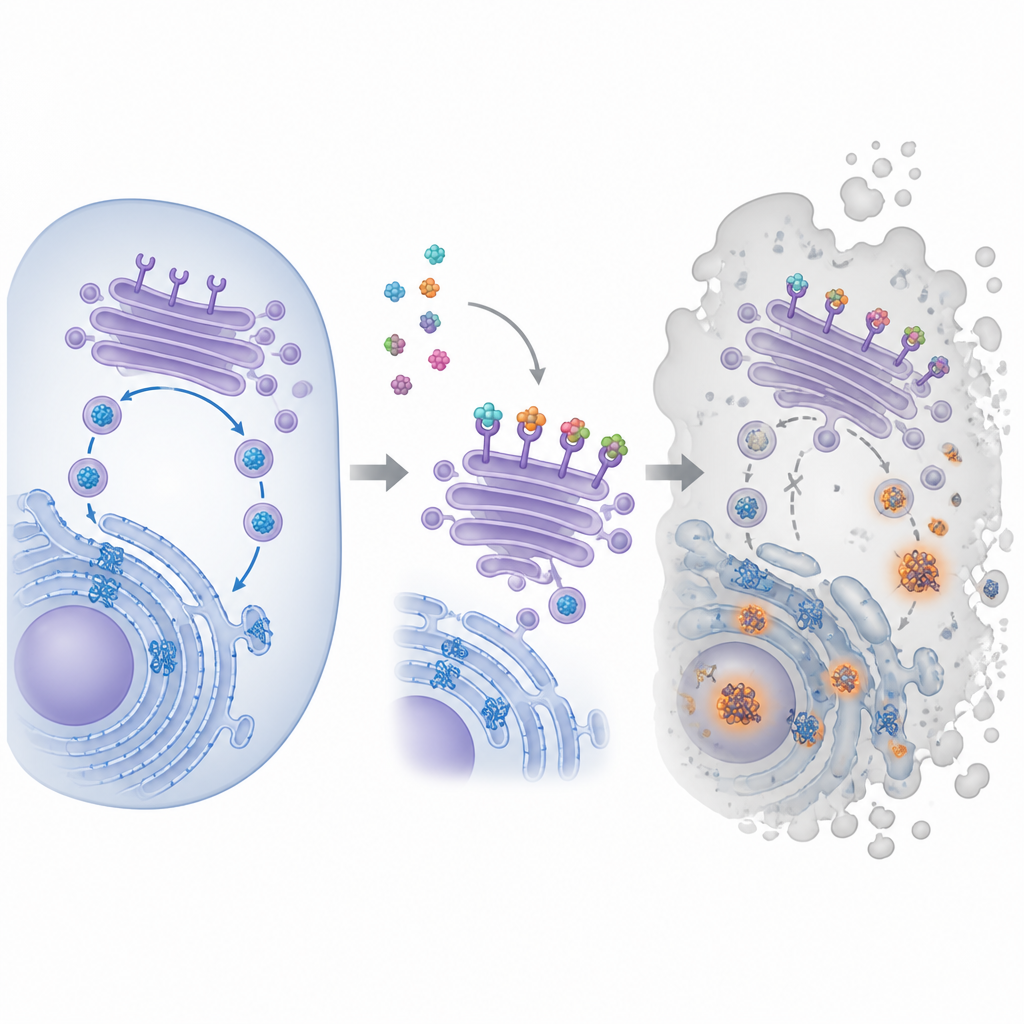
En liten molekyl med ett stort mål
Föreningen i centrum för arbetet kallas pyra-metho-carnil, eller PMC, och upptäcktes ursprungligen i ett bibliotek av naturprodukter. Tidigare studier visade att PMC bromsar tillväxten hos många typer av cancerceller, även när de bär olika genetiska mutationer eller är resistenta mot andra läkemedel. Dess huvudsakliga cellulära mål var dock okänt. För att hitta det fäste forskarna PMC på magnetiska pärlor, lät dem ”fiska” efter bindningspartners i extrakt från cancerceller och identifierade sedan de uppfångade proteinerna. Denna strategi framhävde en proteinfamilj känd som KDEL-receptorer, som sitter i cellens interna transportnav och hjälper till att hämta tillbaka vissa hjälpproteiner till veckningskompartmentet.
Kapning av cellens återvinningsrutt
Inne i cellerna veckas nya proteiner i en labyrintliknande struktur kallad det endoplasmatiska retiklet och passerar sedan genom Golgi, en stapel av membranblåsor som sorterar och skickar dem vidare. KDEL-receptorer patrullerar Golgi och fångar upp hjälpproteiner som bär en kort tagg i slutet, för att skicka dem tillbaka för återanvändning så att veckningsmaskineriet kan hänga med. Forskarna visade att PMC binder till alla tre kända mänskliga KDEL-receptortyper och förändrar deras lokalisering i cellerna. Med fluorescerande taggar fann de att receptorer som normalt var samlade på Golgis framsida förflyttades ur position efter PMC-behandling. Samtidigt visade ett speciellt färgämne växande klumpar av felveckade proteiner, vilket signalerade att looparna för proteinveckning och återvinning började fallera.
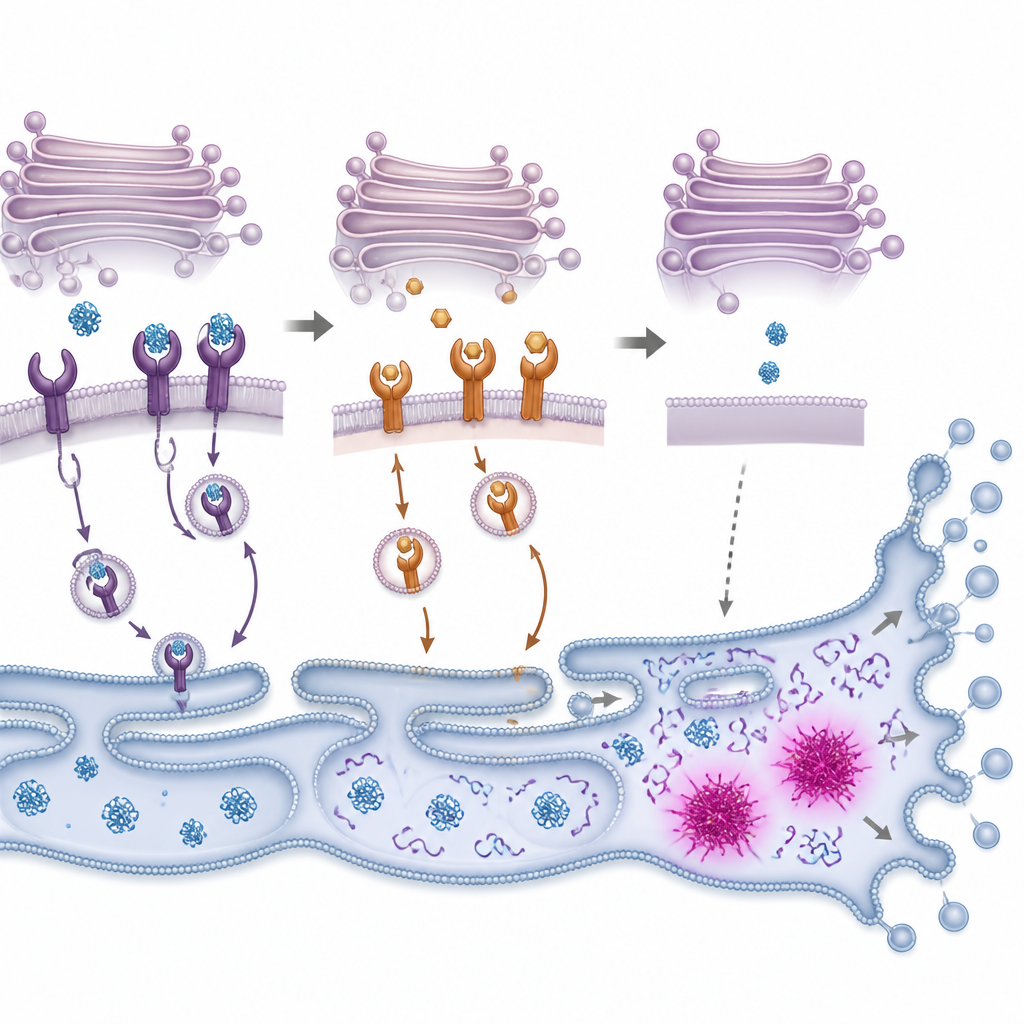
Från proteinöverbelastning till cellsjälvmord
När felveckade proteiner staplas upp slår cellen på ett internt larmssystem ofta kallat den ofullständigt veckade proteiners svar, eller unfolded protein response. Detta system försöker först återställa balansen genom att bromsa ny proteinsyntes och öka kapaciteten att vecka och rensa skadade proteiner. Forskarna observerade att PMC snabbt aktiverade centrala delar av denna respons i koloncancerceller, följt av aktivering av enzymer som bryter ned cellulära komponenter under programmerad celldöd. Att blockera dessa enzymer, eller att sänka nivåerna av en stressresponsiv reglagefaktor kallad CHOP, gjorde cellerna mer benägna att överleva PMC-exponering, om än inte helt. Detta tyder på att PMC pressar cellerna förbi en tipping point där stresslindring misslyckas och självdestruktiva vägar tar över.
Gör cancerceller mer sårbara för stress
Forskarna undrade också om PMC kunde göra cancerceller mer känsliga för andra former av intern stress. De kombinerade en låg, i övrigt ofarlig dos PMC med thapsigargin, en förening som stör kalciumhantering och ofta används för att framkalla stress i proteinveckningskompartmentet. Tillsammans undertryckte de två drogerna celltillväxten starkare än thapsigargin ensamt, och stressmarkörer steg mer, vilket indikerar att PMC sänker tröskeln för skada. För att visa att KDEL-receptorerna i sig är centrala för denna effekt använde forskarna små RNA-molekyler för att direkt minska dessa receptorers nivåer. Den manipulationen ensam utlöste stressresponsen och bromsade cancercellstillväxt på liknande sätt.
Vad detta kan innebära för framtida cancerbehandlingar
Sammanfattningsvis tyder studien på att PMC verkar genom att binda till KDEL-receptorer, störa deras lokalisering och funktion, och därigenom sabotera cellens förmåga att hålla ordning på sitt proteinlager. Cancerceller, som redan opererar nära gränsen för sin kapacitet att hantera proteiner, verkar särskilt sårbara för denna typ av störning och kan pressas in i programmerad celldöd. Medan ytterligare djurstudier och säkerhetstester krävs pekar resultaten på KDEL-receptorer och relaterade proteinstressvägar som lovande ingångspunkter för nya cancerläkemedel och för kombinationer som gör befintliga stressbaserade behandlingar mer effektiva.
Citering: Yoshida, K., Nishi, K., Kitaguchi, T. et al. Pyra-metho-carnil disrupts cancer cell proteostasis and induces apoptosis by binding to KDEL receptors. Sci Rep 16, 15145 (2026). https://doi.org/10.1038/s41598-026-45604-z
Nyckelord: cancerceller, proteinfoldning, stress i det endoplasmatiska retiklet, KDEL-receptorer, apoptos