Clear Sky Science · ja
ピラ‑メトホ‑カルニルはKDEL受容体に結合してがん細胞のプロテオスタシスを乱しアポトーシスを誘導する
がんのタンパク質工場を逆手に取る
がん細胞は急速に増殖し大量のタンパク質を生産するため、それらを注意深く折りたたみ細胞内で送り出す必要がある。本研究は、その内部輸送システムに楔を打ち込み、損傷したタンパク質でがん細胞を過負荷にして自己崩壊させる小分子を探り、腫瘍を狙う新たな手法を示唆している。
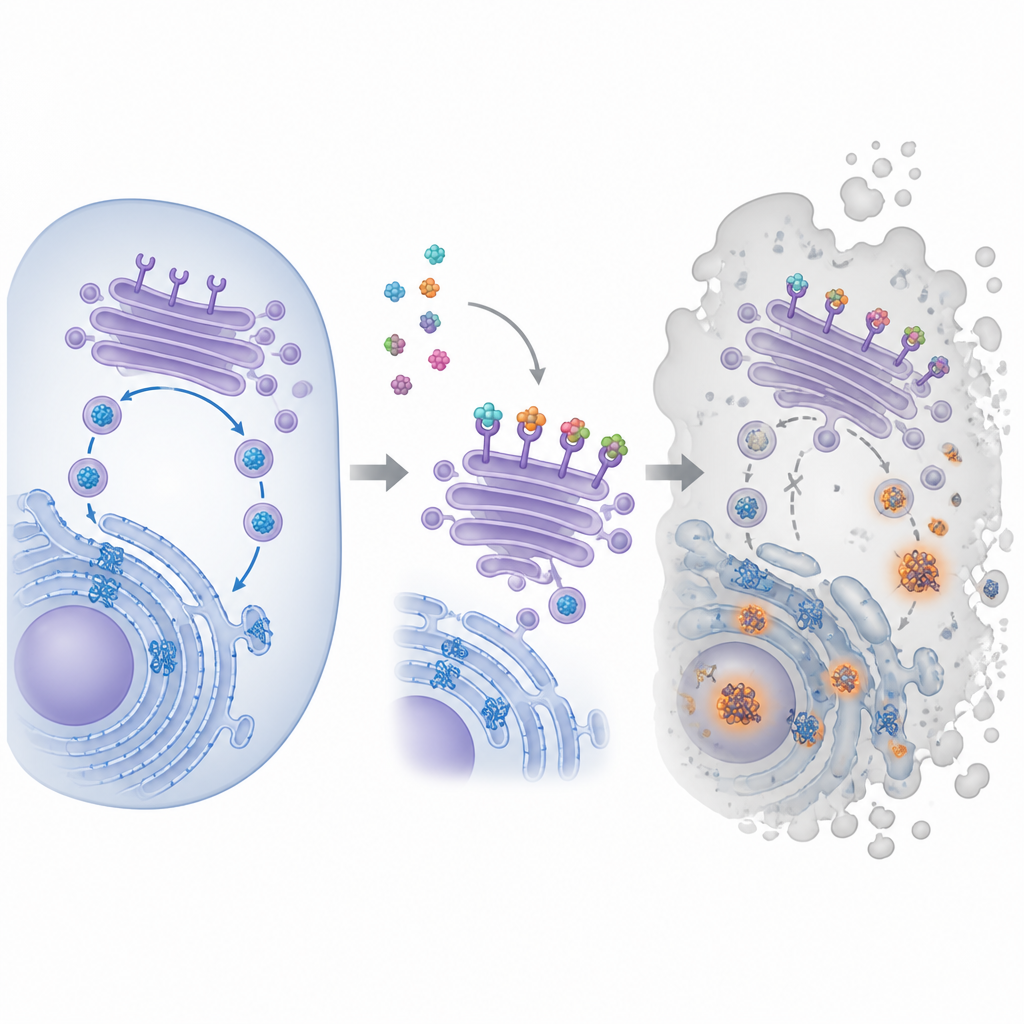
大きな標的を持つ小さな分子
本研究の中心にある化合物はピラ‑メトホ‑カルニル(PMC)と呼ばれ、天然物ライブラリから見いだされた。以前の研究では、PMCはさまざまな遺伝的変異を持つ、あるいは他の薬剤に耐性を示すがん細胞でも増殖を遅らせることが示されていたが、その主な細胞内標的は不明だった。標的を突き止めるため、研究者らはPMCを磁性ビーズに結合させ、がん細胞抽出液中で結合パートナーを漁らせ、捕捉したタンパク質を同定した。この手法により、細胞内の輸送ハブに位置し折りたたみ補助タンパク質を回収するKDEL受容体ファミリーが浮かび上がった。
細胞のリサイクル経路を乗っ取る
細胞内では、新生タンパク質は小胞体と呼ばれる迷路状の構造で折りたたまれ、その後ゴルジ体という膜シート群を通過して仕分け・送付される。KDEL受容体はゴルジで巡回し、末端に短いタグを持つ補助タンパク質をつかんで折りたたみ区画へ送り返し、折りたたみ機構の再利用を助ける。チームはPMCがヒトの既知の3種のKDEL受容体すべてに結合し、それらの細胞内局在を変えることを示した。蛍光標識を用いると、本来ゴルジの前面に集まる受容体がPMC処理後に位置をずらしたことが観察された。同時に、特別な染料で誤って折りたたまれたタンパク質の塊が増えていることが明らかになり、タンパク質の折りたたみとリサイクルのループが破綻し始めていることを示した。
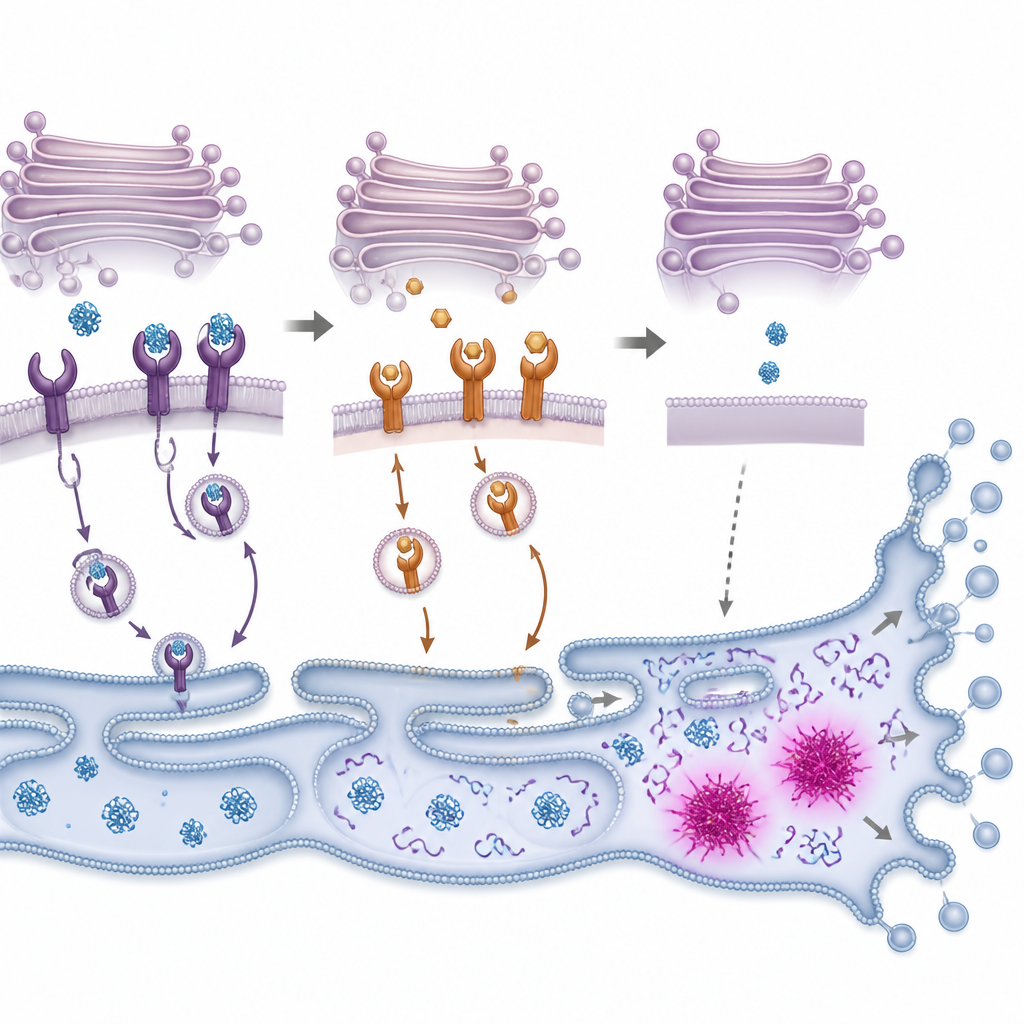
タンパク質過負荷から細胞自殺へ
誤った折りたたみタンパク質が蓄積すると、細胞は一般に小胞体ストレス応答(アンフォールドプロテインレスポンス)と呼ばれる内部警報システムを起動する。このシステムはまず新たなタンパク質合成を抑え、損傷タンパク質を折りたたみ・除去する能力を高めてバランス回復を図る。研究者らはPMCが大腸がん細胞でこの応答の主要経路を速やかに活性化し、その後プログラム細胞死の過程で細胞構成要素を切断する酵素群が活性化されるのを確認した。これらの酵素を阻害するか、ストレス応答性のスイッチであるCHOPの量を減らすと、PMC曝露後に細胞が生き残りやすくなるが完全ではなかった。これはPMCがストレス緩和が失敗する閾値を越えて細胞を押し込み、自己破壊経路が優勢になることを示唆する。
がん細胞のストレス感受性を高める
チームはまた、PMCが他の内部ストレスに対してがん細胞をどれだけ感受性化するかを調べた。低用量で単独ではほとんど無害なPMCと、カルシウム処理を乱して小胞体ストレスを誘発することで広く用いられるサプシガージンを組み合わせると、両者は単独のサプシガージンより強く細胞増殖を抑制し、ストレス指標もより高く上昇した。これはPMCが損傷の閾値を下げることを示す。さらにKDEL受容体自体がこの効果の中心であることを示すため、研究者らは小さなRNA分子を用いてこれら受容体を直接減らした。その操作だけでストレス応答が誘導され、がん細胞の増殖が同様に遅延した。
今後のがん治療にとっての意義
総じて、本研究はPMCがKDEL受容体に結合してそれらの局在と機能を乱し、細胞がタンパク質の在庫を整える能力を破壊することで作用することを示唆している。すでにタンパク質処理能力の限界近くで動作しているがん細胞は、この種の攪乱に特に脆弱であり、プログラム細胞死へと追い込まれ得る。今後、動物実験や安全性評価が必要だが、KDEL受容体や関連するタンパク質ストレス経路は新規抗がん薬や既存のストレスベース治療を増強する組み合わせ戦略の有望な標的であることを示している。
引用: Yoshida, K., Nishi, K., Kitaguchi, T. et al. Pyra-metho-carnil disrupts cancer cell proteostasis and induces apoptosis by binding to KDEL receptors. Sci Rep 16, 15145 (2026). https://doi.org/10.1038/s41598-026-45604-z
キーワード: がん細胞, タンパク質折りたたみ, 小胞体ストレス, KDEL受容体, アポトーシス