Clear Sky Science · ar
بيرا‑ميثو‑كارنيل يعطل توازن البروتين في الخلايا السرطانية ويحفز الاستماتة عبر ارتباطه بمستقبلات KDEL
تحويل مصانع البروتين السرطانية ضد نفسها
تنمو الخلايا السرطانية بسرعة وتنتج كميات هائلة من البروتينات، التي يجب طيّها وشحنها داخل الخلية بعناية. تستكشف هذه الدراسة جزيئًا صغيرًا يعطل ذلك النظام الداخلي للشحن، فيغمر الخلايا السرطانية ببروتينات تالفة حتى تدمر نفسها، بينما يشير إلى نهج جديد لاستهداف الأورام.
جزيء صغير له هدف كبير
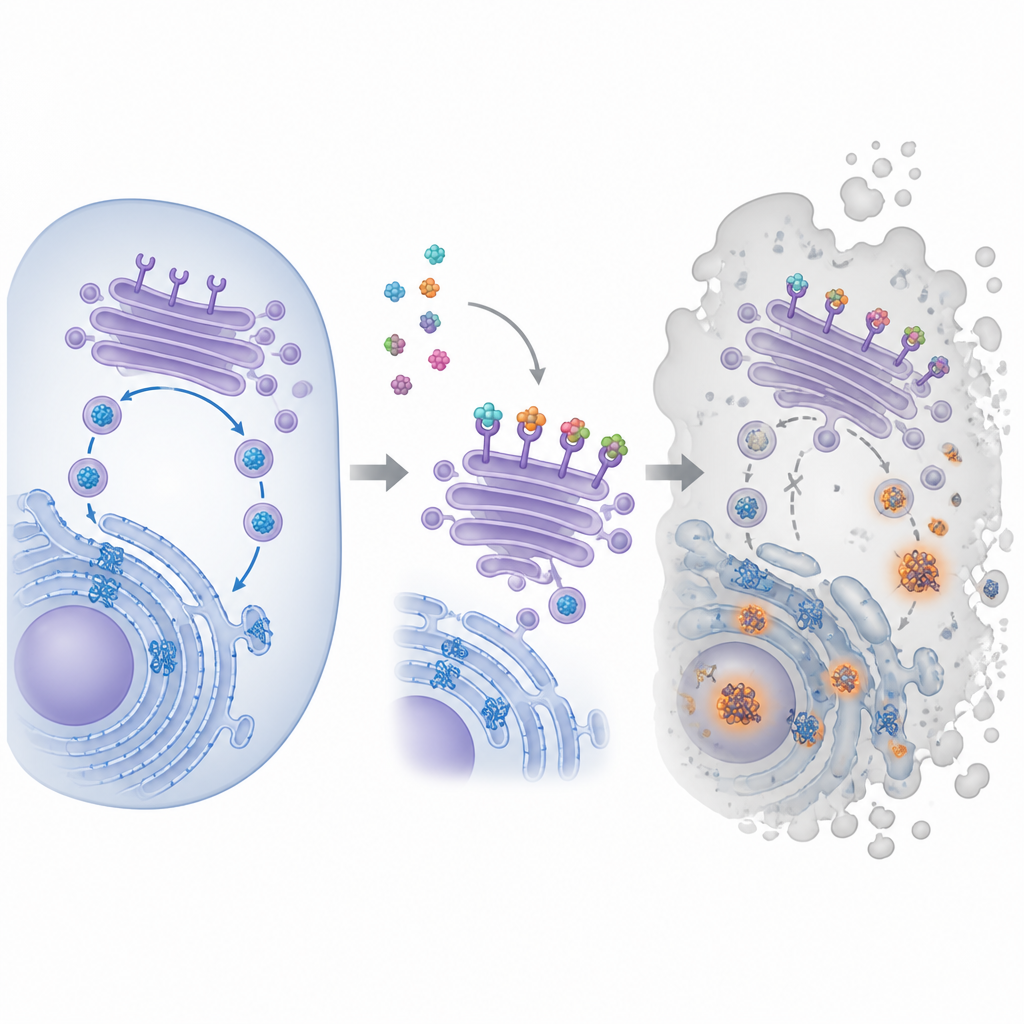
المركب المحوري في هذا العمل يسمى بيرا‑ميثو‑كارنيل، أو PMC، وُجد أصلاً في مكتبة منتجات طبيعية. أظهرت دراسات سابقة أن PMC يبطئ نمو أنواع عديدة من الخلايا السرطانية، حتى عندما تحمل طفرات جينية مختلفة أو مقاومة لأدوية أخرى. ومع ذلك، كان هدفه الرئيسي داخل الخلايا غير معروف. لتحديده، ربط الباحثون PMC بحبات مغناطيسية، وسمحوا لها بالاصطياد في مستخلصات خلايا سرطانية، ثم حددوا البروتينات المأسورة. أبرز هذا النهج عائلة من البروتينات تُعرف بمستقبلات KDEL، التي تقع في مركز الشحن الداخلي للخلية وتساعد في استرجاع بروتينات المساعدة إلى حجرة الطي.
اختطاف مسار إعادة التدوير في الخلية
داخل الخلايا، تُطوى البروتينات الجديدة في هيكل متشابك يسمى الشبكة الإندوبلازمية، ثم تمر عبر جهاز غولجي، سلسلة من الحويصلات الغشائية التي تفرزها وتُعيد توزيعها. تقوم مستقبلات KDEL بدوريات في الغولجي وتقبض على بروتينات المساعدة التي تحمل وسمًا قصيرًا في طرفها، وتعيدها للاستفادة مرة أخرى حتى يستمر نظام الطي. أظهر الفريق أن PMC يرتبط بأنواع مستقبلات KDEL البشرية الثلاثة المعروفة ويغير مواضعها داخل الخلايا. باستخدام وسمات فلورية، وجدوا أن المستقبلات التي كانت عادةً متجمعة في الجانب الأمامي من الغولجي تحركت من مكانها بعد علاج PMC. وفي الوقت نفسه، كشف صبغ خاص عن تكتلات متزايدة من البروتينات غير المطوية بشكل صحيح، مما يشير إلى أن حلقة طي البروتين وإعادة التدوير بدأت تفشل.
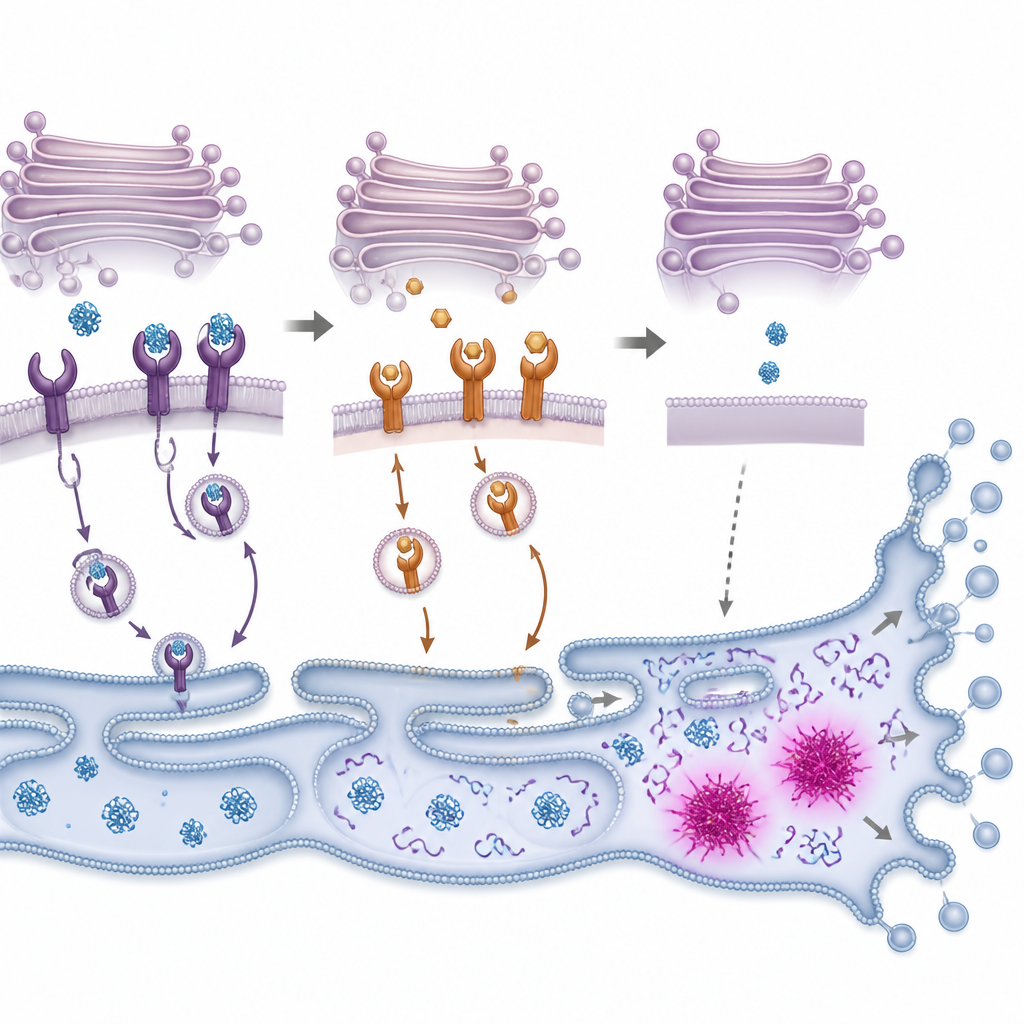
من تراكم البروتين إلى انتحار الخلية
عندما تتراكم البروتينات غير المطوية، تُشغّل الخلايا نظام إنذار داخلي يُسمى غالبًا استجابة البروتين غير المطوي. يحاول هذا النظام أولاً استعادة التوازن عن طريق إبطاء إنتاج البروتين الجديد وزيادة قدرة الطي وإزالة البروتينات التالفة. لاحظ الباحثون أن PMC فعّل بسرعة أجزاء رئيسية من هذه الاستجابة في خلايا سرطان القولون، تلتها تنشيط إنزيمات تقطع مكونات خلوية أثناء الموت المبرمج. إن حجب هذه الإنزيمات، أو خفض مستويات مفتاح استجابي للإجهاد يُدعى CHOP، جعل الخلايا أكثر احتمالًا للبقاء على قيد الحياة بعد تعرضها لـPMC، وإن لم يصبح البقاء كاملاً. ويقترح ذلك أن PMC يدفع الخلايا لما بعد نقطة الانقلاب حيث تفشل آليات تخفيف الإجهاد وتسيطر مسارات الانتحار الخلوية.
جعل الخلايا السرطانية أكثر عرضة للإجهاد
سأل الفريق أيضًا إن كان PMC يمكن أن يجعل الخلايا السرطانية أكثر حساسية لأشكال أخرى من الإجهاد الداخلي. جمعوا جرعة منخفضة من PMC، كانت غير ضارة بمفردها، مع ثابسجارجين، مركب يخل بتعامل الكالسيوم ويُستخدم على نطاق واسع لإثارة الإجهاد في حجرة طي البروتين. معًا، كبح الدواءان نمو الخلايا بقوة أكبر من ثابسجارجين وحده، وارتفعت مؤشرات الإجهاد أكثر، مشيرة إلى أن PMC يخفض العتبة للتلف. ولإظهار أن مستقبلات KDEL نفسها مركزية لهذا التأثير، استخدم العلماء جزيئات RNA صغيرة لتقليل هذه المستقبلات مباشرة. أدى هذا التدخل وحده إلى تحفيز استجابة الإجهاد وإبطاء نمو الخلايا السرطانية بطريقة مماثلة.
ما الذي قد يعنيه هذا لعلاجات السرطان المستقبلية
تُشير الدراسة إجمالًا إلى أن PMC يعمل عبر ارتباطه بمستقبلات KDEL، واضطراب موقعها ووظيفتها، وبالتالي تخريب قدرة الخلية على الحفاظ على نظام البروتين الخاص بها. تبدو الخلايا السرطانية، التي تعمل بالفعل بالقرب من حد قدرتها على معالجة البروتينات، أكثر عرضة لهذا النوع من الاضطراب ويمكن دفعها إلى الموت المبرمج. وعلى الرغم من الحاجة إلى مزيد من العمل في النماذج الحيوانية واختبارات السلامة، تشير النتائج إلى مستقبلات KDEL ومسارات إجهاد البروتين ذات الصلة كنقاط دخول واعدة لأدوية سرطانية جديدة ولتكوينات تُعزز فعالية العلاجات المعتمدة على الإجهاد.
الاستشهاد: Yoshida, K., Nishi, K., Kitaguchi, T. et al. Pyra-metho-carnil disrupts cancer cell proteostasis and induces apoptosis by binding to KDEL receptors. Sci Rep 16, 15145 (2026). https://doi.org/10.1038/s41598-026-45604-z
الكلمات المفتاحية: خلايا سرطانية, طَيّ البروتين, إجهاد الشبكة الإندوبلازمية, مستقبلات KDEL, الاستماتة