Clear Sky Science · fr
Pyra-metho-carnil perturbe la protéostasie des cellules cancéreuses et induit l'apoptose en se liant aux récepteurs KDEL
Retourner les usines à protéines du cancer contre elles-mêmes
Les cellules cancéreuses croissent rapidement et produisent d'immenses quantités de protéines, qui doivent être soigneusement repliées et dispatchées à l'intérieur de la cellule. Cette étude explore une petite molécule qui enraye ce système de distribution interne, surchargeant les cellules cancéreuses de protéines endommagées jusqu'à ce qu'elles s'autodétruisent, tout en ouvrant une nouvelle voie pour cibler les tumeurs.
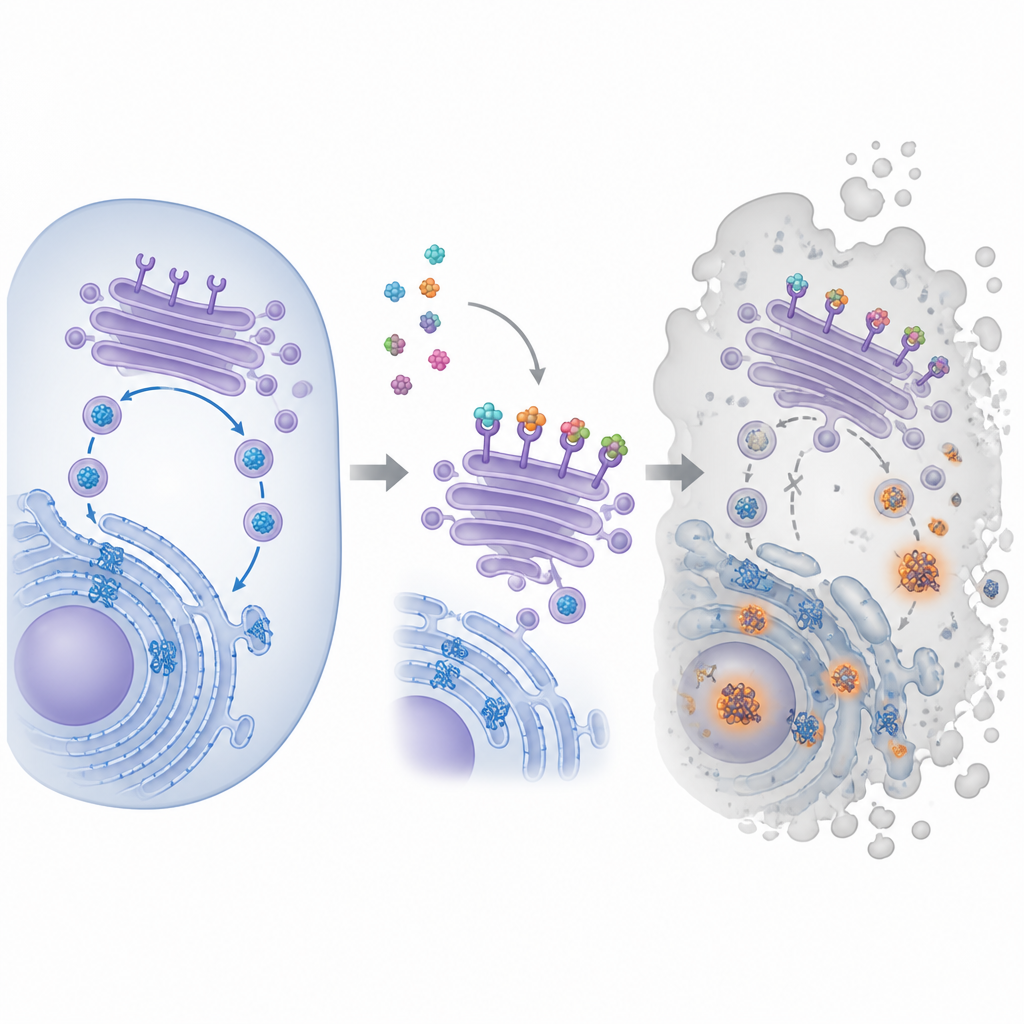
Une petite molécule, une cible majeure
Le composé au centre de ce travail s'appelle pyra‑metho‑carnil, ou PMC, découvert à l'origine dans une bibliothèque de produits naturels. Des études antérieures ont montré que le PMC ralentit la croissance de nombreux types de cellules cancéreuses, même lorsqu'elles portent des mutations génétiques différentes ou résistent à d'autres médicaments. Pourtant, sa cible principale à l'intérieur des cellules restait inconnue. Pour l'identifier, les chercheurs ont fixé le PMC à des billes magnétiques, l'ont utilisé pour pêcher des partenaires de liaison dans des extraits de cellules cancéreuses, puis ont identifié les protéines capturées. Cette approche a mis en évidence une famille de protéines connues sous le nom de récepteurs KDEL, qui se trouvent dans le centre de distribution interne de la cellule et aident à récupérer certaines protéines d'aide vers le compartiment de repliement.
Détourner la voie de recyclage de la cellule
À l'intérieur des cellules, les nouvelles protéines sont repliées dans une structure labyrinthique appelée réticulum endoplasmique, puis passent par le Golgi, une pile de poches membranaires qui trie et expédie les protéines. Les récepteurs KDEL patrouillent dans le Golgi et saisissent les protéines chaperonnes portant une courte étiquette à leur extrémité, les renvoyant pour réutilisation afin que la machinerie de repliement puisse suivre. L'équipe a montré que le PMC se lie aux trois types connus de récepteurs KDEL humains et modifie leur localisation dans la cellule. À l'aide de marquages fluorescents, ils ont constaté que des récepteurs normalement regroupés sur la face antérieure du Golgi se déplaçaient après le traitement au PMC. Simultanément, un colorant spécifique a révélé la formation croissante d'amas de protéines mal repliées, signe que la boucle de repliement et de recyclage commençait à faillir.
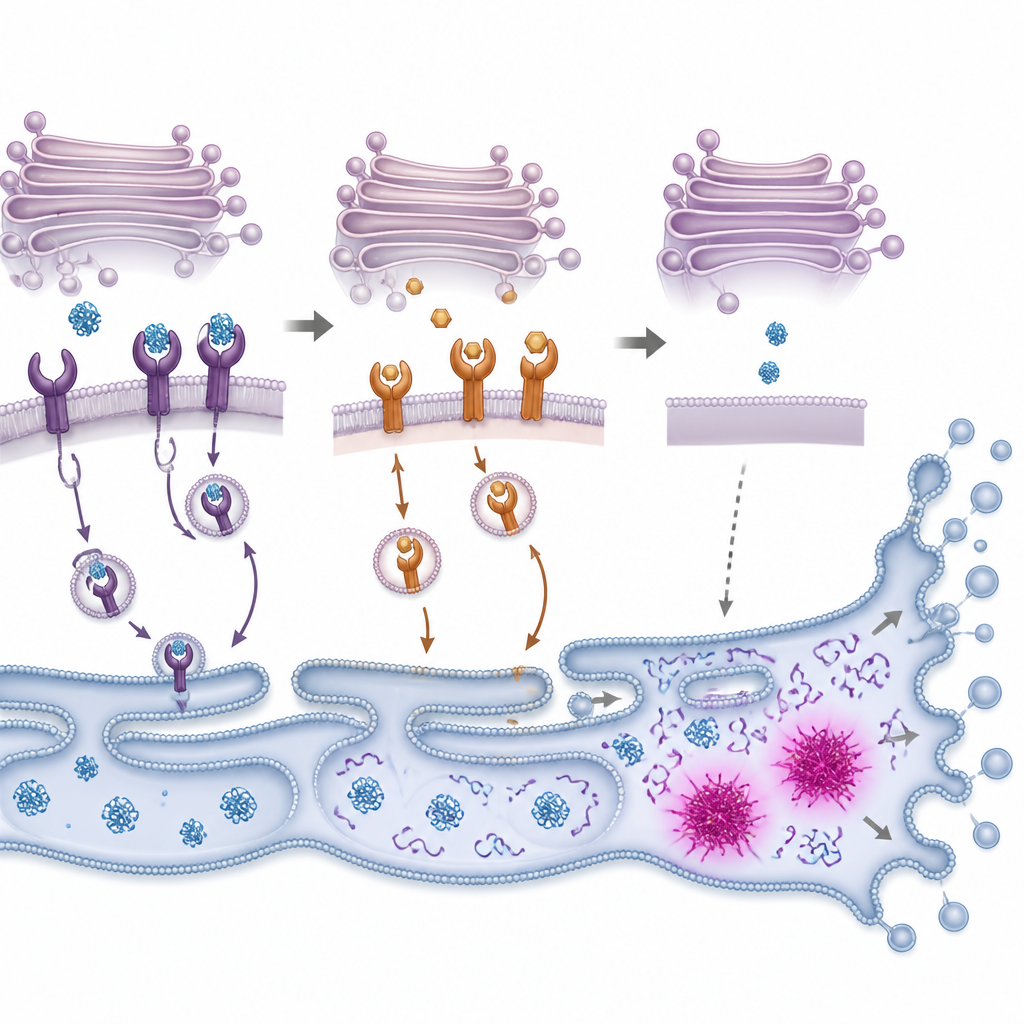
De la surcharge protéique au suicide cellulaire
Lorsque les protéines mal repliées s'accumulent, les cellules activent un système d'alarme interne souvent appelé réponse aux protéines non repliées. Ce système tente d'abord de rétablir l'équilibre en ralentissant la production de nouvelles protéines et en augmentant la capacité à replier et éliminer les protéines endommagées. Les chercheurs ont observé que le PMC activait rapidement des éléments clés de cette réponse dans des cellules de cancer du côlon, puis entraînait l'activation d'enzymes qui découpent les composants cellulaires lors de la mort programmée. Bloquer ces enzymes, ou diminuer les niveaux d'un commutateur sensible au stress nommé CHOP, rendait les cellules plus susceptibles de survivre à l'exposition au PMC, bien pas complètement. Cela suggère que le PMC pousse les cellules au-delà d'un point de basculement où la réparation du stress échoue et où les voies d'autodestruction prennent le relais.
Rendre les cellules cancéreuses plus vulnérables au stress
L'équipe a également testé si le PMC pouvait rendre les cellules cancéreuses plus sensibles à d'autres formes de stress interne. Ils ont combiné une faible dose de PMC, autrement inoffensive, avec la thapsigargine, un composé qui perturbe la gestion du calcium et est largement utilisé pour provoquer le stress du compartiment de repliement. Ensemble, les deux médicaments ont supprimé la croissance cellulaire plus fortement que la thapsigargine seule, et les marqueurs de stress ont augmenté davantage, indiquant que le PMC abaisse le seuil de tolérance aux dommages. Pour montrer que les récepteurs KDEL sont centraux dans cet effet, les scientifiques ont utilisé de petits ARN pour réduire directement ces récepteurs. Cette manipulation seule a déclenché la réponse au stress et ralenti la croissance des cellules cancéreuses de manière comparable.
Quelles implications pour les traitements futurs du cancer
Globalement, l'étude suggère que le PMC agit en se liant aux récepteurs KDEL, en perturbant leur localisation et leur fonction, et en sabotant ainsi la capacité de la cellule à maintenir l'ordre dans son inventaire protéique. Les cellules cancéreuses, qui opèrent déjà près de la limite de leur capacité de gestion des protéines, semblent particulièrement vulnérables à ce type de perturbation et peuvent être poussées vers la mort programmée. Bien que des travaux supplémentaires chez l'animal et des tests de sécurité soient nécessaires, les résultats désignent les récepteurs KDEL et les voies de stress protéique associées comme des points d'entrée prometteurs pour de nouveaux médicaments anticancéreux et pour des combinaisons rendant les traitements basés sur le stress plus efficaces.
Citation: Yoshida, K., Nishi, K., Kitaguchi, T. et al. Pyra-metho-carnil disrupts cancer cell proteostasis and induces apoptosis by binding to KDEL receptors. Sci Rep 16, 15145 (2026). https://doi.org/10.1038/s41598-026-45604-z
Mots-clés: cellules cancéreuses, repliement des protéines, stress du réticulum endoplasmique, récepteurs KDEL, apoptose