Clear Sky Science · nl
Pyra-metho-carnil verstoort proteostase van kankercellen en induceert apoptose door te binden aan KDEL-receptoren
Kankers eiwitfabrieken tegen zichzelf keren
Kankercellen groeien snel en produceren enorme hoeveelheden eiwitten, die zorgvuldig gevouwen en binnen de cel vervoerd moeten worden. Deze studie onderzoekt een kleine molecule die een gat in dat interne transportsysteem slaat, waardoor kankercellen overladen raken met beschadigde eiwitten totdat ze zichzelf afbreken, en die tegelijk wijst op een nieuwe manier om tumoren aan te pakken.
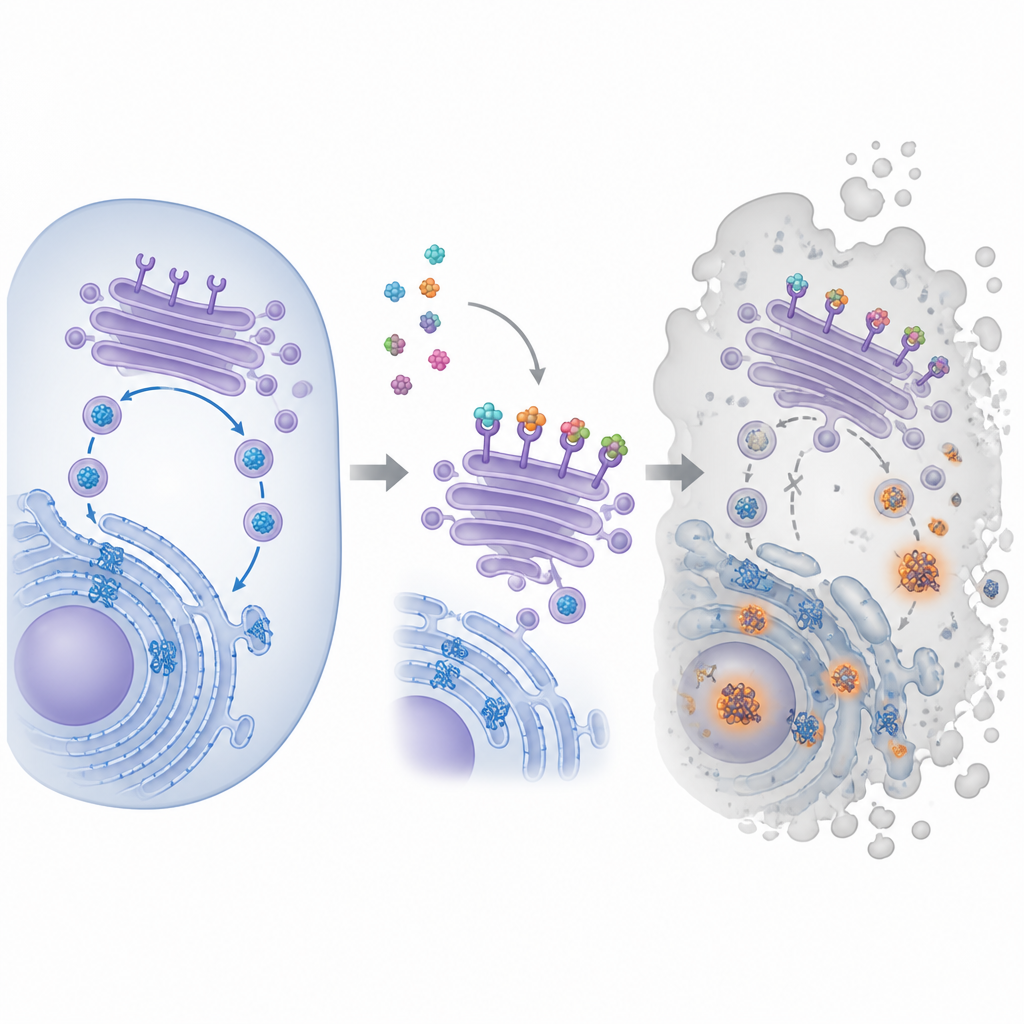
Een kleine molecule met een groot doelwit
De verbinding die centraal staat in dit werk heet pyra‑metho‑carnil, of PMC, oorspronkelijk gevonden in een bibliotheek van natuurlijke producten. Eerdere studies lieten zien dat PMC de groei van veel soorten kankercellen vertraagt, zelfs wanneer ze verschillende genetische mutaties dragen of resistent zijn tegen andere medicijnen. Toch was het belangrijkste intracellulaire doelwit onbekend. Om dat te achterhalen koppelden de onderzoekers PMC aan magnetische bolletjes, lieten die bindingspartners vissen in extracten van kankercellen en identificeerden vervolgens de gevangen eiwitten. Deze aanpak bracht een familie eiwitten aan het licht die bekendstaat als KDEL-receptoren, die in het interne transportcentrum van de cel zitten en helpen bepaalde hulp‑eiwitten terug te halen naar het vouwingcompartiment.
Het recyclagekanaal van de cel kapen
Binnenin cellen worden nieuwe eiwitten gevouwen in een doolhofachtige structuur die het endoplasmatisch reticulum heet, en passeren ze het Golgi‑apparaat, een stapel membraanblaasjes die sorteert en verder verzendt. KDEL-receptoren patrouilleren in de Golgi en grijpen hulp‑eiwitten met een kort merkje aan hun staart vast, zodat die worden teruggestuurd voor hergebruik en de vouwingmachine kan bijbenen. Het team toonde aan dat PMC aan alle drie de bekende menselijke KDEL-receptortypes bindt en verandert waar ze zich in de cel bevinden. Met fluorescerende merkers vonden ze dat receptoren die normaal geconcentreerd aan de voorzijde van de Golgi zitten, na PMC‑behandeling van hun plaats raakten. Tegelijkertijd liet een speciale kleurstof groeiende klonters van misgevouwen eiwitten zien, wat aangeeft dat de eiwitvouwing en het recyclingcircuit beginnen te falen.
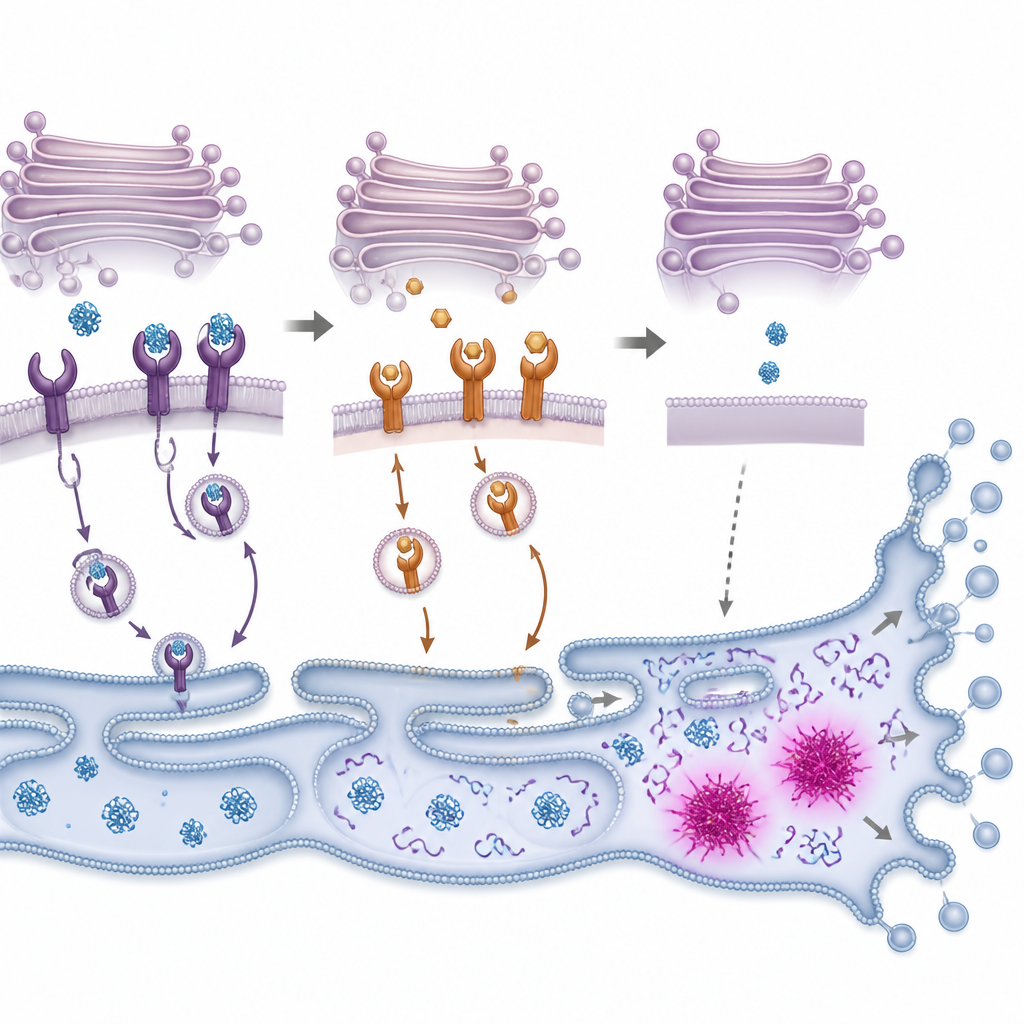
Van eiwitoverbelasting naar celsuïcide
Wanneer misgevouwen eiwitten zich ophopen, schakelen cellen een intern alarmsysteem in dat vaak de unfolded protein response wordt genoemd. Dit systeem probeert eerst het evenwicht te herstellen door de aanmaak van nieuwe eiwitten te vertragen en de capaciteit om beschadigde eiwitten te vouwen en te verwijderen te verhogen. De onderzoekers zagen dat PMC snel sleutelcomponenten van deze respons activeerde in colonkankercellen, gevolgd door activering van enzymen die cellulair materiaal afbreken tijdens geprogrammeerde celdood. Het blokkeren van deze enzymen, of het verlagen van de niveaus van een stressgevoelige schakelaar genaamd CHOP, maakte cellen eerder geneigd PMC te overleven, hoewel niet volledig. Dit suggereert dat PMC cellen voorbij een kantelpunt duwt waar stressverlichting faalt en zelfdestructie‑routes de overhand krijgen.
Kankercellen gevoeliger maken voor stress
Het team vroeg ook of PMC kankercellen gevoeliger kon maken voor andere vormen van interne stress. Ze combineerden een lage, op zichzelf onschadelijke dosis PMC met thapsigargin, een verbinding die de calciumhuishouding verstoort en veel wordt gebruikt om stress in het vouwingcompartiment uit te lokken. Samen onderdrukten de twee middelen de celgroei sterker dan thapsigargin alleen, en stegen stressmarkers hoger, wat aangeeft dat PMC de drempel voor schade verlaagt. Om te laten zien dat de KDEL-receptoren zelf centraal staan in dit effect, gebruikten de wetenschappers kleine RNA-moleculen om deze receptoren direct te verminderen. Die ingreep alleen activeerde de stressrespons en vertraagde de groei van kankercellen op vergelijkbare wijze.
Wat dit kan betekenen voor toekomstige kankerbehandelingen
Al met al suggereert de studie dat PMC werkt door te binden aan KDEL-receptoren, hun locatie en functie te verstoren en daarmee het vermogen van de cel om zijn eiwitvoorraad op orde te houden te saboteren. Kankercellen, die al dichtbij de limiet van hun eiwithanteringscapaciteit opereren, blijken bijzonder kwetsbaar voor dit soort verstoring en kunnen in geprogrammeerde celdood worden geduwd. Hoewel verder werk in dieren en veiligheidsonderzoek nodig is, wijzen de resultaten op KDEL-receptoren en verwante eiwitstresspaden als veelbelovende ingangswegen voor nieuwe kankergeneesmiddelen en voor combinaties die bestaande stressgebaseerde behandelingen effectiever maken.
Bronvermelding: Yoshida, K., Nishi, K., Kitaguchi, T. et al. Pyra-metho-carnil disrupts cancer cell proteostasis and induces apoptosis by binding to KDEL receptors. Sci Rep 16, 15145 (2026). https://doi.org/10.1038/s41598-026-45604-z
Trefwoorden: kankercellen, eiwitvouwing, endoplasmatisch reticulumstress, KDEL-receptoren, apoptose