Clear Sky Science · es
Pyra-metho-carnil interrumpe la proteostasis de células cancerosas e induce apoptosis al unirse a los receptores KDEL
Volviendo las fábricas de proteínas del cáncer contra sí mismas
Las células cancerosas crecen rápidamente y producen enormes cantidades de proteínas, que deben plegarse y distribuirse cuidadosamente dentro de la célula. Este estudio explora una pequeña molécula que introduce un problema en ese sistema interno de envío, sobrecargando a las células cancerosas con proteínas dañadas hasta que se autodestruyen, y apunta a una nueva forma de atacar los tumores.
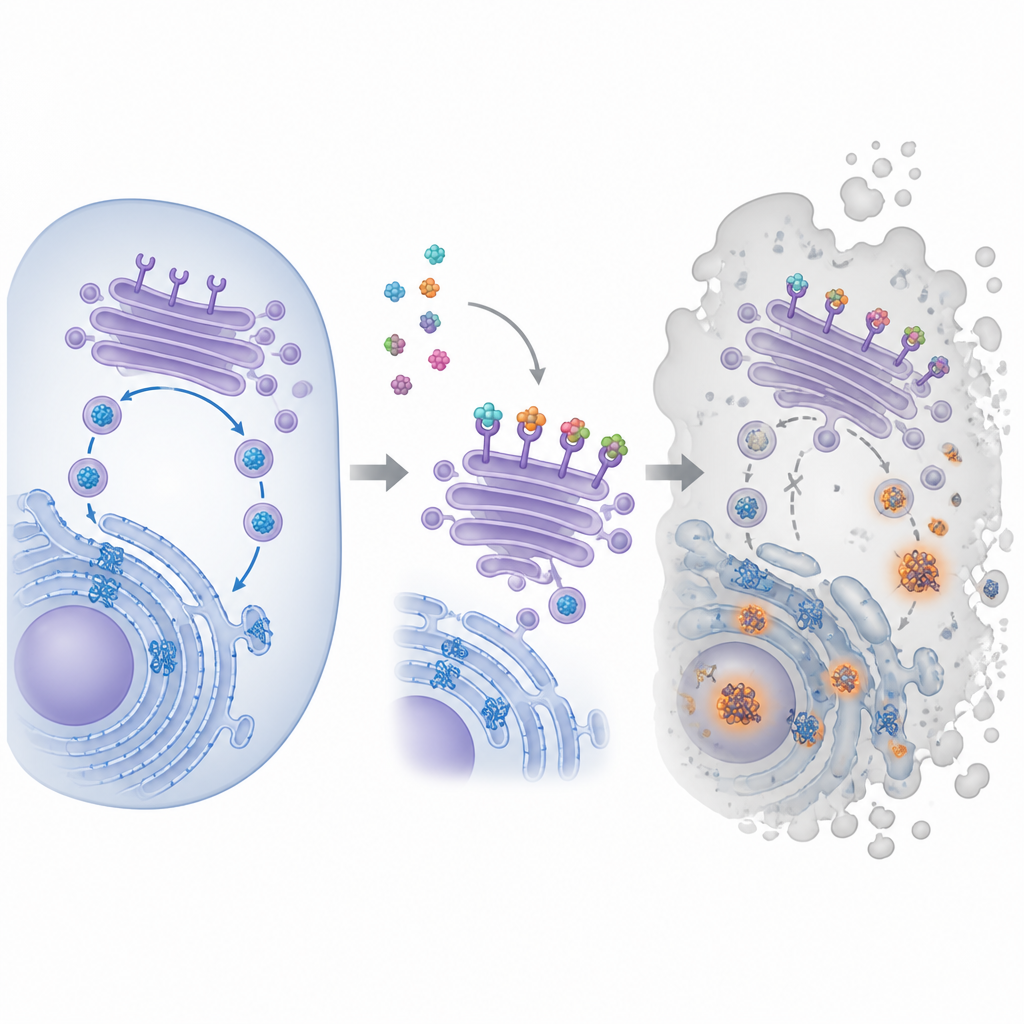
Una pequeña molécula con un gran blanco
El compuesto en el centro de este trabajo se llama pyra‑metho‑carnil, o PMC, originalmente identificado en una biblioteca de productos naturales. Estudios previos mostraron que PMC ralentiza el crecimiento de muchos tipos de células cancerosas, incluso cuando presentan diferentes mutaciones genéticas o son resistentes a otros fármacos. Sin embargo, su objetivo principal dentro de las células era desconocido. Para localizarlo, los investigadores unieron PMC a perlas magnéticas, las usaron como cebo para capturar socios de unión en extractos de células cancerosas y luego identificaron las proteínas atrapadas. Este enfoque puso de relieve una familia de proteínas conocidas como receptores KDEL, que se localizan en el centro de distribución celular y ayudan a recuperar ciertas proteínas auxiliares de vuelta al compartimento de plegamiento.
Secuestrando la ruta de reciclaje de la célula
Dentro de las células, las proteínas nuevas se pliegan en una estructura laberíntica llamada retículo endoplásmico y luego pasan por el Golgi, una pila de sacos membranosos que las ordena y las envía. Los receptores KDEL patrullan el Golgi y capturan proteínas auxiliares que llevan una pequeña etiqueta en su extremo, enviándolas de vuelta para su reutilización y así mantener la maquinaria de plegamiento. El equipo demostró que PMC se une a los tres tipos de receptores KDEL conocidos en humanos y cambia su localización dentro de las células. Usando etiquetas fluorescentes, observaron que receptores que normalmente se concentran en la cara anterior del Golgi se desplazaron tras el tratamiento con PMC. Al mismo tiempo, un colorante especial reveló la formación de agregados de proteínas mal plegadas, señalando que el circuito de plegamiento y reciclaje comenzaba a fallar.
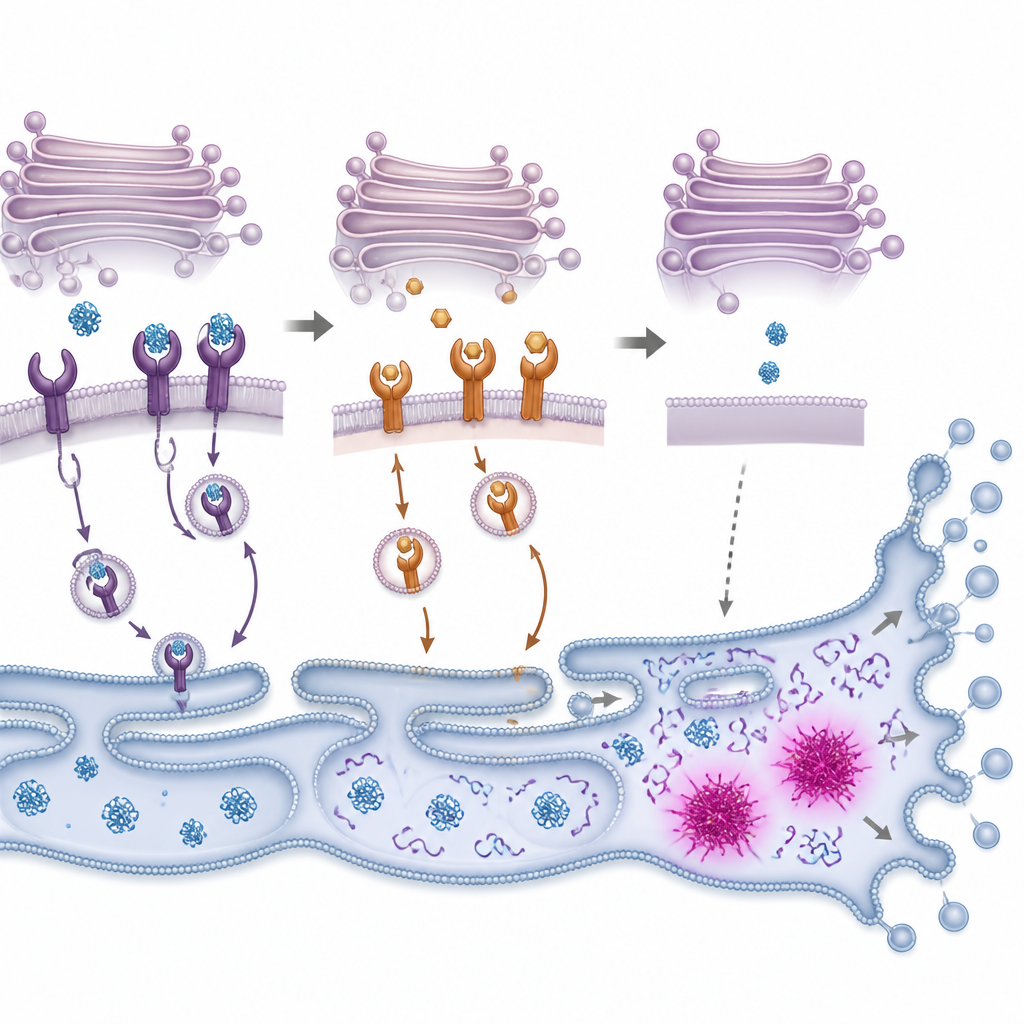
De la sobrecarga de proteínas al suicidio celular
Cuando las proteínas mal plegadas se acumulan, las células activan un sistema de alarma interno conocido como respuesta ante proteínas desplegadas. Este sistema primero intenta restablecer el equilibrio reduciendo la producción de nuevas proteínas y aumentando la capacidad para plegar y eliminar proteínas dañadas. Los investigadores observaron que PMC activó rápidamente componentes clave de esta respuesta en células de cáncer de colon, seguido por la activación de enzimas que descomponen componentes celulares durante la muerte celular programada. Bloquear estas enzimas, o reducir los niveles de un conmutador sensible al estrés llamado CHOP, aumentó la probabilidad de supervivencia tras la exposición a PMC, aunque no por completo. Esto sugiere que PMC empuja a las células más allá de un punto de inflexión en el que las vías de alivio del estrés fallan y se activan las rutas de autodestrucción.
Haciendo a las células cancerosas más vulnerables al estrés
El equipo también investigó si PMC podría sensibilizar a las células cancerosas a otras formas de estrés interno. Combinaron una dosis baja, por lo demás inocua, de PMC con tildipargina, un compuesto que altera el manejo del calcio y que se usa ampliamente para provocar estrés en el compartimento de plegamiento proteico. Juntos, los dos fármacos suprimieron el crecimiento celular con mayor intensidad que la tildipargina sola, y los marcadores de estrés aumentaron más, lo que indica que PMC reduce el umbral de daño. Para demostrar que los propios receptores KDEL son centrales en este efecto, los científicos utilizaron pequeñas moléculas de ARN para reducir directamente estos receptores. Esa manipulación por sí sola desencadenó la respuesta de estrés y ralentizó el crecimiento de las células cancerosas de manera similar.
Qué podría significar esto para futuros tratamientos contra el cáncer
En conjunto, el estudio sugiere que PMC actúa uniéndose a los receptores KDEL, perturbando su localización y función, y saboteando así la capacidad de la célula para mantener en orden su inventario proteico. Las células cancerosas, que ya operan cerca del límite de su capacidad de manejo de proteínas, parecen especialmente vulnerables a este tipo de alteración y pueden ser llevadas a la muerte programada. Aunque se necesitan más estudios en animales y pruebas de seguridad, los resultados señalan a los receptores KDEL y a las vías de estrés proteico relacionadas como puntos de entrada prometedores para nuevos fármacos contra el cáncer y para combinaciones que hagan más eficaces los tratamientos basados en el estrés existentes.
Cita: Yoshida, K., Nishi, K., Kitaguchi, T. et al. Pyra-metho-carnil disrupts cancer cell proteostasis and induces apoptosis by binding to KDEL receptors. Sci Rep 16, 15145 (2026). https://doi.org/10.1038/s41598-026-45604-z
Palabras clave: células cancerosas, plegamiento de proteínas, estrés del retículo endoplásmico, receptores KDEL, apoptosis