Clear Sky Science · pt
Pyra-metho-carnil interrompe a proteostase de células cancerosas e induz apoptose ao se ligar a receptores KDEL
Virando as fábricas de proteínas do câncer contra si mesmas
Células cancerosas crescem rapidamente e produzem enormes quantidades de proteínas, que precisam ser cuidadosamente dobradas e encaminhadas dentro da célula. Este estudo explora uma pequena molécula que enfraquece esse sistema interno de transporte, sobrecarregando as células cancerosas com proteínas danificadas até que elas se autodestruam, ao mesmo tempo em que aponta para uma nova forma de atacar tumores.
Uma pequena molécula com um grande alvo
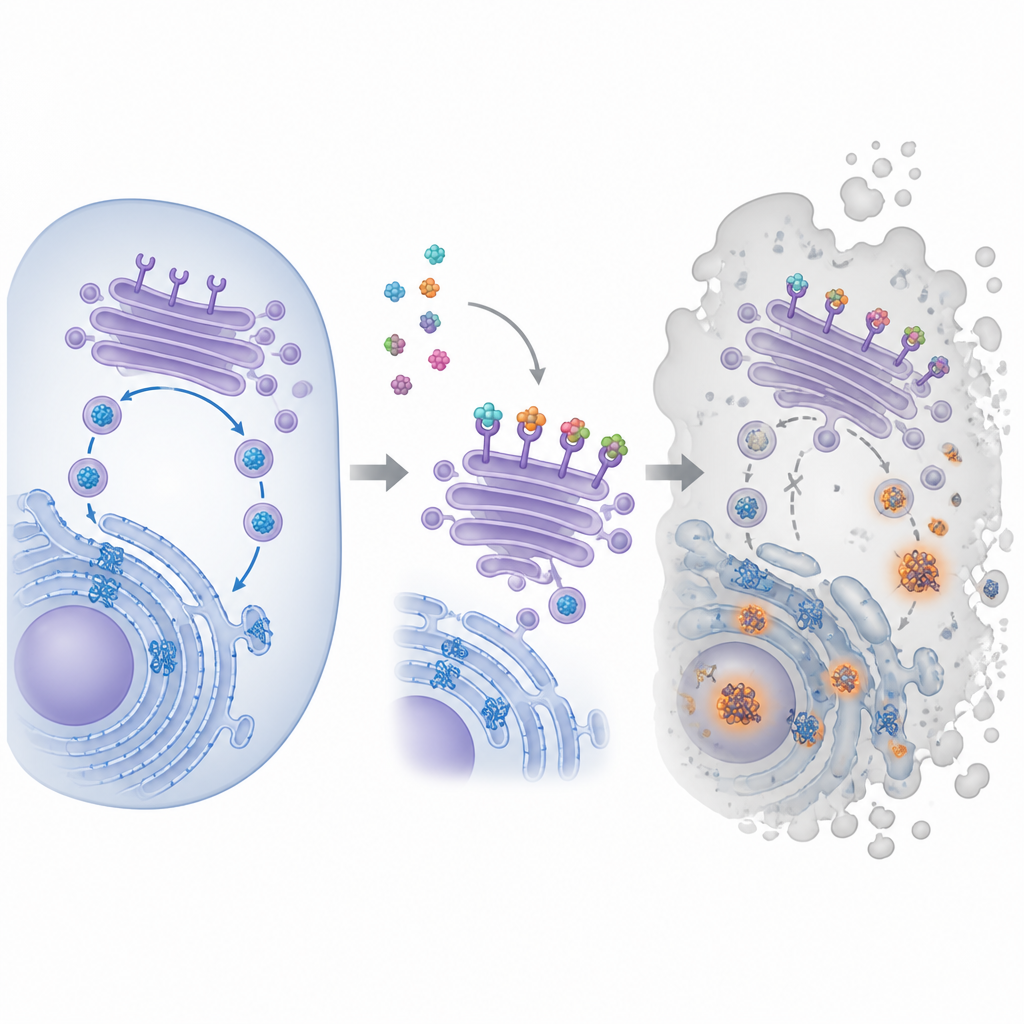
O composto no centro deste trabalho chama-se pyra‑metho‑carnil, ou PMC, originalmente encontrado em uma biblioteca de produtos naturais. Estudos anteriores mostraram que o PMC retarda o crescimento de muitos tipos de células cancerosas, mesmo quando elas apresentam diferentes mutações genéticas ou resistência a outros fármacos. Ainda assim, seu alvo principal dentro das células era desconhecido. Para identificá‑lo, os pesquisadores ligaram o PMC a esferas magnéticas, deixaram‑no “pescar” parceiros de ligação em extratos de células cancerosas e então identificaram as proteínas capturadas. Essa abordagem destacou uma família de proteínas conhecidas como receptores KDEL, que ficam no centro de triagem intracelular da célula e ajudam a recuperar certas proteínas auxiliadoras de volta para o compartimento de dobramento.
Sequestrando a rota de reciclagem da célula
Dentro das células, proteínas novas são dobradas em uma estrutura labiríntica chamada retículo endoplasmático e depois passam pelo complexo de Golgi, um empilhamento de sacos membranosos que as classifica e envia adiante. Receptores KDEL patrulham o Golgi e capturam proteínas assistentes que carregam uma pequena etiqueta na cauda, enviando‑as de volta para reaproveitamento para que a maquinaria de dobramento consiga dar conta do volume. A equipe mostrou que o PMC se liga aos três tipos conhecidos de receptores KDEL humanos e altera onde eles se localizam dentro das células. Usando marcadores fluorescentes, descobriram que receptores normalmente agrupados na face cis do Golgi se deslocaram após o tratamento com PMC. Ao mesmo tempo, um corante especial revelou crescentes aglomerados de proteínas mal dobradas, sinalizando que o ciclo de dobramento e reciclagem começava a falhar.
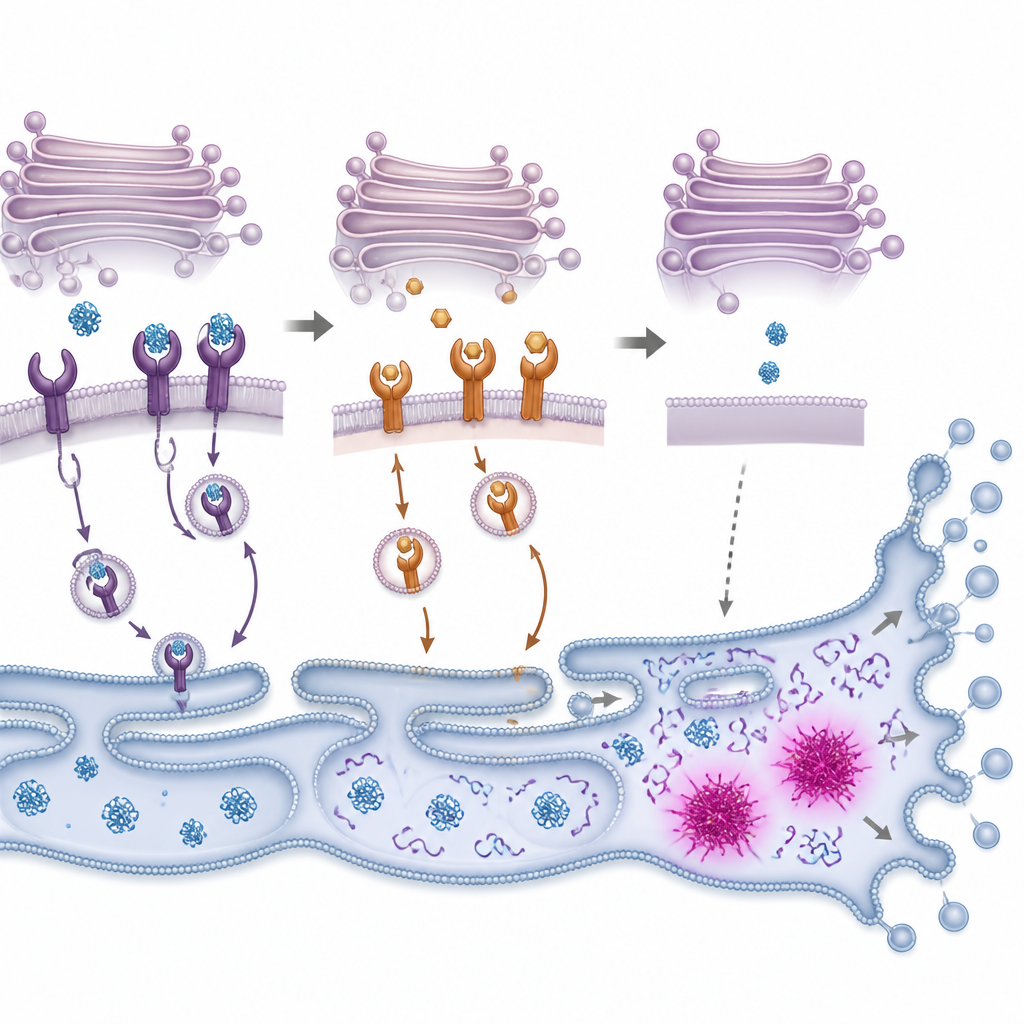
Do excesso de proteínas ao suicídio celular
Quando proteínas mal dobradas se acumulam, as células ativam um sistema de alarme interno frequentemente chamado de resposta a proteínas desnaturadas (unfolded protein response). Esse sistema tenta primeiro restaurar o equilíbrio, desacelerando a produção de novas proteínas e aumentando a capacidade de dobrar e eliminar proteínas danificadas. Os pesquisadores observaram que o PMC ativou rapidamente partes-chave dessa resposta em células de câncer de cólon, seguido pela ativação de enzimas que degradam componentes celulares durante a morte celular programada. Bloquear essas enzimas, ou reduzir os níveis de um interruptor sensível ao estresse chamado CHOP, tornava as células mais propensas a sobreviver à exposição ao PMC, embora não totalmente. Isso sugere que o PMC empurra as células além de um ponto de virada em que os mecanismos de alívio do estresse falham e as vias de autodestruição assumem o controle.
Tornando as células cancerosas mais vulneráveis ao estresse
A equipe também investigou se o PMC poderia tornar as células cancerosas mais sensíveis a outras formas de estresse interno. Eles combinaram uma dose baixa de PMC, por si só inócua, com tivesigargina, um composto que perturba o manejo de cálcio e é amplamente usado para provocar estresse no compartimento de dobramento de proteínas. Juntos, os dois fármacos suprimiram o crescimento celular mais fortemente do que a tivesigargina sozinha, e marcadores de estresse aumentaram mais, indicando que o PMC reduz o limiar para o dano. Para demonstrar que os próprios receptores KDEL são centrais nesse efeito, os cientistas usaram pequenas moléculas de RNA para reduzir diretamente esses receptores. Essa manipulação isolada desencadeou a resposta ao estresse e retardou o crescimento de células cancerosas de forma semelhante.
O que isso pode significar para tratamentos futuros do câncer
No geral, o estudo sugere que o PMC atua ligando‑se aos receptores KDEL, perturbando sua localização e função e, assim, sabotando a capacidade da célula de manter em ordem seu inventário de proteínas. Células cancerosas, que já operam perto do limite de sua capacidade de processamento proteico, parecem especialmente vulneráveis a esse tipo de perturbação e podem ser levadas à morte programada. Embora mais trabalhos em animais e testes de segurança sejam necessários, os resultados apontam os receptores KDEL e as vias relacionadas ao estresse proteico como pontos de entrada promissores para novos fármacos contra o câncer e para combinações que tornem tratamentos baseados em estresse existentes mais eficazes.
Citação: Yoshida, K., Nishi, K., Kitaguchi, T. et al. Pyra-metho-carnil disrupts cancer cell proteostasis and induces apoptosis by binding to KDEL receptors. Sci Rep 16, 15145 (2026). https://doi.org/10.1038/s41598-026-45604-z
Palavras-chave: células cancerosas, dobremento de proteínas, estresse do retículo endoplasmático, receptores KDEL, apoptose