Clear Sky Science · de
Pyra-metho-carnil stört die Proteostase von Krebszellen und induziert Apoptose durch Bindung an KDEL‑Rezeptoren
Die Proteinfabriken der Krebszelle gegen sich selbst wenden
Krebszellen wachsen schnell und produzieren enorme Mengen an Proteinen, die sorgfältig gefaltet und innerhalb der Zelle versendet werden müssen. Diese Studie untersucht ein kleines Molekül, das in dieses interne Versandnetzwerk greift, Krebszellen mit beschädigten Proteinen überlädt, bis sie sich selbst zerstören, und gleichzeitig einen neuen Ansatz zur gezielten Bekämpfung von Tumoren aufzeigt.
Ein kleines Molekül mit großem Ziel
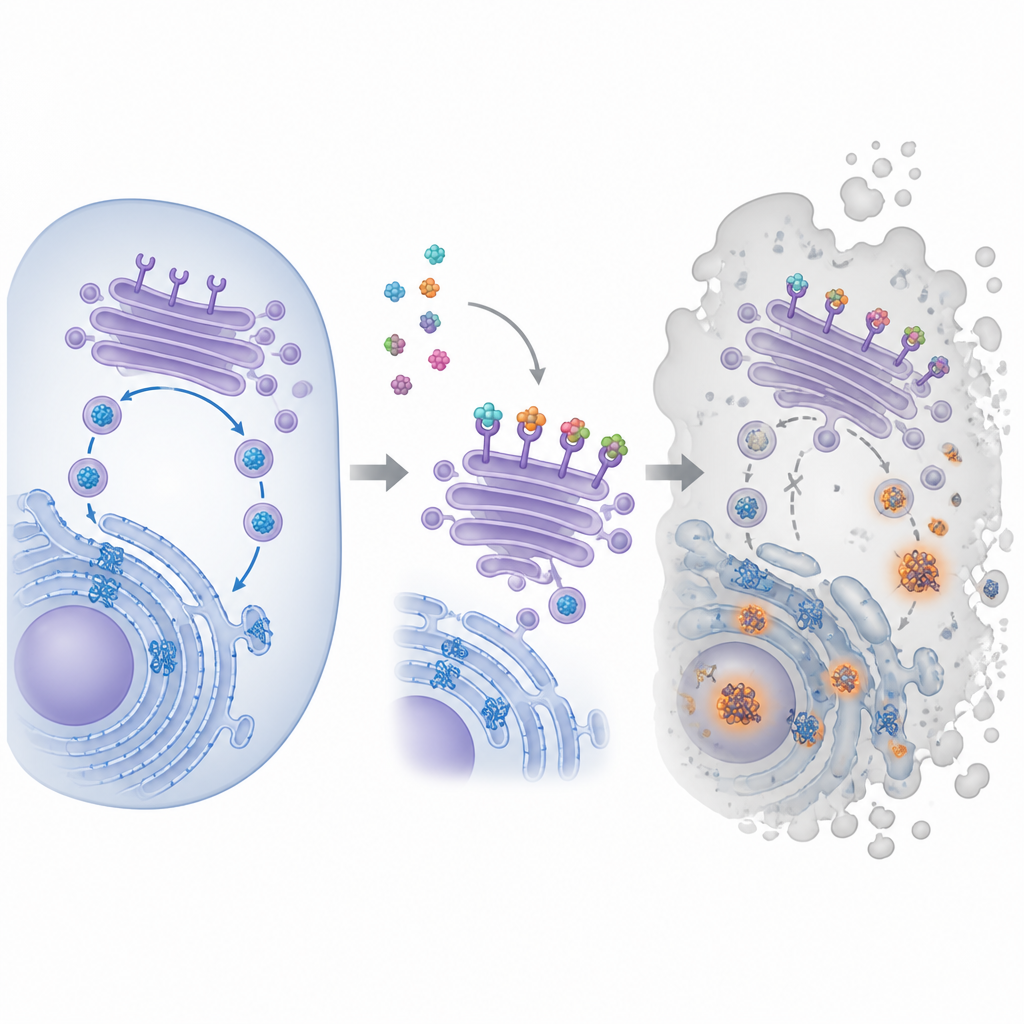
Die Verbindung im Zentrum dieser Arbeit heißt Pyra‑metho‑carnil, kurz PMC, und wurde ursprünglich in einer Naturstoffbibliothek entdeckt. Frühere Studien zeigten, dass PMC das Wachstum vieler Krebszelltypen verlangsamt, selbst bei unterschiedlichen genetischen Veränderungen oder Medikamentenresistenzen. Sein hauptsächliches Ziel in der Zelle war jedoch unbekannt. Um das zu identifizieren, koppelten die Forscher PMC an magnetische Kügelchen, ließen es Bindungspartner in Extrakten von Krebszellen „angeln“ und analysierten dann die gefangenen Proteine. Dieser Ansatz machte eine Proteinfamilie sichtbar, die als KDEL‑Rezeptoren bekannt ist und im internen Versandzentrum der Zelle sitzt und bestimmte Helferproteine zur Wiederverwendung zurück in das Faltungskompartiment holt.
Die Recyclingroute der Zelle kapern
Innerhalb der Zelle werden neue Proteine in einem labyrinthartigen System, dem endoplasmatischen Retikulum, gefaltet und passieren dann den Golgi‑Apparat, einen Stapel membranöser Taschen, der sie sortiert und weiterleitet. KDEL‑Rezeptoren patrouillieren im Golgi und fassen Helferproteine mit einem kurzen Erkennungs‑Tag am Ende, um sie zur Wiederverwendung zurückzuschicken, damit die Faltungsmaschinerie mithalten kann. Das Team zeigte, dass PMC an alle drei bekannten menschlichen KDEL‑Rezeptortypen bindet und ihre Position innerhalb der Zellen verändert. Mit fluoreszenten Markern fanden sie, dass Rezeptoren, die normalerweise am vorderen Bereich des Golgi konzentriert sind, nach PMC‑Behandlung fehlplatziert wurden. Gleichzeitig zeigte ein spezieller Farbstoff wachsende Aggregate fehlgefalteter Proteine, ein Hinweis darauf, dass der Faltungs‑ und Recyclingkreislauf zu versagen beginnt.
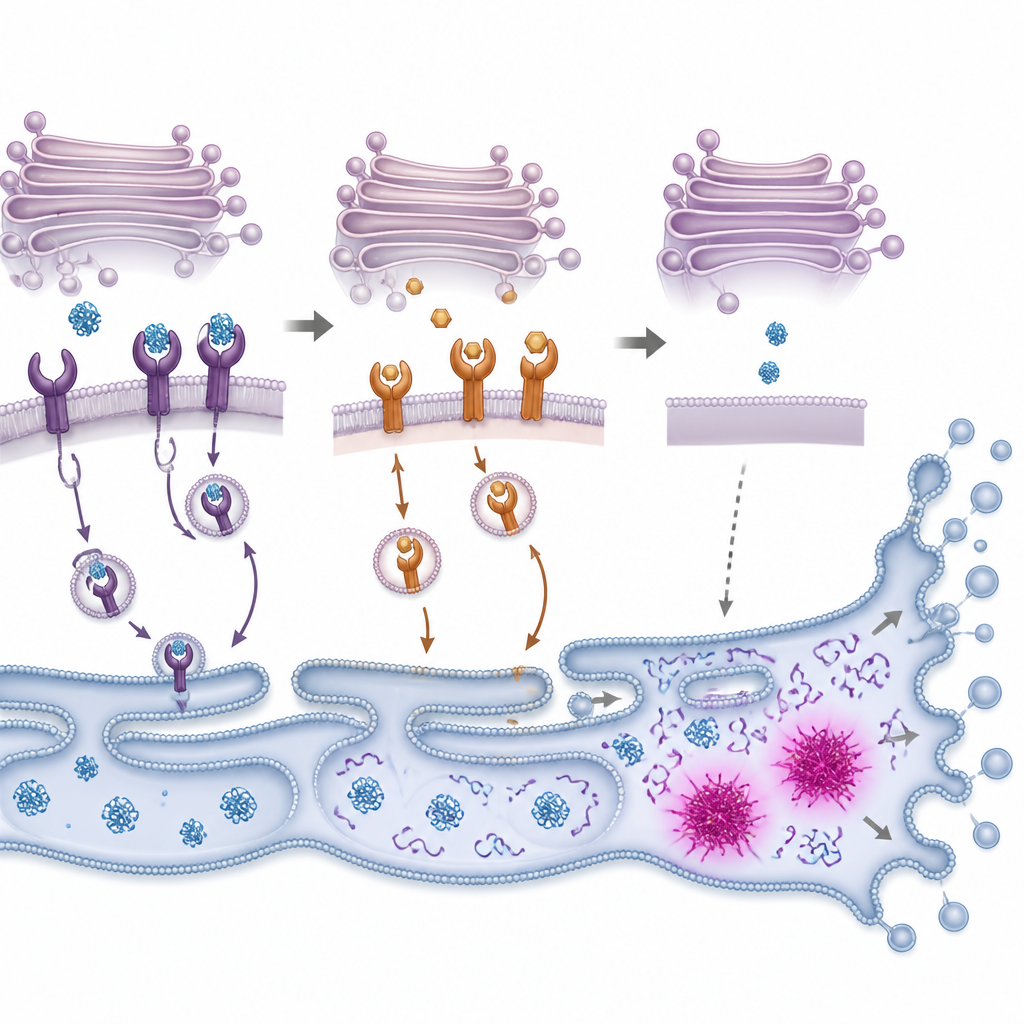
Von Proteinüberladung zur Selbsttötung der Zelle
Sobald sich fehlgefaltete Proteine anhäufen, schalten Zellen ein internes Alarmsystem ein, oft als „unfolded protein response“ bezeichnet. Dieses System versucht zunächst, das Gleichgewicht wiederherzustellen, indem es die Produktion neuer Proteine drosselt und die Kapazität zum Falten und Abbau beschädigter Proteine erhöht. Die Forscher beobachteten, dass PMC in Kolonkarzinomzellen rasch zentrale Komponenten dieser Reaktion aktivierte, gefolgt von der Aktivierung von Enzymen, die während des programmierten Zelltods zelluläre Bestandteile zerschneiden. Die Blockade dieser Enzyme oder die Verringerung des Niveaus eines stress‑antwortenden Schalters namens CHOP ließ die Zellen nach PMC‑Exposition wahrscheinlicher überleben, jedoch nicht vollständig. Das deutet darauf hin, dass PMC Zellen über einen Kipppunkt hinaustreibt, an dem Stressbewältigung versagt und Selbstzerstörungswege übernehmen.
Krebszellen anfälliger für Stress machen
Das Team prüfte außerdem, ob PMC Krebszellen gegenüber anderen Formen internen Stresses empfindlicher machen kann. Sie kombinierten eine niedrige, sonst harmlose Dosis PMC mit Thapsigargin, einer Verbindung, die die Calciumregulation stört und häufig verwendet wird, um Stress im Proteinfaltungskompartiment auszulösen. Zusammen hemmten die beiden Wirkstoffe das Zellwachstum stärker als Thapsigargin allein, und Stressmarker stiegen stärker an, was darauf hindeutet, dass PMC die Schwelle für Schädigung senkt. Um zu zeigen, dass KDEL‑Rezeptoren selbst zentral für diesen Effekt sind, setzten die Wissenschaftler kleine RNA‑Moleküle ein, um diese Rezeptoren direkt zu reduzieren. Diese Manipulation allein löste die Stressantwort aus und verlangsamte das Wachstum von Krebszellen auf ähnliche Weise.
Was das für künftige Krebstherapien bedeuten könnte
Insgesamt deutet die Studie darauf hin, dass PMC wirkt, indem es an KDEL‑Rezeptoren bindet, deren Standort und Funktion stört und so die Fähigkeit der Zelle sabotiert, ihr Proteininventar in Ordnung zu halten. Krebszellen, die bereits nahe an der Kapazitätsgrenze ihrer Proteinverarbeitung operieren, scheinen für eine solche Störung besonders anfällig zu sein und können in den programmierten Zelltod gedrängt werden. Während weitere Arbeiten an Tiermodellen und Sicherheitsprüfungen nötig sind, weisen die Ergebnisse auf KDEL‑Rezeptoren und verwandte Proteinstress‑Wege als vielversprechende Angriffsziele für neue Krebsmedikamente und für Kombinationen, die bestehende stressbasierte Therapien wirksamer machen, hin.
Zitation: Yoshida, K., Nishi, K., Kitaguchi, T. et al. Pyra-metho-carnil disrupts cancer cell proteostasis and induces apoptosis by binding to KDEL receptors. Sci Rep 16, 15145 (2026). https://doi.org/10.1038/s41598-026-45604-z
Schlüsselwörter: Krebszellen, Proteinfaltung, Stress des endoplasmatischen Retikulums, KDEL‑Rezeptoren, Apoptose