Clear Sky Science · it
Pyra-metho-carnil interrompe la proteostasi delle cellule tumorali e induce apoptosi legandosi ai recettori KDEL
Rivoltare contro se stesse le fabbriche di proteine del cancro
Le cellule tumorali crescono rapidamente e producono enormi quantità di proteine, che devono essere accuratamente ripiegate e indirizzate all’interno della cellula. Questo studio esplora una piccola molecola che mette i bastoni fra le ruote a quel sistema interno di smistamento, sovraccaricando le cellule tumorali con proteine danneggiate fino a farle autodistruggere, suggerendo al contempo un nuovo modo per colpire i tumori.
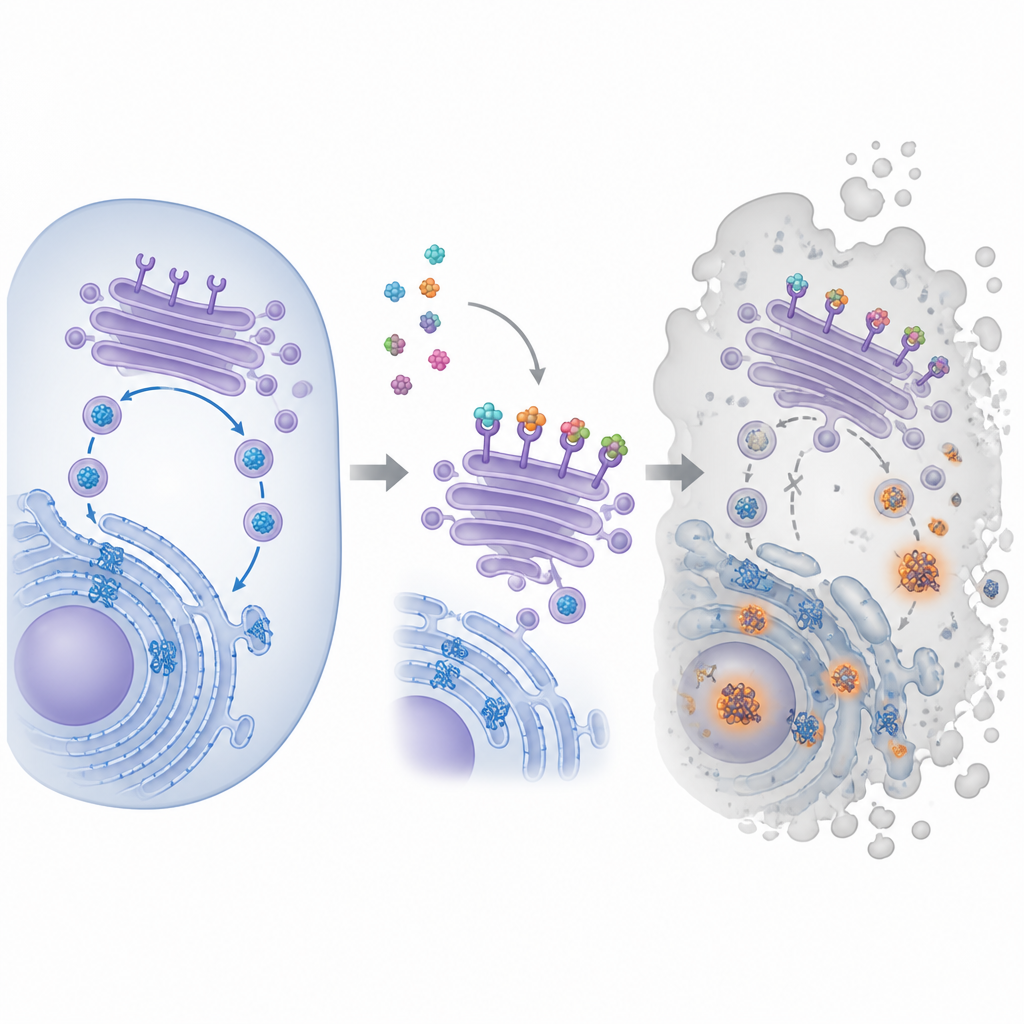
Una piccola molecola con un grande bersaglio
Il composto al centro di questo lavoro si chiama pyra‑metho‑carnil, o PMC, scoperto inizialmente in una libreria di prodotti naturali. Studi precedenti avevano mostrato che PMC rallenta la crescita di molti tipi di cellule tumorali, anche quando presentano diverse mutazioni genetiche o sono resistenti ad altri farmaci. Tuttavia il suo bersaglio principale all’interno delle cellule era sconosciuto. Per individuarlo, i ricercatori hanno attaccato PMC a perle magnetiche, le hanno usate per pescare i partner di legame negli estratti di cellule tumorali e poi hanno identificato le proteine catturate. Questo approccio ha messo in luce una famiglia di proteine note come recettori KDEL, che risiedono nell’hub di smistamento interno della cellula e aiutano a recuperare certe proteine ausiliarie riportandole al compartimento di ripiegamento.
Dirottare la via di riciclo della cellula
All’interno delle cellule, le nuove proteine vengono ripiegate in una struttura labirintica chiamata reticolo endoplasmatico e poi passano attraverso l’apparato del Golgi, una pila di tasche membranose che le smista e le invia oltre. I recettori KDEL pattugliano il Golgi e afferrano proteine ausiliarie che portano un breve segnale terminale, rimandandole indietro per il riuso così che la macchina del ripiegamento possa reggere il carico. Il gruppo ha dimostrato che PMC si lega a tutti e tre i tipi noti di recettori KDEL umani e modifica la loro collocazione all’interno delle cellule. Usando etichette fluorescenti, hanno osservato che recettori normalmente concentrati sul lato anteriore del Golgi si spostavano dalla loro posizione dopo il trattamento con PMC. Allo stesso tempo, un colorante speciale ha rivelato aggregati crescenti di proteine mal ripiegate, segno che il circuito di ripiegamento e riciclo delle proteine stava cominciando a cedere.
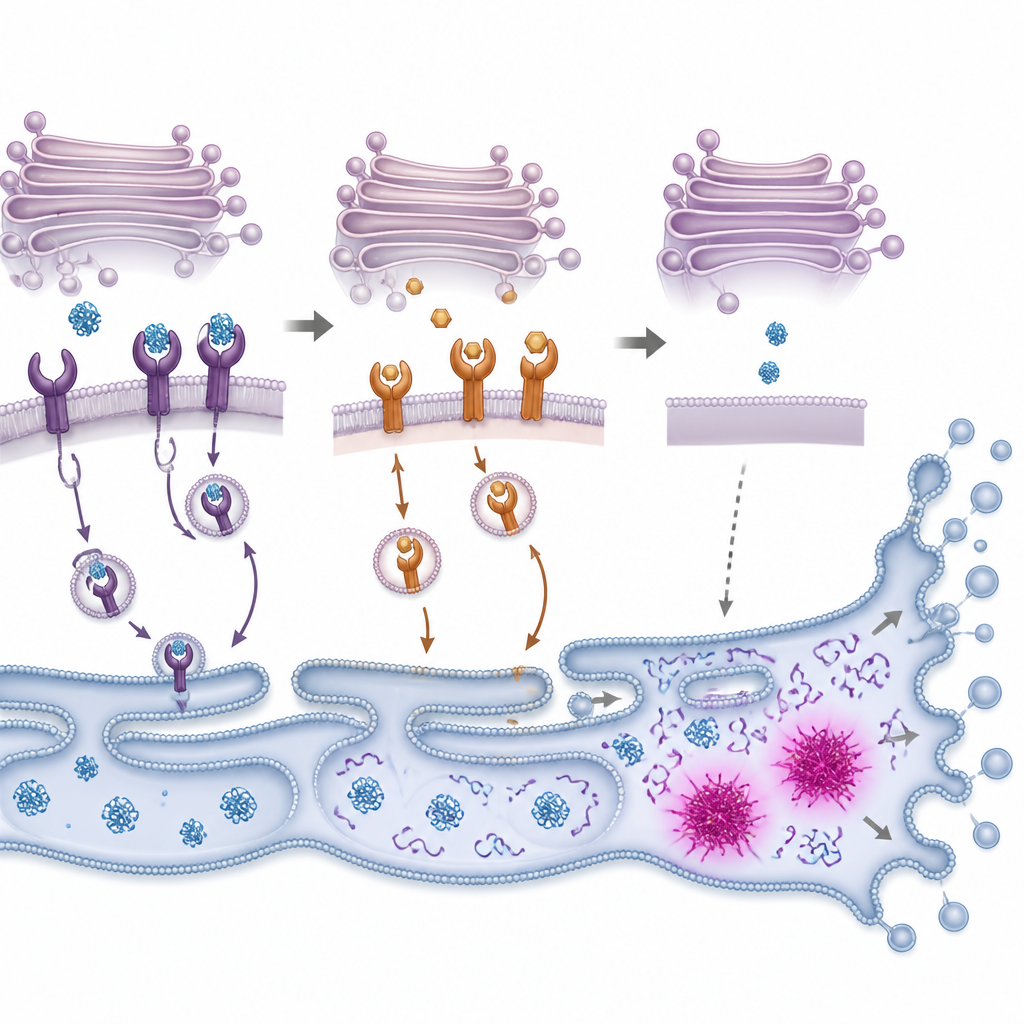
Dall’overload proteico al suicidio cellulare
Quando le proteine mal ripiegate si accumulano, le cellule attivano un sistema di allarme interno spesso chiamato risposta alle proteine non ripiegate. Questo sistema cerca inizialmente di ripristinare l’equilibrio rallentando la produzione di nuove proteine e aumentando la capacità di ripiegare e eliminare quelle danneggiate. I ricercatori hanno osservato che PMC attiva rapidamente componenti chiave di questa risposta in cellule tumorali del colon, seguita dall’attivazione di enzimi che degradano componenti cellulari durante la morte cellulare programmata. Bloccare questi enzimi, o ridurre i livelli di un interruttore sensibile allo stress chiamato CHOP, ha aumentato la probabilità che le cellule sopravvivessero all’esposizione a PMC, sebbene non completamente. Ciò suggerisce che PMC spinge le cellule oltre un punto critico in cui i meccanismi di sollievo dallo stress falliscono e prevalgono le vie di autodistruzione.
Rendere le cellule tumorali più vulnerabili allo stress
Il gruppo ha poi indagato se PMC potesse rendere le cellule tumorali più sensibili ad altre forme di stress interno. Hanno combinato una dose bassa, altrimenti innocua, di PMC con thapsigargin, un composto che altera la gestione del calcio e viene ampiamente usato per indurre stress nel compartimento di ripiegamento delle proteine. Insieme, i due farmaci hanno sopresso la crescita cellulare in misura maggiore rispetto al solo thapsigargin, e i marcatori di stress sono aumentati di più, indicando che PMC abbassa la soglia per il danno. Per dimostrare che sono i recettori KDEL stessi a essere centrali in questo effetto, gli scienziati hanno usato piccole molecole di RNA per ridurre direttamente questi recettori. Questa manipolazione da sola ha innescato la risposta di stress e rallentato la crescita delle cellule tumorali in modo analogo.
Cosa potrebbe significare per i futuri trattamenti contro il cancro
Nel complesso, lo studio suggerisce che PMC agisce legandosi ai recettori KDEL, perturbandone la localizzazione e la funzione e sabotando così la capacità della cellula di mantenere in ordine il proprio inventario proteico. Le cellule tumorali, che già operano vicino al limite della loro capacità di gestione delle proteine, risultano particolarmente vulnerabili a questo tipo di perturbazione e possono essere spinte verso la morte programmata. Pur richiedendo ulteriori studi su modelli animali e test di sicurezza, i risultati indicano i recettori KDEL e le vie di stress proteico correlate come punti di ingresso promettenti per nuovi farmaci anti‑tumorali e per combinazioni che potenzino trattamenti basati sullo stress già esistenti.
Citazione: Yoshida, K., Nishi, K., Kitaguchi, T. et al. Pyra-metho-carnil disrupts cancer cell proteostasis and induces apoptosis by binding to KDEL receptors. Sci Rep 16, 15145 (2026). https://doi.org/10.1038/s41598-026-45604-z
Parole chiave: cellule tumorali, ripiegamento delle proteine, stress del reticolo endoplasmatico, recettori KDEL, apoptosi