Clear Sky Science · ru
Пира‑мето‑карнил нарушает протеостаз раковых клеток и вызывает апоптоз, связываясь с KDEL‑рецепторами
Обращение белковых «фабрик» рака против них самих
Раковые клетки быстро растут и вырабатывают огромные количества белков, которые нужно тщательно сворачивать и транспортировать внутри клетки. В этом исследовании изучается небольшая молекула, нарушающая эту внутреннюю транспортную систему, перегружая раковые клетки повреждёнными белками до тех пор, пока они не самоуничтожатся, что указывает на новый способ нацеливания опухолей.
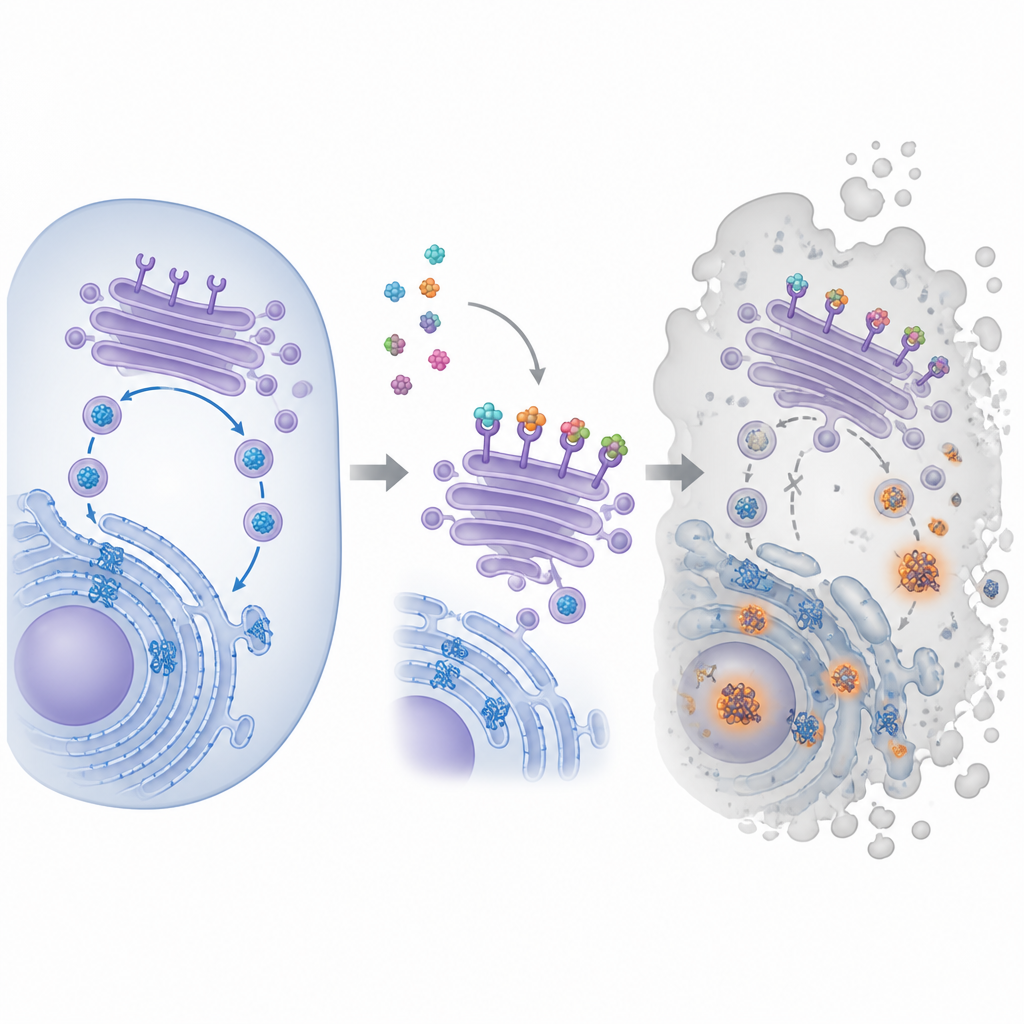
Небольшая молекула с большой целью
Соединение в центре этого исследования называется пира‑мето‑карнил, или PMC, и было обнаружено в библиотеке природных продуктов. Ранние работы показали, что PMC замедляет рост многих типов раковых клеток, даже если они несут разные генетические мутации или устойчивы к другим препаратам. Однако его основной внутриклеточный мишень оставалась неизвестной. Чтобы выяснить это, исследователи прикрепили PMC к магнитным шарикам, позволили им «выловить» связывающиеся партнёры в экстрактах раковых клеток и затем идентифицировали захваченные белки. Этот подход выделил семейство белков, известных как KDEL‑рецепторы, которые локализуются в внутриклеточном транспортном хабе и помогают возвращать определённые шапероны обратно в компартмент свёртывания.
Перехват маршрута утилизации клетки
Внутри клетки новые белки сворачиваются в запутанной структуре, называемой эндоплазматическим ретикулумом, а затем проходят через комплекс Гольджи — стопку мембранных карманов, которые сортируют и направляют их дальше. KDEL‑рецепторы патрулируют Гольджи и захватывают шапероны с коротким тегом на хвосте, отправляя их назад для повторного использования, чтобы свёртывающая аппаратура могла справляться с нагрузкой. Авторы показали, что PMC связывается со всеми тремя известными человеческими типами KDEL‑рецепторов и изменяет их субклеточную локализацию. С помощью флуоресцентных меток они обнаружили, что рецепторы, обычно сосредоточенные на передней стороне Гольджи, перемещаются с места после обработки PMC. Одновременно специальный краситель выявил образование всё больших скоплений неправильно свернутых белков, что указывает на начало сбоя в цикле свёртывания и утилизации белков.
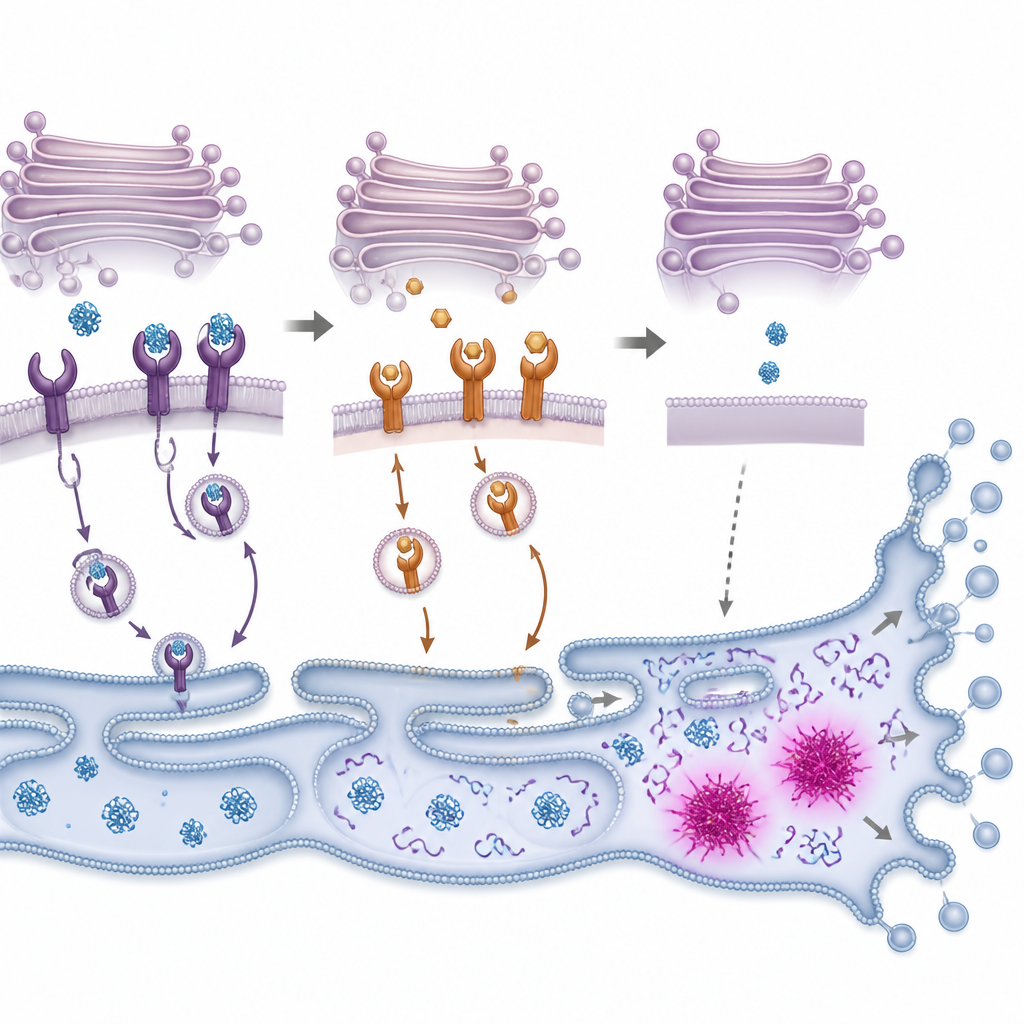
От перегруза белками до клеточного самоубийства
Когда неправильно свернутые белки накапливаются, клетки включают внутреннюю систему сигнализации, часто называемую ответом на накопление неправильно свернутых белков. Эта система сначала пытается восстановить равновесие, замедляя синтез новых белков и повышая способность сворачивать и утилизировать повреждённые белки. Исследователи наблюдали, что PMC быстро активирует ключевые элементы этого ответа в клетках колоректального рака, за чем следует активация ферментов, разрушающих клеточные компоненты во время программируемой гибели. Блокирование этих ферментов или снижение уровня стресс‑индуцируемого переключателя CHOP увеличивало шансы клеток выжить при воздействии PMC, хотя и не полностью. Это указывает на то, что PMC толкает клетки за предел критической точки, где механизмы снятия стресса терпят неудачу и включаются пути самоуничтожения.
Повышение уязвимости раковых клеток к стрессу
Авторы также проверили, может ли PMC сделать раковые клетки более чувствительными к другим видам внутриклеточного стресса. Они сочетали низкую, в остальном безвредную, дозу PMC с тапсифаргином — соединением, нарушающим обмен кальция и широко используемым для вызова стресса в компартменте свёртывания белков. Вместе оба препарата сильнее подавляли рост клеток, чем тапсифаргин в одиночку, и маркеры стресса повышались сильнее, что указывает на то, что PMC снижает порог повреждения. Чтобы показать, что сами KDEL‑рецепторы важны для этого эффекта, учёные использовали малые молекулы РНК для их прямого уменьшения. Это вмешательство само по себе вызвало стресс‑ответ и замедлило рост раковых клеток аналогичным образом.
Что это может значить для будущего лечения рака
В целом исследование предполагает, что PMC действует, связываясь с KDEL‑рецепторами, нарушая их локализацию и функцию и тем самым саботируя способность клетки поддерживать порядок в белковом инвентаре. Раковые клетки, которые уже работают близко к пределу своей способности обрабатывать белки, особенно уязвимы к такого рода нарушениям и могут быть подтолкнуты к программируемой гибели. Хотя необходимы дальнейшие исследования на животных и испытания безопасности, результаты указывают на KDEL‑рецепторы и связанные пути стресса белков как перспективные мишени для новых противораковых препаратов и для комбинаций, которые повысят эффективность существующих стресс‑ориентированных методов лечения.
Цитирование: Yoshida, K., Nishi, K., Kitaguchi, T. et al. Pyra-metho-carnil disrupts cancer cell proteostasis and induces apoptosis by binding to KDEL receptors. Sci Rep 16, 15145 (2026). https://doi.org/10.1038/s41598-026-45604-z
Ключевые слова: раковые клетки, свертывание белков, стресс эндоплазматического ретикулума, KDEL‑рецепторы, апоптоз