Clear Sky Science · he
פיירה‑מתו‑קארניל מפורר את הפרוטאוסטזיס בתאי סרטן ומעורר אפופטוזה על ידי קשירה לקולטני KDEL
להפנות את מפעלי החלבון של הסרטן נגד עצמם
תאי סרטן גדלים במהירות ומייצרים כמויות עצומות של חלבונים, שצריכים לעבור קיפול מדויק ושילוח בתוך התא. מחקר זה בוחן מולקולה קטנה שמפרה את מערכת השילוח הפנימית, מעמיסה על תאי הסרטן חלבונים פגומים עד שהם מתמוטטים ומפעילים מנגנוני מוות‑עצמי, ובכך מצביע על אסטרטגיה חדשה למיקוד גידולים.
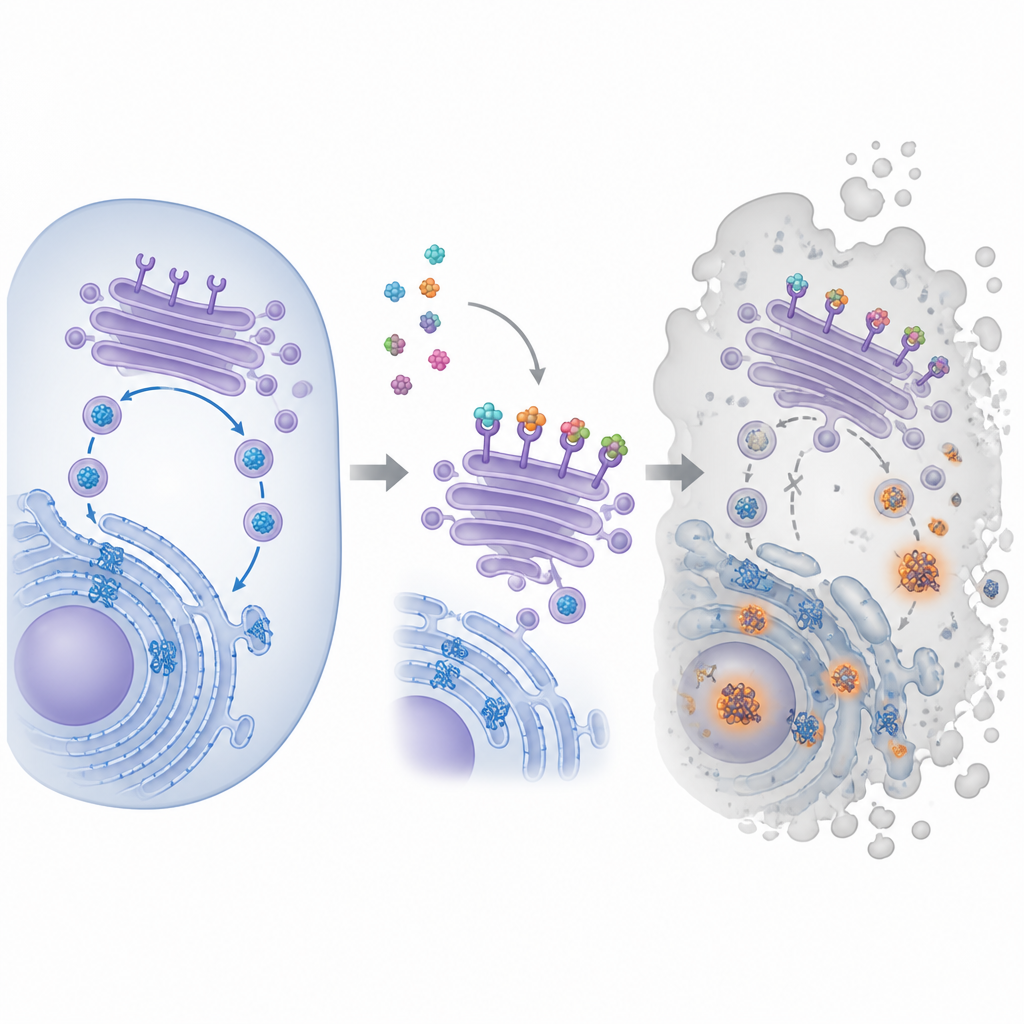
מולקולה קטנה עם מטרה גדולה
התרכובת שבמרכז העבודה נקראת פיירה‑מתו‑קארניל, או PMC, והיא נמצאה תחילה בספריית תוצרי טבע. מחקרים קודמים הראו ש‑PMC מאט את גדילת סוגים רבים של תאים סרטניים, גם כאשר הם נושאים מוטציות שונות או עמידות לתרופות אחרות. עם זאת, מטרתה העיקרית בתוך התאים נותרה לא ידועה. כדי לאתרה, החוקרים צירפו את PMC לפנינים מגנטיות, השתמשו בהן כדי לדוג שותפים לקשירה מתוך תמציות תאי סרטן, ואז זיהו את החלבונים שנלכדו. הגישה הזו הדגישה משפחה של חלבונים הידועים כקולטני KDEL, שנמצאים בצומת השילוח התוך‑תאי ועוזרים להחזיר חלבונים מסייעים חזרה למחלקת הקיפול.
חטיפת נתיב המיחזור של התא
בתוך התא החלבונים החדשים מקופלים במבנה מסועף הנקרא רשתית אנדופלזמטית, ולאחר מכן עוברים דרך הגולג'י, ערימת כיסים ממברנליים שממיינת ושולחת אותם הלאה. קולטני KDEL סורקים את הגולג'י ותופסים חלבונים מסייעים שנושאים תג קצר בזנבם, ושולחים אותם חזרה לשימוש חוזר כדי שמכונת הקיפול תוכל להמשיך לתפקד. הצוות הראה ש‑PMC נקשר לכל שלושת סוגי קולטני KDEL האנושיים ומשנה את מיקומם בתוך התאים. באמצעות תגים פלואורסצנטיים הם מצאו שקולטים שלרוב מקובצים בצד הקדמי של הגולג'י זזו ממקומם לאחר טיפול ב‑PMC. בו‑בזמן, צבע מיוחד חשף הצטברות גושים של חלבונים לא מקופלים, מה שמעיד שמעגל הקיפול והמיחזור מתחיל להיכשל.
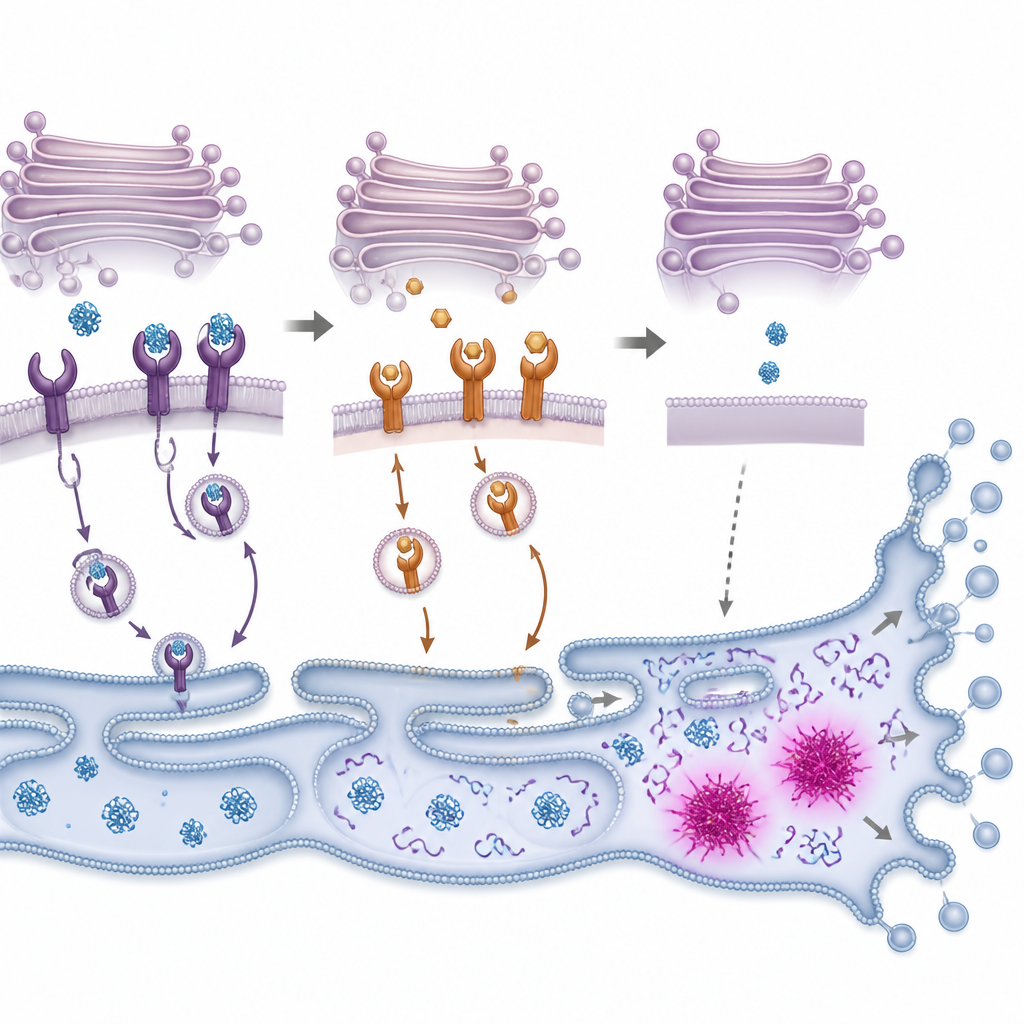
ממעוות חלבונים אל התאבדות תאי
כאשר חלבונים לא מקופלים מצטברים, התאים מדליקים מערכת אזעקה פנימית שלרוב נקראת תגובת החלבון הלא מקופל (UPR). המערכת הזו מנסה ראשית לשקם את האיזון על‑ידי האטת ייצור החלבון והגברת היכולת לקפל ולנקות חלבונים פגומים. החוקרים ראו ש‑PMC הפעיל במהירות מרכיבים מרכזיים של תגובה זו בתאי סרטן במעי הגס, ואחר כך הוביל להפעלת אנזימים שמבצעים פירוק מרכיבים תאים בתהליכים של מוות מתוכנת. חסימת אנזימים אלה, או הקטנת רמותו של מתג רגיש־לחץ בשם CHOP, העלתה את סיכויי הישרדות התאים לחשיפה ל‑PMC, אם כי לא באופן מוחלט. ממצאים אלה מצביעים על כך ש‑PMC דוחף את התאים מעבר לנקודת שווי משקל שבה שחרור הלחץ נכשל ומנגנוני ההשמדה העצמית משתלטים.
להגביר את הפגיעות של תאי הסרטן ללחץ
הצוות גם בדק האם PMC יכול להפוך תאי סרטן לרגישים יותר לצורות אחרות של לחץ פנימי. הם שילבו מינון נמוך של PMC, שלחלוטין לא היה מזיק לבדו, עם תפסיגרגין (thapsigargin), תרכובת שמפריעה לטיפול בסידן ומשמשת באופן נרחב לגרום למתח במחלקת קיפול החלבונים. יחד, שתי התרופות דיכאו את גדילת התאים בעוצמה רבה יותר מתפסיגרגין לבדו, וסימני המתח עלו גבוה יותר, מה שמעיד ש‑PMC מוריד את סף הנזק. כדי להראות שקולטני KDEL עצמם מרכזיים לאפקט זה, המדענים השתמשו במולקולות RNA קטנות כדי להפחית את רמות הקולטנים ישירות. המניפולציה הזו מעצמה עוררה את תגובת המתח והאטה את גדילת תאי הסרטן באופן דומה.
מה משמעות הדבר לטיפולי סרטן עתידיים
בסך הכל המחקר מציע ש‑PMC פועל על‑ידי קשירה לקולטני KDEL, שיבוש מיקומם ותפקודם, וכך סבאטז' על יכולת התא לשמור על מלאי החלבונים בסדר. תאי סרטן, שכבר פועלים קרוב לגבול יכולתם לטפל בחלבונים, נראים פגיעים במיוחד לשיבוש כזה וניתן לדחוק אותם למוות מתוכנת. בעוד שיש צורך בעבודות המשך בחיות ובבדיקות בטיחות, התוצאות מצביעות על קולטני KDEL ונתיבי מתח חלבוני קשורים כנקודות כניסה מבטיחות לתרופות סרטן חדשות ולשילובים שמשפרים את היעילות של טיפולים המבוססים על יצירת לחץ תאית.
ציטוט: Yoshida, K., Nishi, K., Kitaguchi, T. et al. Pyra-metho-carnil disrupts cancer cell proteostasis and induces apoptosis by binding to KDEL receptors. Sci Rep 16, 15145 (2026). https://doi.org/10.1038/s41598-026-45604-z
מילות מפתח: תאי סרטן, קיפול חלבונים, מתח ברשת התוך‑תאית (ER), קולטני KDEL, אפופטוזה