Clear Sky Science · pl
Pyra-metho-carnil zaburza proteostazę komórek nowotworowych i wywołuje apoptozę przez wiązanie z receptorami KDEL
Obrócenie fabryk białek raka przeciwko nim samym
Komórki nowotworowe rosną szybko i produkują ogromne ilości białek, które muszą być starannie złożone i dostarczone wewnątrz komórki. To badanie opisuje małą cząsteczkę, która wrzuca kluczowy trybik w system wewnętrznego transportu, przeciążając komórki nowotworowe uszkodzonymi białkami aż do ich samodestrukcji, jednocześnie wskazując nowy sposób celowania w guzy.
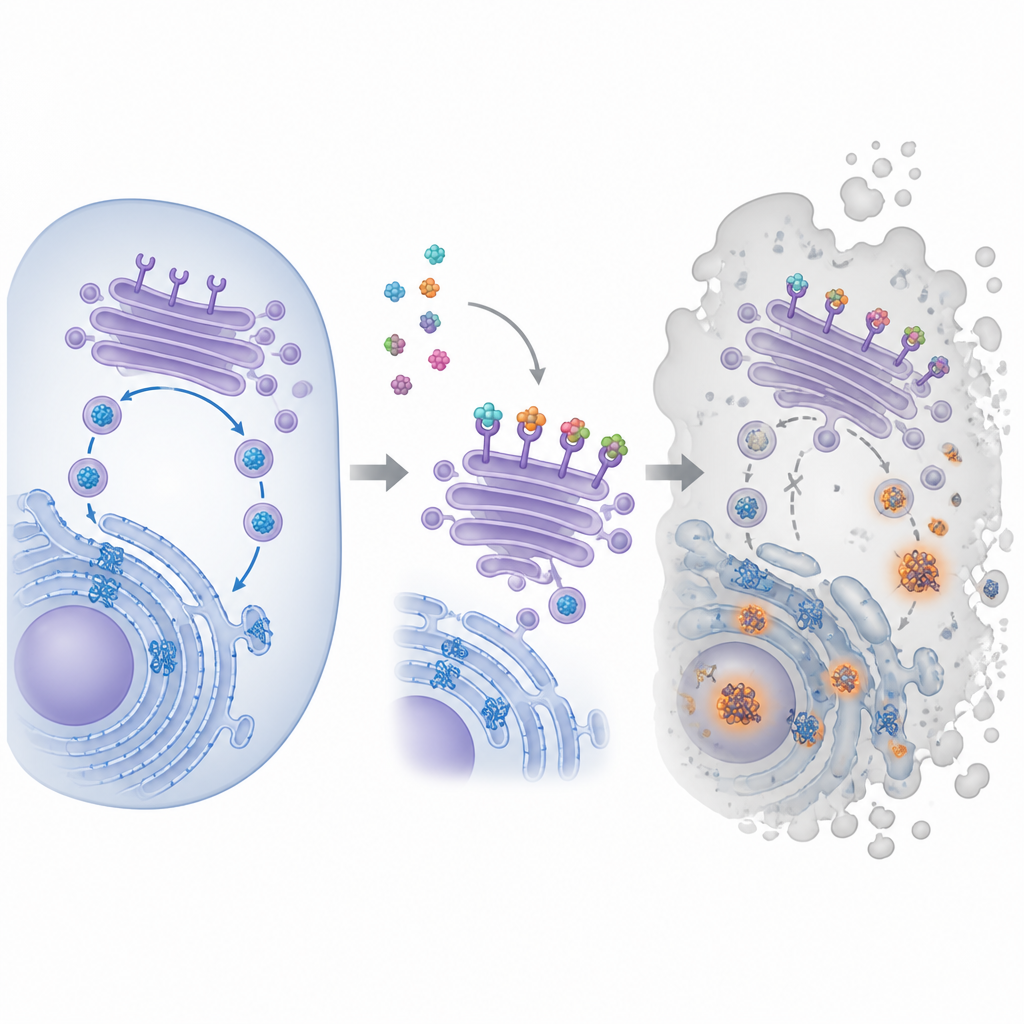
Mała cząsteczka o dużym celu
Związek będący w centrum tego badania nosi nazwę pyra‑metho‑carnil, w skrócie PMC, odkryty pierwotnie w bibliotece produktów naturalnych. Wcześniejsze prace wykazały, że PMC spowalnia wzrost wielu typów komórek nowotworowych, nawet takich z różnymi mutacjami genetycznymi lub opornych na inne leki. Jego główny cel wewnątrz komórek pozostawał jednak nieznany. Aby to ustalić, badacze przyłączyli PMC do magnetycznych kulek, użyli ich do „łowienia” partnerów wiążących w ekstraktach z komórek nowotworowych, a następnie zidentyfikowali wychwycone białka. To podejście wyróżniło rodzinę białek znanych jako receptory KDEL, które znajdują się w wewnętrznym centrum transportowym komórki i pomagają odzyskiwać pewne białka pomocnicze do kompartmentu fałdowania.
Przejęcie trasy recyklingu komórkowego
W komórkach nowe białka są składane w labiryncie zwanym retikulum endoplazmatycznym, a następnie przechodzą przez aparat Golgiego, zestaw błoniastych kieszeni, który sortuje i wysyła je dalej. Receptory KDEL patrolują Golgiego i chwytają białka pomocnicze z krótkim znacznikiem u końca, odsyłając je z powrotem do ponownego użycia, aby maszyny do fałdowania mogły nadążać. Zespół wykazał, że PMC wiąże wszystkie trzy znane ludzkie typy receptorów KDEL i zmienia ich lokalizację w komórkach. Przy użyciu znaczników fluorescencyjnych stwierdzono, że receptory zwykle skoncentrowane po przedniej stronie Golgiego przesunęły się z miejsca po leczeniu PMC. Równocześnie specjalny barwnik ujawnił rosnące skupiska nieprawidłowo złożonych białek, co sygnalizuje, że pętla fałdowania i recyklingu białek zaczyna zawodzić.
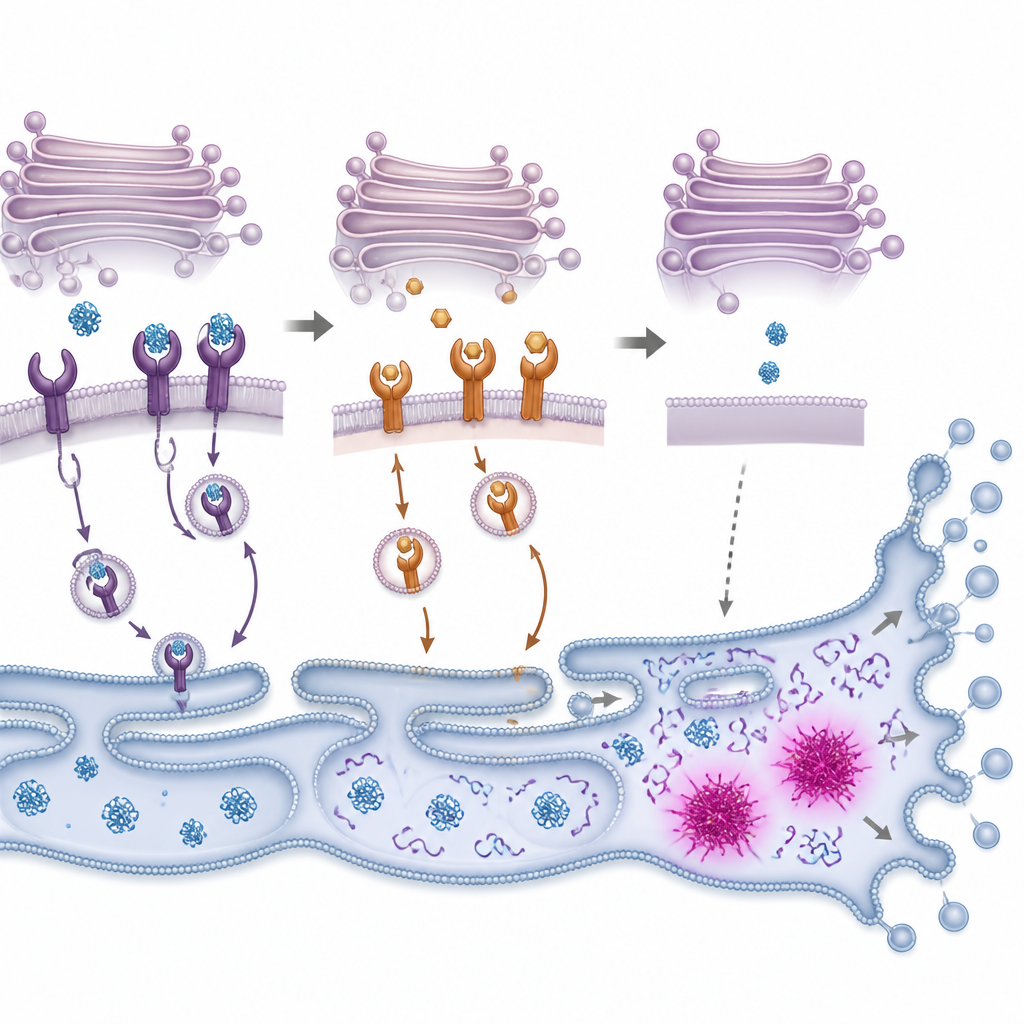
Od przeciążenia białkami do samobójstwa komórki
Kiedy nieprawidłowo złożone białka się kumulują, komórka uruchamia wewnętrzny system alarmowy często nazywany odpowiedzią na niezłożone białka. System ten najpierw próbuje przywrócić równowagę, spowalniając syntezę nowych białek i zwiększając zdolność do fałdowania oraz usuwania uszkodzonych białek. Badacze zaobserwowali, że PMC szybko aktywuje kluczowe elementy tej odpowiedzi w komórkach raka jelita grubego, po czym następuje aktywacja enzymów rozkładających składniki komórkowe w trakcie zaprogramowanej śmierci. Zablokowanie tych enzymów lub zmniejszenie poziomu przełącznika reagującego na stres o nazwie CHOP zwiększało szanse przeżycia komórek narażonych na PMC, choć nie całkowicie. Sugeruje to, że PMC przepycha komórki za punkt krytyczny, w którym mechanizmy łagodzenia stresu zawodzą i przejmują kontrolę ścieżki samodestrukcji.
Uczynienie komórek nowotworowych bardziej podatnymi na stres
Zespół sprawdził także, czy PMC może zwiększyć wrażliwość komórek nowotworowych na inne formy stresu wewnątrzkomórkowego. Połączyli niską, inaczej niegroźną dawkę PMC z tą samą dawką thapsigarginy, związku zaburzającego gospodarkę wapniową i powszechnie stosowanego do wywoływania stresu w kompartmentcie fałdowania białek. W połączeniu oba leki silniej hamowały wzrost komórek niż sama thapsigarginа, a markery stresu wzrosły bardziej, co wskazuje, że PMC obniża próg uszkodzenia. Aby wykazać, że to same receptory KDEL są kluczowe dla tego efektu, naukowcy użyli małych cząsteczek RNA do bezpośredniego zmniejszenia poziomu tych receptorów. Sama ta manipulacja wywołała odpowiedź na stres i spowolniła wzrost komórek nowotworowych w podobny sposób.
Co to może znaczyć dla przyszłych terapii przeciwnowotworowych
Ogólnie rzecz biorąc, badanie sugeruje, że PMC działa poprzez wiązanie się z receptorami KDEL, zaburzanie ich lokalizacji i funkcji, a w konsekwencji sabotaż zdolności komórki do utrzymania porządku w zasobach białkowych. Komórki nowotworowe, które już funkcjonują blisko granicy swoich możliwości przetwarzania białek, wydają się szczególnie wrażliwe na taki rodzaj zakłóceń i można je zmusić do zaprogramowanej śmierci. Choć potrzebne są dalsze badania na zwierzętach i testy bezpieczeństwa, wyniki wskazują receptory KDEL i powiązane szlaki stresu białkowego jako obiecujące punkty wejścia dla nowych leków przeciwnowotworowych oraz dla terapii łączonych, które zwiększają skuteczność istniejących metod opartych na indukcji stresu.
Cytowanie: Yoshida, K., Nishi, K., Kitaguchi, T. et al. Pyra-metho-carnil disrupts cancer cell proteostasis and induces apoptosis by binding to KDEL receptors. Sci Rep 16, 15145 (2026). https://doi.org/10.1038/s41598-026-45604-z
Słowa kluczowe: komórki nowotworowe, fałdowanie białek, stres retikulum endoplazmatycznego, receptory KDEL, apoptoza