Clear Sky Science · zh
基于计算规则的MAPK/ERK系统调控模型
为何微小的细胞开关至关重要
我们的细胞每一秒都要决定是生长、分裂、移动,还是自我销毁。一个核心的决策者是被称为 MAPK/ERK 通路的一连串蛋白质。它也是癌症中最常被扰动的系统之一。尽管教科书常把这条通路描绘为一条简单的接力链,实际上它是一个相互作用密集的网络。该研究构建了这一网络的详细计算模型,旨在回答一个实用问题:同一条通路如何既产生平缓、可调的响应,又能做出明确的开/关决策?序列相近的蛋白如何协作或竞争以控制细胞命运?
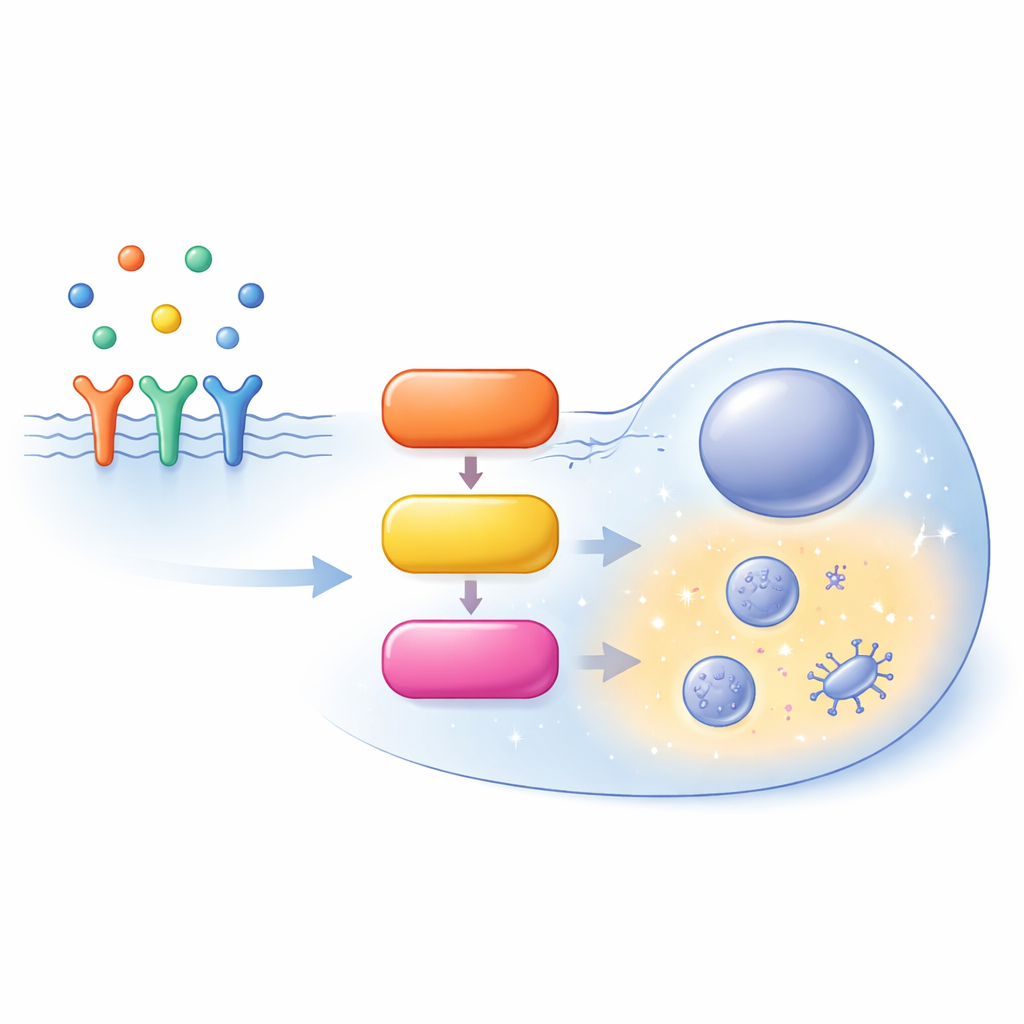
细胞内的一条繁忙高速路
MAPK/ERK 通路从细胞表面开始,生长因子与受体结合并招募一个名为 SOS 的辅助蛋白。SOS 激活 RAS,RAS 是一个附着在细胞膜内侧的小分子开关。活化的 RAS 随后招募一类称为 RAF 的酶家族,RAF 激活 MEK,MEK 再激活 ERK。被激活的 ERK 进一步调控细胞内数百个靶点,决定细胞是增殖、分化、迁移还是进行程序性死亡。这条路径并非直线,而是充满反馈回路、分支以及同一蛋白的并行变体(同工型),使其行为高度依赖于具体背景。
从简单级联到基于规则的网络
为了捕捉这种复杂性,作者采用了基于规则的建模方法,这种方法编码相互作用模式,而不是逐一列举每一种可能的分子状态。模型包含两种 MEK(MEK1 和 MEK2)以及三种 RAF(BRAF、CRAF 和 ARAF),还包括像 14-3-3 蛋白这样的调控伙伴。模型内置了一个增强性反馈(活化的 RAS 提升其激活因子 SOS)和三个抑制性反馈(活化的 ERK 抑制 SOS、RAF 和 MEK)。由于每种蛋白可以以多种方式被修饰和结合,传统模型会出现状态爆炸;基于规则的方法在保持可管理性的同时,仍能表示超过 600 种不同的分子物种和成千上万条反应。
解释渐进与开关式信号
实验证明了一个令人困惑的模式:在 RAS 和 RAF 水平上,活动随生长因子剂量上升而逐渐增加,但在级联底端 ERK 常常以近乎全有或全无的方式被打开。该模型解释称,在低剂量时,RAS 仅在细胞膜的小斑块上被激活。随着剂量增加,更多膜区域转入活化状态。在局部,RAS 开关具有双稳态——它会从关闭突变为开启——但因为只有一部分膜是活跃的,整个细胞范围内的平均 RAS 与 RAF 活性看起来是平滑的。在下游,MEK 和 ERK 的双步激活像一个强大的放大器,使得即便上游活动适中也能产生几乎完全的 ERK 激活,从而呈现出陡峭的开关式响应。来自 ERK 到 SOS 的负反馈则将持续刺激转化为节律性的 ERK 活动脉冲,其周期取决于生长因子强度和反馈强度。
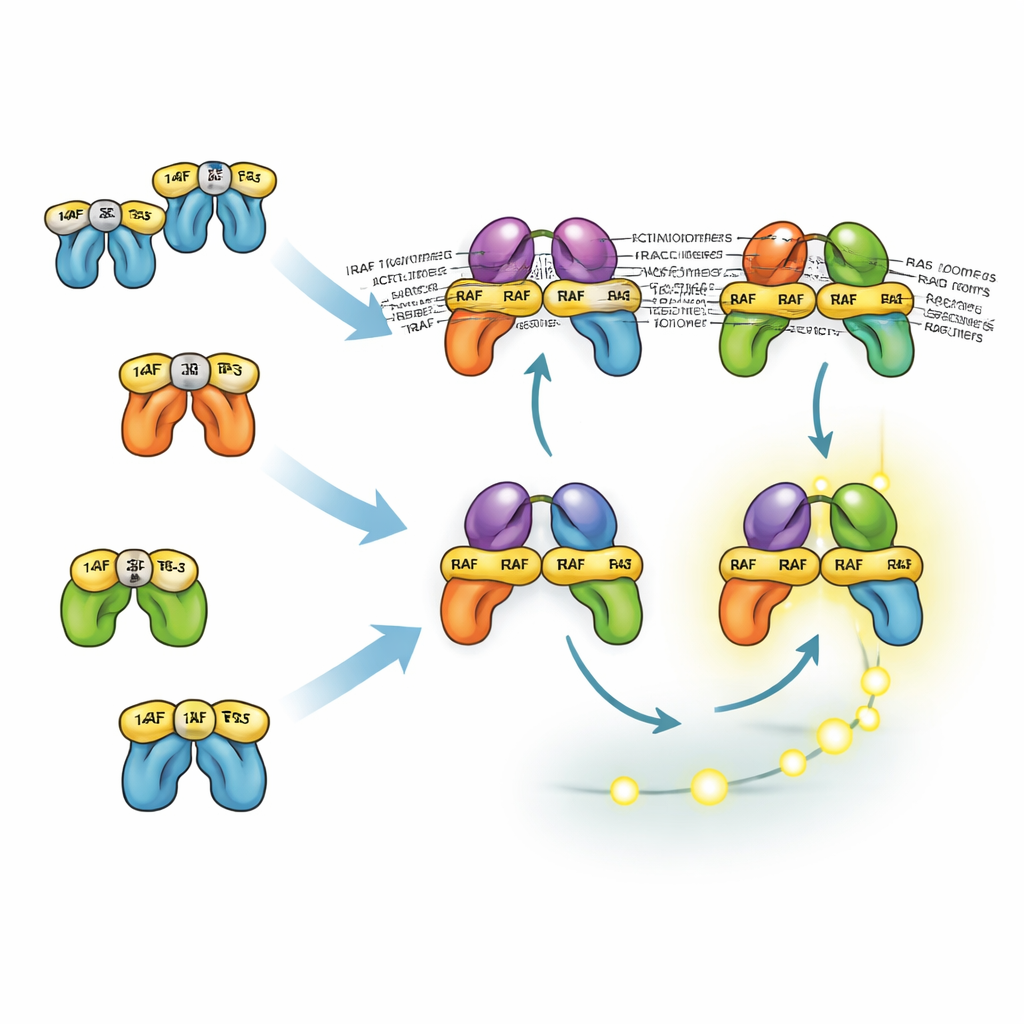
长得相似的蛋白如何分担与划分任务
三种 RAF 同工型表现不同,是因为它们与 14-3-3 蛋白的相互作用方式不同,后者既能将 RAF 锁定为不活跃构象,也能稳定活性 RAF 二聚体。BRAF 在其尾端有主要的 14-3-3 对接位点,使其在仍能结合 RAS 并与 CRAF 或 ARAF 形成二聚体的同时保持与 14-3-3 的关联。这些混合二聚体尤其稳定并且在激活 MEK 方面高效。相比之下,CRAF 和 ARAF 更依赖头端与 14-3-3 的结合,这会阻碍它们被招募到 RAS。因此,缺少 BRAF 的二聚体通常不够稳定且丰度较低。然而模型显示,即使没有 BRAF,细胞仍能产生强烈的 ERK 信号,因为上游的正反馈和下游的放大效应会补偿。这有助于解释为何仅靶向 BRAF 的药物常常只能部分抑制 ERK,需与 MEK 或 ERK 抑制剂联用。
平衡运动、生存与死亡
模型还追踪了 RAF 超出开启 ERK 之外的作用。当在 ERK 驱动的负反馈下二聚体解离时,开放构象的 CRAF 能结合控制细胞运动和存活的伙伴,例如激酶 ROKα 或促凋亡蛋白 MST2。随着生长因子水平和 14-3-3 丰度的变化,平衡会在富含 BRAF 的强驱动 ERK 的二聚体、以 CRAF 和 ARAF 为基础调节运动性的复合体,以及释放 MST2 促使细胞死亡的池之间移动。由于这些平衡对刺激强度的响应是平滑的,而 ERK 的输出可以近乎开关式,这条通路既能调整行为的细微方面,又能做出决定性的命运选择。
这对理解细胞意味着什么
通过将同工型特异性相互作用、局部膜开关和嵌套反馈回路编织在一起,模型展示了同一分子通路如何既能作为调光器,也能作为数字开关。不同组织和肿瘤中观察到的 BRAF、CRAF、ARAF、MEK1、MEK2 与 14-3-3 的含量差异,自然会导致 ERK 信号的不同动力学模式,从脉冲到持续高原不等。这表明相同核心成分的细胞类型特异性连线可以将 MAPK/ERK 通路重用于多样的生理功能,同时也说明有效的治疗需要考虑的不只是单一靶点,而是这些分子开关所处的完整调控环境。
引用: Kocieniewski, P., Lipniacki, T. A computational rule-based model of MAPK/ERK system regulation. Sci Rep 16, 14437 (2026). https://doi.org/10.1038/s41598-026-44353-3
关键词: MAPK ERK 信号传导, RAF 同工型, 14-3-3 调控, 计算通路模型, 细胞命运动力学