Clear Sky Science · es
Un modelo computacional basado en reglas de la regulación del sistema MAPK/ERK
Por qué importan los pequeños interruptores celulares
Cada segundo, nuestras células deben decidir si crecer, dividirse, moverse o autodestruirse. Un tomador de decisiones central es una cadena de proteínas llamada vía MAPK/ERK. También es uno de los sistemas más frecuentemente alterados en el cáncer. Aunque los libros de texto suelen representar esta vía como un relevo sencillo, en realidad es una densa red de elementos interaccionantes. Este estudio construye un modelo informático detallado de esa red para plantear una pregunta práctica: ¿cómo puede una misma vía producir a la vez respuestas suaves y graduadas y decisiones nítidas y todo-o-nada, y cómo cooperan o compiten proteínas muy parecidas para controlar el destino celular?
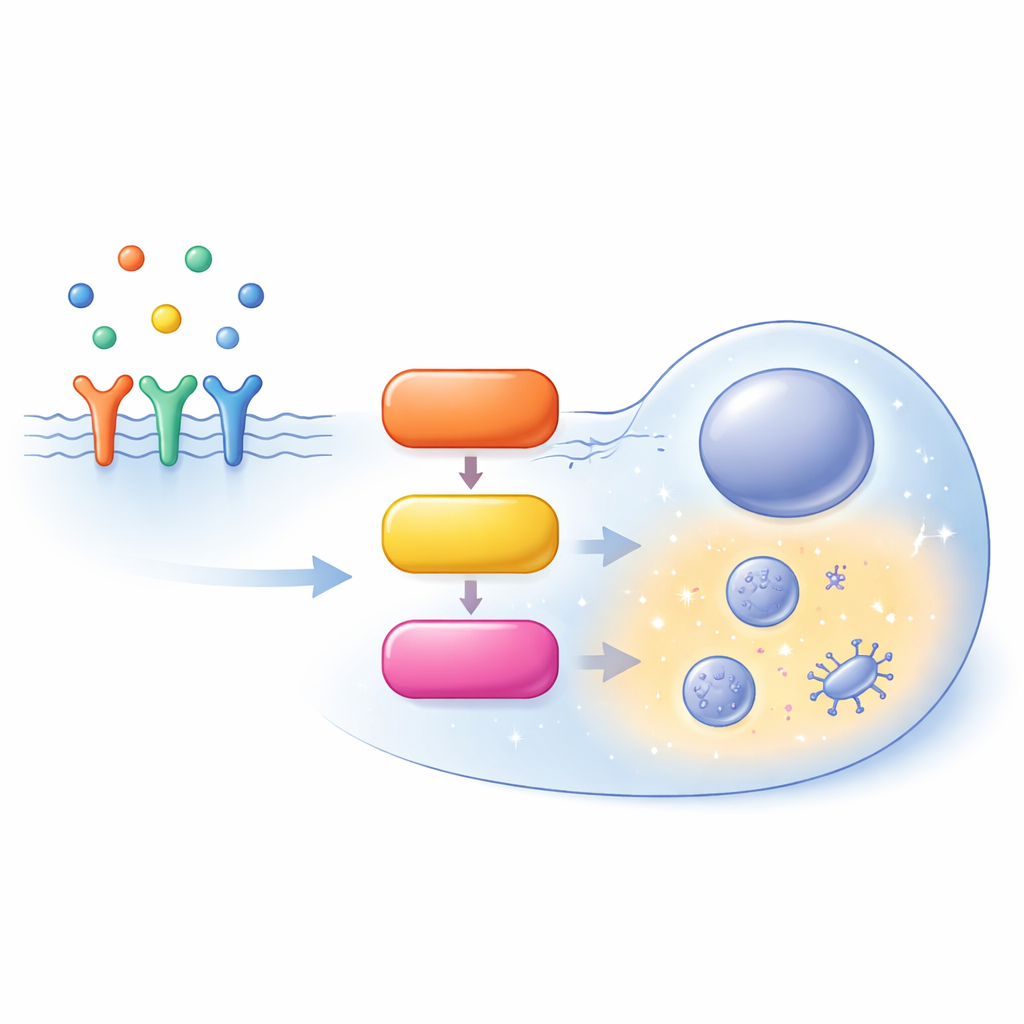
Una carretera concurrida dentro de la célula
La vía MAPK/ERK comienza en la superficie celular, donde factores de crecimiento se unen a receptores y reclutan una proteína auxiliar llamada SOS. SOS activa a RAS, un pequeño interruptor molecular anclado a la cara interna de la membrana celular. RAS activo recluta entonces a una familia de enzimas conocidas como RAF, que activan a MEK, que a su vez activa a ERK. ERK activado regula luego cientos de dianas en toda la célula, determinando si la célula prolifera, se diferencia, migra o sufre muerte programada. Lejos de ser una línea recta simple, esta ruta está llena de bucles de retroalimentación, ramificaciones y variantes paralelas de las mismas proteínas (isoformas), lo que hace que su comportamiento dependa mucho del contexto.
De una cascada simple a una red basada en reglas
Para captar esta complejidad, los autores usan modelado basado en reglas, un método que codifica patrones de interacción en lugar de listar cada posible estado molecular uno por uno. Su modelo incluye dos versiones de MEK (MEK1 y MEK2) y tres versiones de RAF (BRAF, CRAF y ARAF), así como socios regulatorios como las proteínas 14-3-3. También incorpora una retroalimentación reforzadora (donde RAS activo aumenta su propio activador SOS) y tres retroalimentaciones de frenado (donde ERK activo atenúa a SOS, RAF y MEK). Porque cada proteína puede ser modificada y unirse de muchas maneras distintas, un modelo tradicional explotaría en tamaño; el enfoque basado en reglas lo mantiene manejable a la vez que representa más de 600 especies moleculares distintas y miles de reacciones.
Explicando señales graduadas y tipo interruptor
Los experimentos han mostrado un patrón intrigante: a nivel de RAS y RAF, la actividad aumenta gradualmente conforme sube la dosis del factor de crecimiento, pero en el extremo de la cascada ERK a menudo se enciende de forma casi todo-o-nada. El modelo explica esto proponiendo que, a dosis bajas, RAS se activa solo en pequeños parches de la membrana celular. A medida que la dosis aumenta, más porciones de la membrana pasan al estado activo. Localmente, el interruptor de RAS es bistable—salta de forma abrupta de apagado a encendido—pero como solo una fracción de la membrana está activa, la actividad media de RAS y RAF en toda la célula parece suave. A valle, la activación en dos pasos de MEK y ERK actúa como un amplificador potente, de modo que incluso una actividad moderada arriba produce casi una activación completa de ERK, dando una respuesta nítida y tipo interruptor. La retroalimentación negativa de ERK hacia SOS convierte luego la estimulación sostenida en pulsos rítmicos de actividad de ERK, cuyo periodo depende de la intensidad del factor de crecimiento y de la fuerza de la retroalimentación.
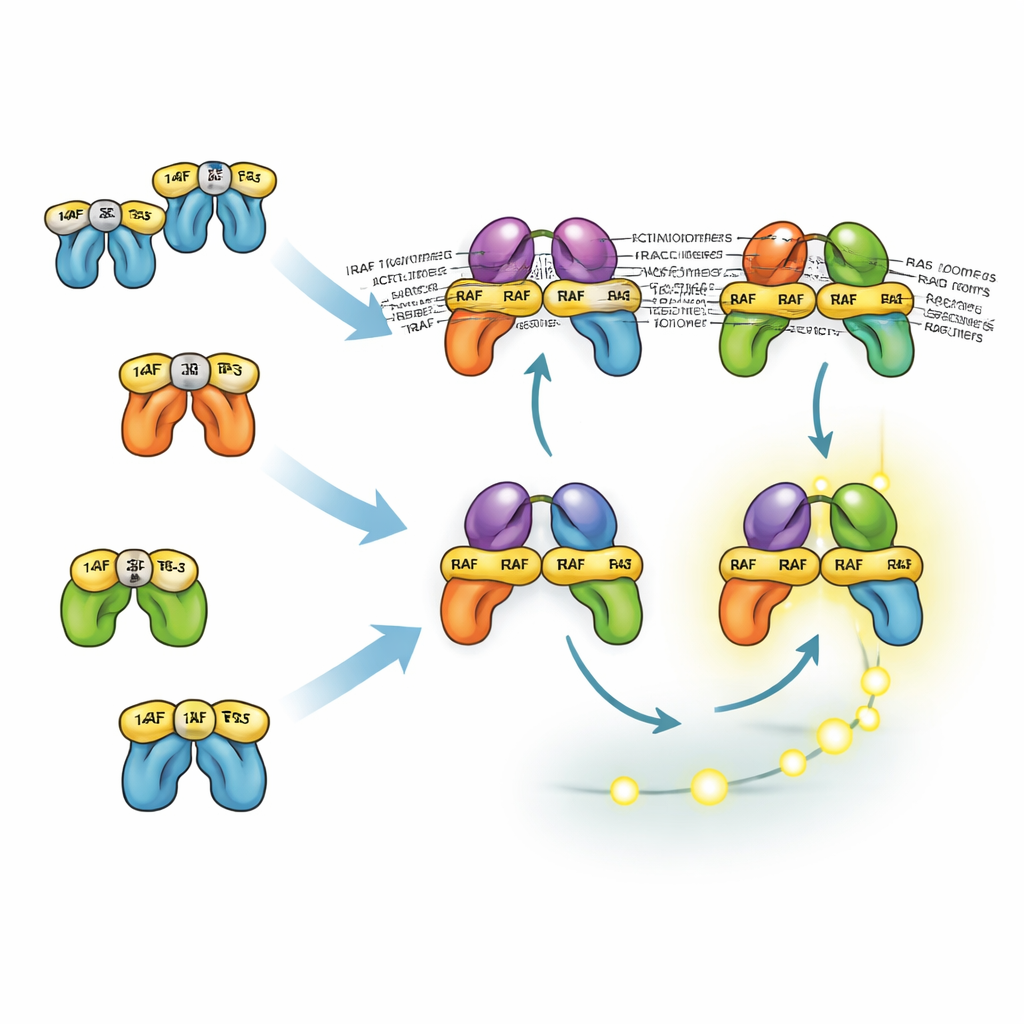
Cómo las proteínas similares comparten y dividen tareas
Las tres isoformas RAF se comportan de modo distinto debido a cómo interaccionan con las proteínas 14-3-3, que pueden tanto bloquear a las moléculas RAF en una conformación inactiva como estabilizar pares activos de RAF. El principal sitio de anclaje de 14-3-3 en BRAF está en su cola, lo que le permite permanecer asociado a 14-3-3 mientras sigue uniéndose a RAS y formando dímeros con CRAF o ARAF. Esos dímeros mixtos son especialmente estables y eficaces en activar MEK. En contraste, CRAF y ARAF dependen más de la unión por el extremo de la cabeza a 14-3-3, lo que bloquea su reclutamiento por RAS. Como resultado, los dímeros que carecen de BRAF son menos estables y por lo general menos abundantes. Aun así, el modelo muestra que, incluso sin BRAF, las células pueden generar señales ERK fuertes porque la retroalimentación positiva upstream y la amplificación downstream compensan. Esto ayuda a explicar por qué los fármacos que apuntan solo a BRAF suelen inhibir ERK de forma parcial y deben combinarse con inhibidores de MEK o ERK.
Equilibrando movimiento, supervivencia y muerte
El modelo también rastrea funciones de RAF que van más allá de encender ERK. Cuando los dímeros se disocian bajo la retroalimentación negativa impulsada por ERK, formas abiertas de CRAF pueden unirse a socios que controlan el movimiento y la supervivencia celular, como la quinasa ROKα o la proteína pro-muerte MST2. A medida que cambian los niveles de factores de crecimiento y de abundancia de 14-3-3, el equilibrio se desplaza entre dímeros ricos en BRAF que estimulan fuertemente ERK, complejos basados en CRAF y ARAF que modulan la motilidad, y reservorios que liberan MST2 para promover la muerte celular. Porque estos equilibrios responden de forma gradual a la intensidad del estímulo mientras que la salida de ERK puede ser casi todo-o-nada, la misma vía puede ajustar aspectos sutiles del comportamiento y aun así tomar decisiones contundentes sobre el destino.
Qué significa esto para entender las células
Al entrelazar interacciones específicas de isoformas, conmutación local en la membrana y bucles de retroalimentación anidados, el modelo muestra cómo una vía molecular puede actuar tanto como regulador gradual (dimmer) como interruptor digital. Las variaciones en las cantidades de BRAF, CRAF, ARAF, MEK1, MEK2 y 14-3-3, tal como se observan entre tejidos y tumores, conducen de forma natural a distintos patrones dinámicos de señalización ERK, desde pulsos hasta mesetas sostenidas. Esto sugiere que el cableado específico del tipo celular de los mismos componentes centrales puede reconvertir la vía MAPK/ERK para roles fisiológicos diversos, y que las terapias eficaces deberán considerar no solo dianas individuales sino el contexto regulatorio completo en el que operan estos interruptores moleculares.
Cita: Kocieniewski, P., Lipniacki, T. A computational rule-based model of MAPK/ERK system regulation. Sci Rep 16, 14437 (2026). https://doi.org/10.1038/s41598-026-44353-3
Palabras clave: Señalización MAPK ERK, Isoformas RAF, Regulación 14-3-3, Modelo computacional de vía, Dinámica del destino celular