Clear Sky Science · it
Un modello computazionale basato su regole della regolazione del sistema MAPK/ERK
Perché contano gli interruttori microscopici della cellula
Ogni secondo, le nostre cellule devono decidere se crescere, dividersi, muoversi o autodistruggersi. Un decisore centrale è una catena di proteine chiamata via MAPK/ERK. È anche uno dei sistemi più frequentemente alterati nel cancro. Sebbene i manuali spesso presentino questa via come una semplice staffetta, in realtà è una fitta rete di componenti interagenti. Questo studio costruisce un modello informatico dettagliato di quella rete per porsi una domanda pratica: come può una singola via produrre contemporaneamente risposte graduali e decisioni nette tutto-o-nulla, e come proteine strettamente correlate cooperano o competono per controllare il destino cellulare?
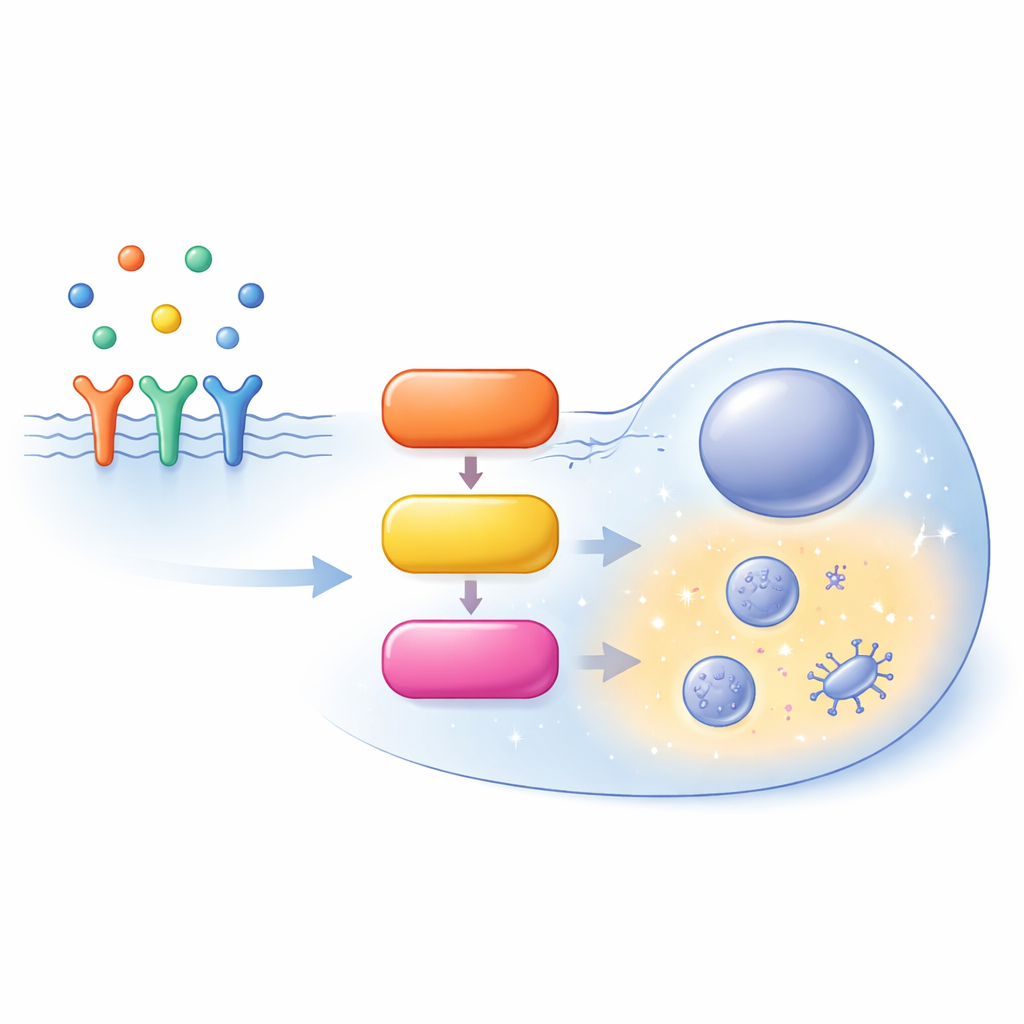
Una trafficata autostrada all’interno della cellula
La via MAPK/ERK inizia alla superficie cellulare, dove i fattori di crescita si legano ai recettori e reclutano una proteina ausiliaria chiamata SOS. SOS attiva RAS, un piccolo interruttore molecolare ancorato alla faccia interna della membrana cellulare. RAS attivo recluta quindi una famiglia di enzimi noti come RAF, che attivano MEK, il quale a sua volta attiva ERK. ERK attivato regola poi centinaia di bersagli in tutta la cellula, determinando se la cellula prolifera, si differenzia, migra o va incontro a morte programmata. Piuttosto che essere una linea retta semplice, questo percorso è pieno di anelli di retroazione, diramazioni e varianti parallele delle stesse proteine (isoforme), rendendo il suo comportamento altamente dipendente dal contesto.
Da una cascata semplice a una rete basata su regole
Per catturare questa complessità, gli autori usano la modellizzazione basata su regole, un metodo che codifica schemi di interazione invece di elencare uno per uno tutti gli stati molecolari possibili. Il loro modello include due versioni di MEK (MEK1 e MEK2) e tre versioni di RAF (BRAF, CRAF e ARAF), oltre a partner regolatori come le proteine 14-3-3. Integra inoltre una retroazione positiva (dove RAS attivo potenzia il suo attivatore SOS) e tre retroazioni inibitorie (dove ERK attivo attenua SOS, RAF e MEK). Poiché ciascuna proteina può essere modificata e legata in molti modi diversi, un modello tradizionale esploderebbe in dimensioni; l’approccio basato su regole lo mantiene gestibile rappresentando comunque oltre 600 specie molecolari distinte e migliaia di reazioni.
Spiegare segnali graduali e a interruttore
Gli esperimenti hanno mostrato un pattern sorprendente: a livello di RAS e RAF, l’attività aumenta gradualmente con la dose del fattore di crescita, ma al fondo della cascata ERK spesso si attiva in modo quasi tutto-o-nulla. Il modello spiega questo proponendo che, a basse dosi, RAS si attiva solo in piccole patch della membrana cellulare. Con l’aumentare della dose, una porzione maggiore della membrana passa allo stato attivo. Localmente, l’interruttore RAS è bistabile—salta bruscamente da spento ad acceso—ma poiché solo una frazione della membrana è attiva, l’attività media di RAS e RAF su tutta la cellula appare graduale. A valle, l’attivazione in due passaggi di MEK e ERK funziona come un potente amplificatore, così che anche un’attività a monte modesta produce un’attivazione quasi completa di ERK, generando una risposta netta e simile a un interruttore. La retroazione negativa da ERK verso SOS converte poi una stimolazione costante in impulsi ritmici di attività ERK, il cui periodo dipende dall’intensità del fattore di crescita e dalla forza della retroazione.
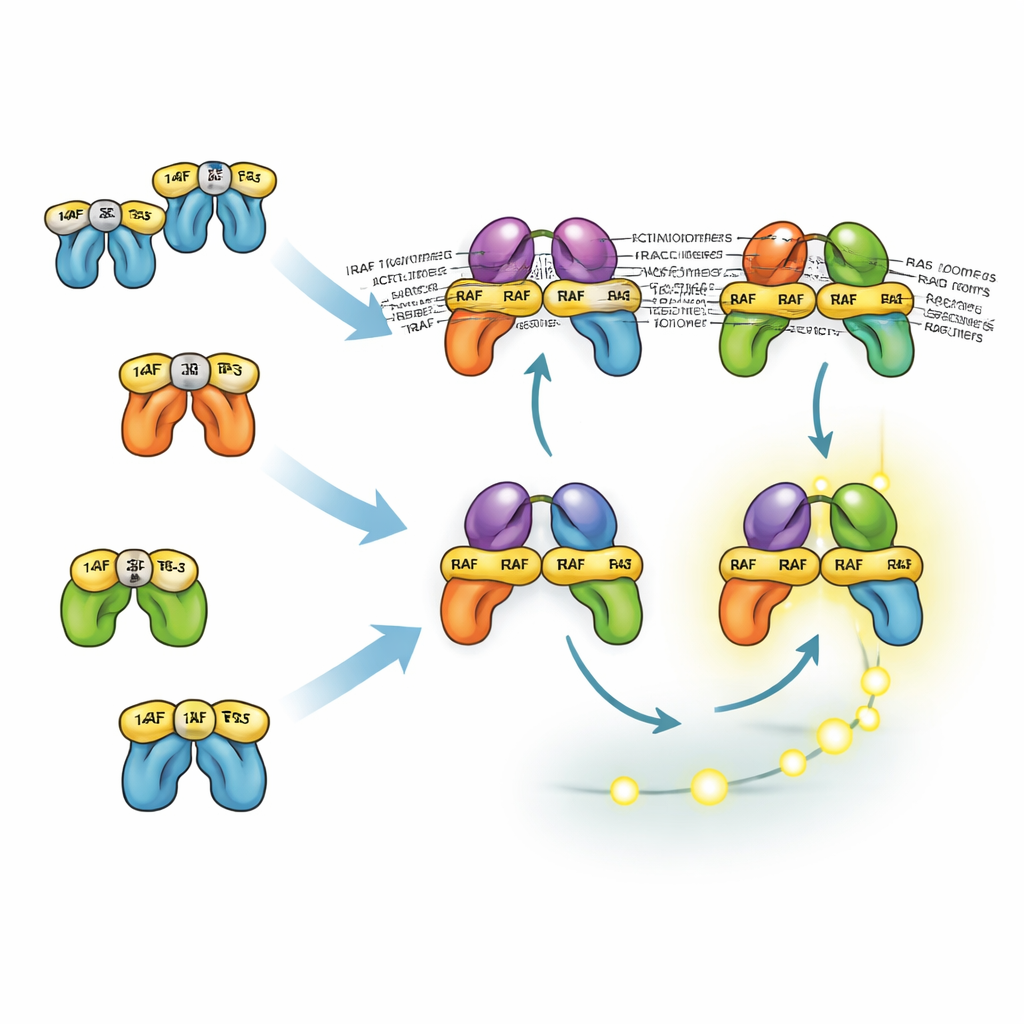
Come proteine simili condividono e dividono i compiti
Le tre isoforme RAF si comportano diversamente a causa del loro modo di interagire con le proteine 14-3-3, che possono sia bloccare le molecole RAF in una conformazione inattiva sia stabilizzare coppie attive di RAF. Il sito di ancoraggio principale di BRAF per 14-3-3 si trova nella sua coda, permettendole di restare associata a 14-3-3 pur legando RAS e formando dimeri con CRAF o ARAF. Questi dimeri misti sono particolarmente stabili ed efficienti nell’attivare MEK. Al contrario, CRAF e ARAF fanno maggiormente affidamento sul legame alla testa con 14-3-3, che ostacola il loro reclutamento da parte di RAS. Di conseguenza, i dimeri privi di BRAF sono meno stabili e di solito meno abbondanti. Tuttavia il modello mostra che, anche senza BRAF, le cellule possono comunque generare forti segnali ERK perché la retroazione positiva a monte e l’amplificazione a valle compensano. Questo aiuta a spiegare perché i farmaci che mirano solo BRAF spesso sopprimono ERK solo parzialmente e devono essere combinati con inibitori di MEK o ERK.
Bilanciare movimento, sopravvivenza e morte
Il modello traccia anche ruoli di RAF che vanno oltre l’attivazione di ERK. Quando i dimeri si disfano sotto la retroazione negativa indotta da ERK, forme aperte di CRAF possono legare partner che controllano movimento e sopravvivenza cellulare, come la chinasi ROKα o la proteina pro-apoptotica MST2. All’aumentare o diminuire dei livelli di fattore di crescita e dell’abbondanza di 14-3-3, l’equilibrio si sposta tra dimeri ricchi di BRAF che guidano fortemente ERK, complessi basati su CRAF e ARAF che modulano la motilità, e pool che liberano MST2 per favorire la morte cellulare. Poiché questi bilanci rispondono in modo graduale alla forza dello stimolo mentre l’uscita di ERK può essere quasi tutto-o-nulla, la stessa via può sintonizzare aspetti sottili del comportamento e al contempo prendere decisioni nette sul destino.
Cosa significa per la comprensione delle cellule
Intrecciando interazioni specifiche per isoforma, commutazione locale della membrana e anelli di retroazione nidificati, il modello mostra come una singola via molecolare possa comportarsi sia da dimmer che da interruttore digitale. Variazioni nelle quantità di BRAF, CRAF, ARAF, MEK1, MEK2 e 14-3-3, come osservato nei diversi tessuti e tumori, portano naturalmente a schemi dinamici diversi della segnalazione ERK, dagli impulsi a plateau sostenuti. Ciò suggerisce che il cablaggio specifico del tipo cellulare degli stessi componenti di base può riconfigurare la via MAPK/ERK per ruoli fisiologici diversi, e che terapie efficaci dovranno considerare non solo singoli bersagli ma l’intero contesto regolatorio in cui operano questi interruttori molecolari.
Citazione: Kocieniewski, P., Lipniacki, T. A computational rule-based model of MAPK/ERK system regulation. Sci Rep 16, 14437 (2026). https://doi.org/10.1038/s41598-026-44353-3
Parole chiave: segnalazione MAPK ERK, isoforme RAF, regolazione 14-3-3, modello computazionale della via, dinamiche del destino cellulare