Clear Sky Science · ru
Вычислительная модель на правилах регуляции системы MAPK/ERK
Почему важны крошечные клеточные переключатели
Каждую секунду клетки решают — расти, делиться, перемещаться или самоуничтожаться. Ключевым «решалой» является цепочка белков, известная как путь MAPK/ERK. Этот путь также часто нарушается при раке. Хотя учебники нередко представляют его как простую цепочку передач, на деле это густая сеть взаимодействующих компонентов. В этом исследовании построена подробная компьютерная модель этой сети, чтобы задать практический вопрос: как один путь одновременно может давать плавные градуированные ответы и резкие «вкл/выкл» решения, и как близкие по структуре белки взаимодействуют или конкурируют, контролируя судьбу клетки?
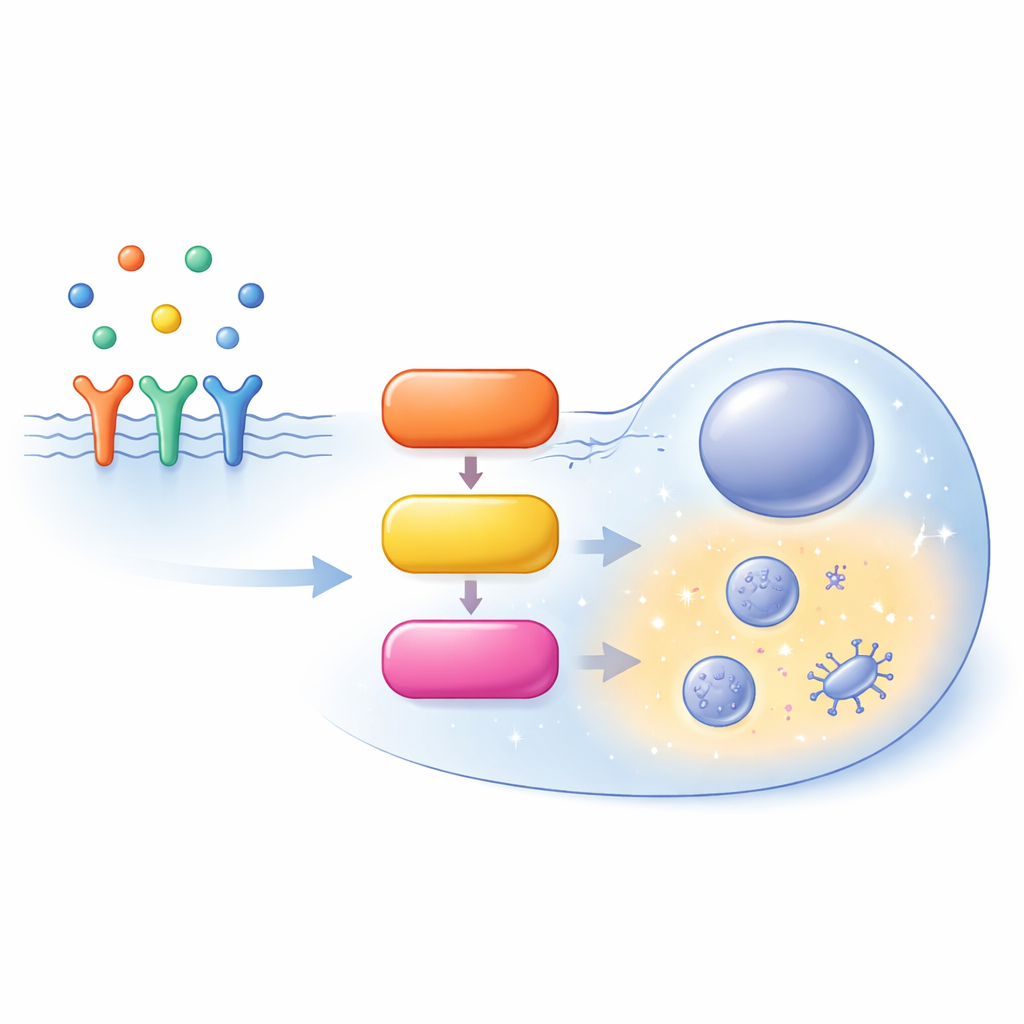
Оживлённая магистраль внутри клетки
Путь MAPK/ERK начинается на поверхности клетки, где ростовые факторы связываются с рецепторами и привлекают вспомогательный белок SOS. SOS активирует RAS — маленький молекулярный переключатель, прикреплённый к внутренней стороне мембраны. Активный RAS привлекает семейство ферментов RAF, которые активируют MEK, а тот, в свою очередь, активирует ERK. Активированный ERK регулирует сотни мишеней по всей клетке, определяя, будет ли клетка пролиферировать, дифференцироваться, мигрировать или проходить запрограммированную смерть. Этот маршрут далёк от простой прямой: он полон петлей обратной связи, ветвлений и параллельных вариантов одних и тех же белков (изоформ), что делает поведение пути сильно зависимым от контекста.
От простой каскадной схемы к сетевой модели на правилах
Чтобы уловить эту сложность, авторы используют правило-ориентированное моделирование — метод, который кодирует шаблоны взаимодействий вместо того, чтобы перечислять все возможные молекулярные состояния по одному. В их модели учтены две версии MEK (MEK1 и MEK2) и три версии RAF (BRAF, CRAF и ARAF), а также регуляторные партнёры, такие как белки 14-3-3. Модель включает одно усиливающее положительное звено (когда активный RAS усиливает своего активатора SOS) и три тормозящих обратных связки (когда активный ERK ослабляет SOS, RAF и MEK). Поскольку каждый белок может модифицироваться и связываться множеством способов, традиционная модель разросталась бы до неуправляемых размеров; подход на правилах остаётся компактным, при этом представляя более 600 различных молекулярных видов и тысячи реакций.
Объяснение градуированных и переключающихся сигналов
Эксперименты показали любопытную закономерность: на уровне RAS и RAF активность растёт постепенно по мере увеличения дозы ростового фактора, тогда как в конце каскада ERK часто включается почти по принципу «всё или ничего». Модель объясняет это так: при низких дозах RAS активируется лишь небольшими участками мембраны. По мере роста дозы всё большая часть мембраны переходит в активное состояние. Локально RAS ведёт себя бистабильно — он скачком переходит из выключенного в включённое состояние — но поскольку активна лишь часть мембраны, средняя активность RAS и RAF по всей клетке выглядит плавной. Далее двухступенчатая активация MEK и ERK действует как мощный усилитель, так что даже умеренная входная активность даёт почти полную активацию ERK, обеспечивая резкий, переключающийся ответ. Негативная обратная связь от ERK к SOS затем преобразует устойчивую стимуляцию в ритмические импульсы активности ERK, период которых зависит от силы ростового фактора и интенсивности обратной связи.
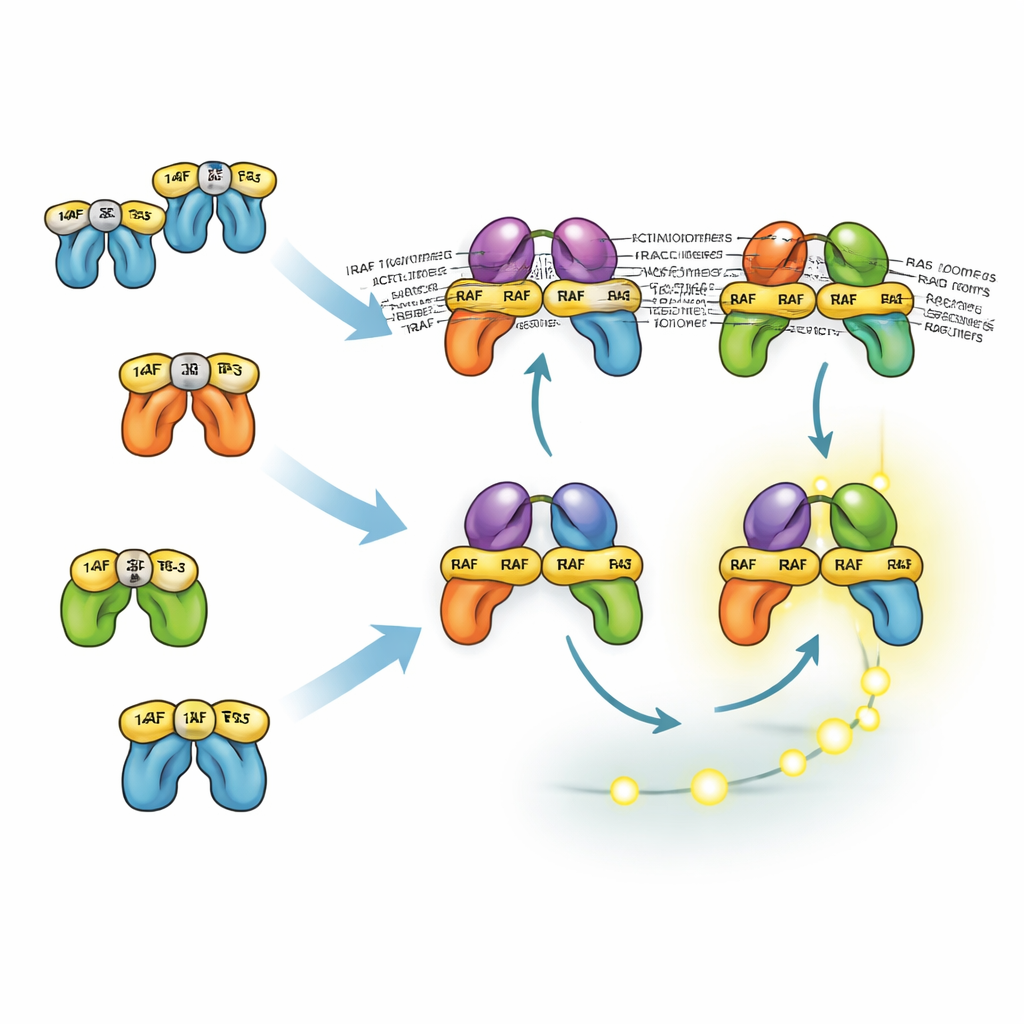
Как похожие белки делят и распределяют задачи
Три изоформы RAF ведут себя по-разному из‑за особенностей взаимодействия с белками 14-3-3, которые могут как «запирать» RAF в неактивной форме, так и стабилизировать активные пары RAF. Главная точка прикрепления 14-3-3 у BRAF находится на хвостовом участке, что позволяет ему оставаться ассоциированным с 14-3-3 и одновременно связываться с RAS и образовывать димеры с CRAF или ARAF. Эти смешанные димеры особенно стабильны и эффективны в активации MEK. Напротив, CRAF и ARAF в большей степени полагаются на «головное» связывание с 14-3-3, которое блокирует их привлечение к RAS. В результате димеры без BRAF менее стабильны и обычно менее многочисленны. Тем не менее модель показывает, что даже при отсутствии BRAF клетки могут генерировать сильные сигналы ERK, поскольку upstream-положительная обратная связь и downstream-усиление компенсируют это. Это помогает объяснить, почему препараты, нацеленные только на BRAF, часто лишь частично подавляют ERK и требуют комбинирования с ингибиторами MEK или ERK.
Баланс между движением, выживанием и смертью
Модель также отслеживает функции RAF, выходящие за рамки простого включения ERK. Когда димеры распадаются под действием ERK-опосредованной негативной обратной связи, открытые формы CRAF могут связывать партнёров, контролирующих движение и выживание клетки, таких как киназа ROKα или белок, способствующий смерти, MST2. По мере изменения уровней ростового фактора и доступности 14-3-3 смещается баланс между димерами, богатыми BRAF и сильно стимулирующими ERK, комплексами на основе CRAF и ARAF, которые модулируют подвижность, и пулами, освобождающими MST2 для продвижения клеточной гибели. Поскольку эти балансы реагируют плавно на силу стимуляции, а выход ERK может быть почти «всё или ничего», один и тот же путь может точно настраивать тонкие аспекты поведения и одновременно принимать решительные решения о судьбе клетки.
Что это значит для понимания клеток
Объединив специфичные для изоформ взаимодействия, локальные мембранные переключения и вложенные петли обратной связи, модель показывает, как один молекулярный путь может служить одновременно диммером и цифровым переключателем. Варьирование уровней BRAF, CRAF, ARAF, MEK1, MEK2 и 14-3-3, наблюдаемое в разных тканях и опухолях, естественно ведёт к разным динамическим паттернам сигнализации ERK — от импульсов до устойчивых плато. Это указывает на то, что типоспецифическая «проводка» одних и тех же базовых компонентов может переназначать путь MAPK/ERK для разнообразных физиологических ролей, и что эффективная терапия должна учитывать не только отдельные мишени, но и полный регуляторный контекст, в котором действуют эти молекулярные переключатели.
Цитирование: Kocieniewski, P., Lipniacki, T. A computational rule-based model of MAPK/ERK system regulation. Sci Rep 16, 14437 (2026). https://doi.org/10.1038/s41598-026-44353-3
Ключевые слова: Сигнализация MAPK ERK, Изоформы RAF, Регуляция 14-3-3, Вычислительная модель путей, Динамика судьбы клетки